 |
|
Эта операция называется омылением, так как соли карбоновых кислот используют для изготовления мыла.
Физические свойства
Низшие кислоты с числом атомов углерода до 3 – легколетучие бесцветные жидкости с характерным острым запахом, смешиваются с водой в любых соотношениях. Большинство кислот С4 – С9 – маслянистые жидкости с неприятным запахом. Растворимость в воде сильно уменьшается с ростом молекулярной массы. Кислоты от С10 и выше – твердые вещества, нерастворимые в воде. Плотности муравьиной и уксусной кислот больше единицы, остальных – меньше единицы. Температура кипения возрастает с увеличением молекулярной массы, при одном и том же числе углеродных атомов кислоты нормального строения кипят выше, чем кислоты с разветвленным углеродным скелетом. Сравнение температур кипения кислот и спиртов с одинаковым числом углеродных атомов показало, что кислоты кипят при значительно более высоких температурах, чем спирты. Это свидетельствует о более высокой ассоциации молекул кислот по сравнению со спиртами за счет образования водородных связей.
Карбоновые кислоты, как и спирты, способны образовывать водородные связи. Если акцептором является достаточно сильное основание, образование водородной связи предшествует полному переносу протона к основанию. По Бренстеду соединение – донор водорода считают «кислотой». Будет ли данное соединение «донором водорода» («кислотой»), зависит от природы «акцептора водорода» («основания»). Чем сильнее основание, тем больше вероятность того, что данное соединение будет вести себя по отношению к нему как кислота:
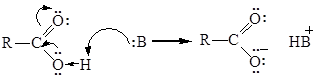
Межмолекулярные водородные связи, возникающие между молекулами карбоновых кислот, настолько прочны, что даже в газообразном состоянии значительная часть молекул существует в виде димеров:

С ростом углеводородной цепи способность кислот к образованию водородных связей уменьшается.
Лекция 21. ХИМИЧЕСКИЕ СВОЙСТВА
КАРБОНОВЫХ КИСЛОТ
Строение карбоксильной группы. Кислотные свойства, константа кислотности, влияние на нее структурных и электронных факторов.Реакции со щелочами и карбонатами, металлами. Карбоксилат-анионы. Реакции замещения гидроксильной группы: взаимодействие схлоридами фосфора и тионилхлоридом. Механизм реакции этерификации. Кислотный катализ.
Группы С=О и О-Н, образующие карбоксильную группу, взаимно влияют друг на друга и проявляют иные свойства, чем в карбонильных соединениях и спиртах.

Карбоновые кислоты имеют три реакционных центра, в соответствии с этим все реакции карбоновых кислот можно разделить на три типа:
- протекающие с разрывом связи О-Н;
- протекающие с разрывом связи С-О;
- протекающие с разрывом связи С-Н.
1. Диссоциация карбоновых кислот. Карбоновые кислоты обладают более выраженными кислотными свойствами, чем спирты, из-за стабилизации карбоксилат-аниона, вызванной делокализацией p-электронов. Другими словами, карбоксилат-ион стабилизирован вследствие резонанса:

Степень делокализации изменяется в ряду RCОО– >> RCOОH >> RОH, RO– (рис. 21.1).
Кислотность выражают количественно через константу диссоциации Ка или через рКа. Константы диссоциации большинства карбоновых кислот составляют около 10-5 (например, для уксусной кислоты 1,8∙10-5), что свидетельствует о довольно высокой концентрации неионизированной формы кислоты. Поэтому большая часть карбоновых кислот относится к слабым кислотам. Кислотность больше для тех кислот, в молекуле которых имеется заместитель, стабилизирующий карбоксилат-анион. Электроноакцепторные заместители в молекуле карбоновой кислоты, оттягивающие электроны от карбоксильной группы, стабилизируют карбоксилат-ион и увеличивают способность его образования, т.е. увеличивают силу кислоты. Электронодонорные заместители оказывают противоположное действие.



Рис. 21.1. Энергия:
а – стабилизация, вызванная делокализацией в RCOOH; b – стабилизация, обусловленная
делокализацией в RCOО-; 1 – гипотетическая кривая, делокализация отсутствует;
2 – истинная кривая, имеется делокализация
Влияние заместителей на кислотность показано в табл. 21.1.
Таблица 21.1
Влияние заместителей на кислотность
| Кислота | рКа |
| СН3СООН | 4.8 |
| СН3СН2СООН | 4.8 |
| ClСН2СООН | 2.9 |
| Cl2СНСООН | 1.3 |
| Сl3CСООН | 0.7 |
| FСН2СООН | 2.6 |
| F3CСООН | 0.2 |
2.Образование солей. Органические кислоты образуют соли с металлами, их оксидами, карбонатами, гидрокарбонатами и щелочами, например:
СН3СООН + NaOH ® СН3СОО-Na+ + H2O
3.Образование галогенангидридов. Под действием галогенидов фосфора (PCl5, PCl3, PBr3) карбоновые кислоты образуют галогенангидриды (гидроксил замещается на галоген):

Хлорангидриды могут также быть получены действием на карбоновые кислоты тионилхлорида:

4. Реакция с аммиаком. При комнатной температуре карбоновые кислоты образуют с аммиаком аммонийные соли, которые при нагревании превращаются в амиды карбоновых кислот:

5. Образование ангидридов кислот:
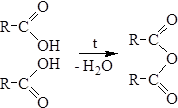
6. Декарбоксилирование. Карбоновые кислоты способны отщеплять диоксид углерода. Как правило, при этом образуется углеводород. Алифатические карбоновые кислоты декарбоксилируются в присутствии различных катализаторов, содержащих медь (например, Cu / хинолин).
CH3СН2СООН ® CH3CH3 + CO2
К реакциям декарбоксилирования относится и синтез Кольбе (см. лекцию 2, ч. 1).
7. Реакция этерификации. В присутствии сильной кислоты (например, серной) карбоновые кислоты дают со спиртами сложные эфиры:
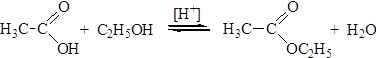
В результате реакции образуется равновесная смесь. Чтобы сместить равновесие в сторону образования продукта, используют большой избыток спирта или удаляют воду по мере ее образования.
Механизм этерификации представляет собой реакцию присоединения –отщепления (нуклеофильное ацильное замещение),его можно представить в виде следующих стадий:
Стадия 1. Атака молекулы карбоновой кислоты протоном:
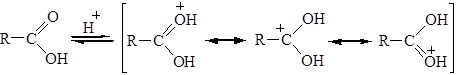
Стадия 2. Нуклеофильная атака молекулой спирта карбонильного атома углерода:
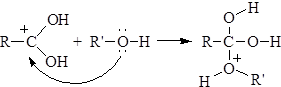
Стадия 3. Изомеризация образовавшегося аддукта:
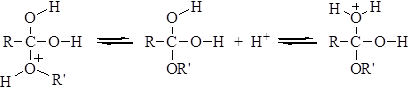
Стадия 4. Отщепление воды и депротонирование продукта реакции:

8. Восстановление кислот (реакции по карбонильной группе). Высшие карбоновые кислоты более доступны, чем соответствующие спирты. Поэтому их восстановление до спиртов имеет важное промышленное значение. Общая схема реакции:

Карбоновые кислоты можно восстановить только с помощью очень сильных восстановителей. Поэтому при восстановлении кислот никогда не получают альдегиды, а только первичные спирты.
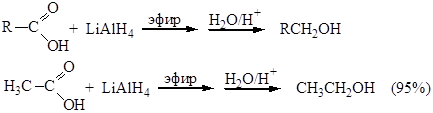
Можно использовать диборан (ВН3)2.

9. Реакции по α-углеродному атому. Атомы водорода в α-положении относительно карбоксильной группы обладают повышенной подвижностью и склонны вступать в различные реакции замещения, характерные и для альдегидов и кетонов.
а) Реакция Гелля – Фольгарда – Зелинского заключается в замещении α-водородного атома на галоген (хлор или бром) в присутствии фосфора:

В качестве продукта получают галогенангидрид α-галоген-замещенной карбоновой кислоты.
б) Сложноэфирная конденсация Кляйзена характерна для сложных эфиров и также основана на повышенной кислотности α-водородных атомов (С-Н кислотность). Реакция катализируется основаниями, например, амидом натрия NaNH2 или этилатом натрия С2Н5О-Na+:

Механизм реакции:


Все стадии конденсации Кляйзена обратимы.
Отдельные представители
Муравьиная кислота. Получают из ее натриевой соли (формиата), которая образуется при пропускании оксида углерода через 15-30% раствор щелочи:
NaOH + CO ® HCOO¯Na+
Суспензию формиата натрия затем разлагают муравьиной кислотой.
Муравьиная кислота применяется для приготовления катализаторов, в медицине и в ряде синтезов. Из ее производных наибольшее значение имеет N,N-диметилформамид HCON(CH3)2. Он является селективным растворителем при выделении ацетилена из газовых смесей и при абсорбции НСl, SO2, CO2 и некоторых других газов.
Муравьиная кислота обладает многими химическими свойствами карбоновых кислот, но ей присущи и некоторые специфические особенности:
1) является хорошим восстановителем (легко окисляется):
HCOOH + HgCl2 ® Hg + CO2 + 2 HCl
Восстановительные свойства муравьиной кислоты объясняются тем, что она в одно и то же время является кислотой и оксиальдегидом, что видно из ее формулы.
2) при нагревании с концентрированной Н2SO4 распадается с образованием воды и СО:
HCOOH ® H2O + CO
3) соли щелочных металлов при сплавлении распадаются с образованием солей щавелевой кислоты (оксалаты):
2 HCOO¯Na+ ® H2 + +Na¯OOC–COO¯Na+
Уксусная кислота. Широко применяется для получения сложных эфиров, уксусного ангидрида, винилацетата, а также в производстве красителей, лекарственных и душистых веществ. Большое практическое значение имеют и соли уксусной кислоты – натрия, алюминия, хрома, железа, меди, свинца и др. В промышленности уксусная кислота получается рядом способов:
1) окислением алканов;
2) окислением этанола;
3) гидратацией ацетилена и окислением получаемого ацетальдегида;
4) уксуснокислым брожением сахарсодержащих растворов.
Высшие жирные кислоты. Встречаются в природе в свободном состоянии и в составе жиров. Низшие члены ряда (С4 – С10) входят в состав липидов молока. Кислоты с длиной цепи С8 – С14 содержатся в маслах некоторых семян. Наиболее распространены в природе пальмитиновая С15Н31СООН и стеариновая С17Н35СООН кислоты.
Лекция 22. ФУНКЦИОНАЛЬНЫЕ ПРОИЗВОДНЫЕ
КАРБОНОВЫХ кислот. двухосновные карбоновЫЕ кислоты. НЕНАСЫЩЕННЫЕ КИСЛОТЫ
Функциональные производные карбоновых кислот: галогенангидриды, ангидриды, сложные эфиры, амиды,нитрилы. Способы получения. Химические свойства производных кислот. Двухосновные карбоновые кислоты. Номенклатура. Кислотность. Особенности физических и химических свойств, декарбоксилирование и ангидридизация. Малоновый эфир. Синтезы на основенатрий-малонового эфира. α,β-ненасыщенные кислоты. Сопряжение карбоксильной группы с двойной связью. Реакции присоединения. Способыполучения акриловой и метакриловой кислот и их эфиров. Двухосновные ненасыщенные кислоты: малеиновая и фумаровая. Малеиновый ангидрид: получение, применение.
ФУНКЦИОНАЛЬНЫЕ ПРОИЗВОДНЫЕ
КАРБОНОВЫХ КИСЛОТ
При взаимодействии карбоновых кислот с нуклеофилами получают соединения общей формулы:

Это функциональные производные карбоновых кислот, общим структурным элементом является ацильная группа  .
.
К функциональным производным карбоновых кислот также относятся соли и нитрилы:
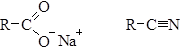
Чтобы дать названия производным карбоновых кислот, надо знать номенклатуру ацильных групп (см. лекцию 20).
ГАЛОГЕНАНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
Это соединения общей формулы:
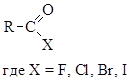
Названия галогенангидридов карбоновых кислот строят следующим образом:

Способы получения
Галогенангидриды карбоновых кислот можно получать следующими способами:
а) из карбоновых кислот действием PCl5, PCl3, PBr3, SOCl2

б) присоединением НХ к кетенам:
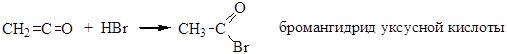
Физические свойства
Галогенангидриды карбоновых кислот – высокополярные соединения. Они имеют довольно высокие температуры кипения и плавления. Галогенангидриды – соединения с резким, раздражающим запахом, что связано с их гидролизом с образованием НХ и карбоновой кислоты.
Химические свойства
На атоме углерода ацильной группы сосредоточен довольно высокий положительный заряд, обусловленный смещением электронной плотности:
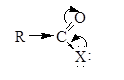
Из строения галогенангидридов следует, что галоген чрезвычайно подвижен в этих соединениях и легко вступает в реакции с нуклеофильными реагентами, протекающими по схеме:

Галогенангидриды являются самыми сильными ацилирующими агентами, т.е. с их помощью можно вводить в молекулы органических соединений ацилы  , замещая атом водорода в спиртах, аминах и ароматических углеводородах на ацильную группу.
, замещая атом водорода в спиртах, аминах и ароматических углеводородах на ацильную группу.
1. Гидролиз галогенангидридов:

Ацилгалогениды гидролизуются водой без применения специальных катализаторов и образуют карбоновые кислоты.
2. Ацилирование спиртов (О-ацилирование, алкоголиз):

3. Ацилирование аминов и их производных (N-ацилирование, аммонолиз) приводит к образованию незамещенных и N‑замещенных амидов:
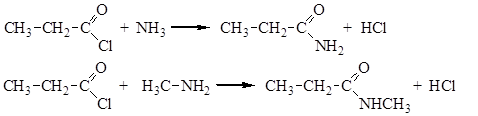
Примером N-ацилирования может служить получение бензанилида:
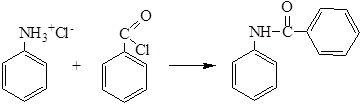
4. Ацилирование ароматических соединений (С-ацилирование, реакция Фриделя-Крафтса):

5. Реакция с солями карбоновых кислот приводит к образованию смешанных ангидридов:

АНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
Ангидриды карбоновых кислот называют согласно названиям соответствующих карбоновых кислот.

Способы получения
1. Ацилирование карбоновых кислот и их солей ацилгалогенидами:
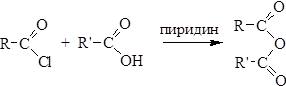
2. Ацилирование карбоновых кислот ангидридами:

3. Взаимодействие карбоновых кислот с кетенами:
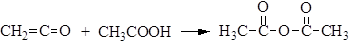
Физические свойства
Ангидриды низших кислот (начиная с уксусной) – жидкости с резким запахом. Уксусный ангидрид имеет т. кип. 140°С, является одним из продуктов промышленного органического синтеза и широко используется в промышленности для ацилирования целлюлозы и аминов.
Химические свойства
1. Гидролиз ангидридов карбоновых кислот протекает легко в присутствии кислот.
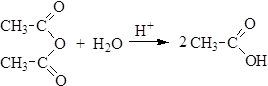
2. Ацилирование спиртов протекает в присутствии кислотных или основных катализаторов. Как ацилирующие агенты ангидриды менее реакционноспособны, чем соответствующие галогенангидриды.
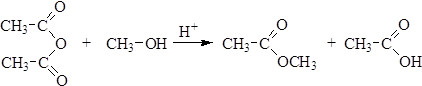
3. Ацилирование аминов и аммиака не требует применения катализаторов.

4.Ацилирование ароматических соединений. Ангидриды широко используют для ацилирования реакционноспособных ароматических соединений в присутствии кислотных катализаторов.

СЛОЖНЫЕ ЭФИРЫ
Сложные эфиры карбоновых кислот имеют важное практическое значение в качестве растворителей, гидравлических жидкостей, смазочных масел, пластификаторов и мономеров.
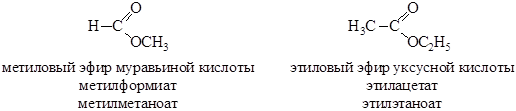
Способы получения
1. Этерификация карбоновых кислот спиртами в присутствии кислотных катализаторов:

2. Ацилирование спиртов ангидридами и хлорангидридами карбоновых кислот:

3. Взаимодействие спиртов с кетенами:
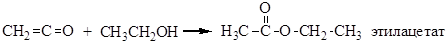
4. Взаимодействие кислот с алкенами и алкинами:

Физические свойства
Сложные эфиры низших спиртов и кислот – жидкости с приятным фруктовым запахом. Используются для ароматизации напитков; в качестве растворителей лаков и красок.

Химические свойства
1. Гидролиз сложных эфиров. Сложные эфиры легко гидролизуются в присутствии сильных кислот или оснований. Гидролиз протекает как реакция, обратная реакции этерификации.
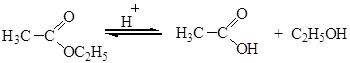
В щелочной среде реакция гидролиза необратима.
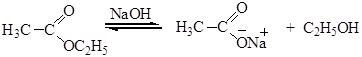
2. Переэтерификация – превращение одного сложного эфира в другой под действием соответствующего спирта в присутствии катализатора (кислотного или основного).
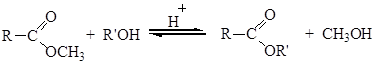
3. Восстановление сложных эфиров. Сложные эфиры восстанавливаются с разрывом связи между карбонильным атомом углерода и кислородом алкоксигруппы:

Восстановление можно проводить под действием натрия в этаноле.
АМИДЫ
Это производные карбоновых кислот, в которых гидроксил в карбоксильной группе замещен на аминогруппу. Общая формула этих соединений:

Амиды можно называть по названию ацилов. По систематической номенклатуре к названию соответствующего алкана добавляется окончание –амид:
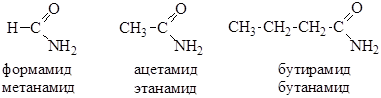
Способы получения
Методы получения амидов мы рассмотрели при изучении химических свойств карбоновых кислот и их галогенангидридов.
Кроме указанных методов, амиды могут быть получены из сложных эфиров, ангидридов и нитрилов.
1. Ацилирование аммиака сложными эфирами:
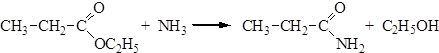
2. Ацилирование аммиака ангидридами кислот:

3. Гидролиз нитрилов:
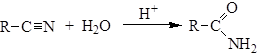
4. Промышленный способ получения формамида:
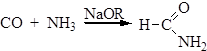
Физические свойства
Простейший амид – формамид – жидкость при обычных условиях, остальные амиды – твердые вещества. Амиды имеют самые высокие температуры плавления из всех производных карбоновых кислот, что связано с образованием сильных межмолекулярных водородных связей.
Химические свойства
1. Гидролиз амидов. При нагревании амидов с водой происходит их гидролиз, в результате которого в зависимости от рН среды образуются карбоновые кислоты или их соли:



2. Дегидратация амидов происходит при нагревании с Р2О5 и приводит к образованию нитрилов:

3. Замещение атомов водорода на металл. Основные свойства аминогруппы в амидах сильно понижены, она проявляет кислотные свойства – замещение атомов водорода на металл:
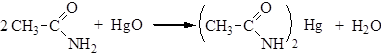
4. Действие азотистой кислоты на амиды приводит к образованию карбоновых кислот:
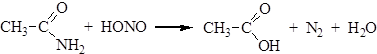
5. Образование аминов (перегруппировка Гофмана). При взаимодействии со щелочными растворами галогенов амиды подвергаются расщеплению по Гофману с получением аминов, содержащих на один атом углерода меньше, чем исходный амид:

НИТРИЛЫ
Важнейшими представителями нитрилов являются ацетонитрил СН3СN (применяется как полярный растворитель) и акрилонитрил CH2=CH-CN (мономер для получения синтетического волокна нитрона и для производства дивинилнитрильного синтетического каучука, обладающего масло– и бензостойкостью).
Способы получения
Основным способом получения нитрилов является дегидратация амидов на кислотных катализаторах:

Нитрилы также образуются по реакции нуклеофильного замещения галогена в галогеналканах (см. лекцию 12).
Химические свойства
1. Гидролиз нитрилов в кислой и щелочной среде проходит с образованием амидов и далее до карбоновых кислот или их солей:

2. Алкоголиз нитрилов приводит к образованию иминоэфиров, также являющихся производными карбоновых кислот:
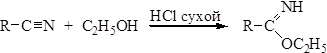
3. Восстановление нитрилов позволяет получать амины с тем же числом углеродных атомов, что и в соответствующей карбоновой кислоте:

СОЛИ КАРБОНОВЫХ КИСЛОТ
По систематической номенклатуре названия солей карбоновых кислот образуют путем добавления окончания –оат к названию соответствующего алкана и названия противоиона (металла или аммония). Используют также тривиальные названия карбоксилат-анионов, добавляя к ним название металла:

Методы получения солей рассмотрены выше.
С химическими свойствами солей мы знакомились при рассмотрении методов получения алканов (электролиз по Кольбе и декарбоксилирование), альдегидов и кетонов (пиролиз кальциевых и бариевых солей).
ДВУХОСНОВНЫЕ НАСЫЩЕННЫЕ КИСЛОТЫ
Двухосновные предельные (насыщенные) кислоты имеют общую формулу СnН2n(СООН)2. Из них важнейшими являются:
HOOC-COOH – щавелевая, этандикарбоновая кислота;
HOOC-СН2-COOH – малоновая, пропандикарбоновая кислота;
HOOC-СН2-СН2-COOH – янтарная, бутандикарбоновая кислота;
HOOC-СН2-СН2-СН2-COOH – глутаровая, пентандикарбоновая кислота;
HOOC-СН2-СН2-СН2-СН2-COOH – адипиновая, гександикарбоновая кислота.
Способы получения
Общие методы получения двухосновных кислот аналогичны способам получения одноосновных кислот (окисление гликолей, гидролиз динитрилов, синтез Кольбе – см. лекцию 20). Существуют и специфические способы получения двухосновных карбоновых кислот.
1. Окисление оксикислот:

2. Окисление циклоалканов. Это промышленный способ получения адипиновой кислоты:
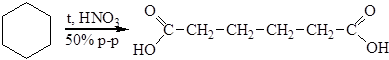
Побочно образуются также янтарная и щавелевая кислоты. Адипиновая кислота применяется для синтеза волокна найлон 6,6 и пластификаторов.
Физические свойства
Дикарбоновые кислоты – твердые вещества. Низшие кислоты хорошо растворимы в воде, но плохо – в органических растворителях.
Химические свойства
Двухосновные кислоты более сильные, чем одноосновные, они характеризуются двумя константами диссоциации – Ка1 и Ка2.

Диссоциация первой карбоксильной группы протекает легче. Это особенно заметно для щавелевой и малоновой кислот и связано с тем, что неионизированная карбоксильная группа проявляет электроноакцепторный индуктивный эффект по отношению к ионизированной карбоксильной группе и стабилизирует тем самым образующийся карбоксилат-анион.
Дикарбоновые кислоты, в которых две карбоксильные группы разделены цепью из шести и более атомов, проявляют свойства, аналогичные монокарбоновым кислотам. Механизм реакций образования диамидов, сложных диэфиров и др. для дикарбоновых кислот тот же, что и для монокарбоновых кислот.
1. Отношение к нагреванию. Примером необычного поведения дикарбоновых кислот, обусловленного наличием двух карбоксильных групп, могут служить реакции, протекающие при нагревании.
Так, щавелевая кислота при нагревании до 150°С отщепляет диоксид углерода с образованием муравьиной кислоты:
НООС–СООН ® НСООН + СО2
Малоновая кислота и ее моно– и дизамещенные гомологи при нагревании несколько выше их температур плавления отщепляют СО2 с образованием уксусной кислоты или ее моно– и дизамещенных гомологов:
НООС–СН2–СООН ® СН3СООН + СО2
НООС-СН(СН3)-СООН ® СН3СН2СООН + СО2
НООС-С(СН3)2-СООН ® (СН3)2СНСООН + СО2
Дикарбоновые кислоты, содержащие четыре или пять атомов углерода между карбоксильными группами (янтарная и глутаровая кислоты), при нагревании отщепляют воду и образуют циклические ангидриды:
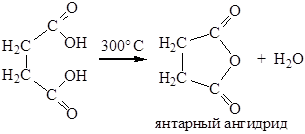
Подобные циклические соединения получают и из амидов:

2. Пиролиз кальциевых и бариевых солей. При пиролизе кальциевых или бариевых солей адипиновой, пимелиновой и пробковой кислот происходит отщепление СО2 и образуются циклические кетоны:

3. Синтезы на основе малонового эфира. Имеют большое значение в органической химии.
Атом водорода метиленовой группы, находящейся между ацильными группами диэтилового эфира малоновой кислоты (малоновый эфир), обладает кислотными свойствами и дает натриевую соль с этилатом натрия. Эту соль (натрий – малоновый эфир) алкилируют галогеналканами по механизму нуклеофильного замещения SN2. На основе натрий-малонового эфира получают одно– и двухосновные кислоты:
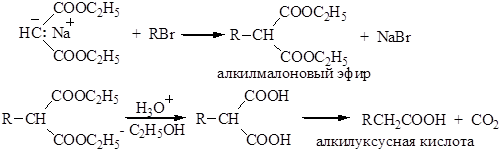
Синтез на основе малонового эфира является одним из лучших способов получения карбоновых кислот. Планирование синтеза карбоновых кислот с использованием малонового эфира сводится к выбору подходящего алкилгалогенида. Для этого получаемую кислоту рассматривают как моно– или диалкилуксусную кислоту. При действии галогенангидридов карбоновых кислот с последующим гидролизом и декарбоксилированием из натрий-малонового эфира получают кетоны:

НЕНАСЫЩЕННЫЕ ОДНООСНОВНЫЕ
KAPБОHOBЫE КИСЛОТЫ
Непредельные одноосновные кислоты этиленового ряда имеют общуюформулу CnH2n-1COOH, ацетиленового и диенового рядов – CnH2n-3CООH. Примеры непредельных одноосновных кислот:
CH2=СНCОOH – акриловая кислота, пропеновая кислота;
СН2=СНСН2СООН – винилуксусная кислота, 3-бутеновая кислота;
СН3СН=СНСООН – кротоновая кислота, 2-бутеновая кислота;
СН2=С(СН3)СООН – α-метилакриловая кислота, метакриловая кислота, метилпропеновая кислота;
СН≡С-СООН – пропиоловая кислота, пропиновая кислота;
СН3СН2СН=СНСН2СН=СН(СН2)7СООН – линоленовая кислота.
Получают непредельные кислоты окислением α,β-ненасыщенных альдегидов, отщеплением галогеноводородов от α– и β-галоген-карбоновых кислот, дегидратацией β-гидроксикарбоновых кислот, гидролизом непредельных нитрилов, например:

Непредельные одноосновные кислоты отличаются от предельных большими константами диссоциации. Причиной их большей кислотности является относительное увеличение электроотрицательности атомов углерода заместителя, связанного с карбоксильной группой, в ряду Сsp3 < Сsp2 < Сsp, что приводит к повышению устойчивости карбоксилат-аниона, образующегося при диссоциации карбоновой кислоты, за счет отрицательного индуктивного эффекта ненасыщенного заместителя (насыщенный углеводородный радикал, напротив, обладает положительным индуктивным эффектом и дестабилизирует анион). Ненасыщенные кислоты образуют все обычные производные кислот – соли, ангидриды, галогенангидриды, амиды, сложные эфиры. За счет кратных связей они вступают в реакции присоединения, окисления и полимеризации.
Благодаря взаимному влиянию карбоксильной группы и кратной связи присоединение галогеноводородов к α,β-непредельным кислотам происходит таким образом, что водород направляется к наименее гидрогенизированному атому углерода, т.е. присоединение протекает по направлению 1,4 с последующей перегруппировкой:

Этиленовые кислоты типа акриловой кислоты и их эфиры значительно легче подвергаются полимеризации, чем соответствующие им углеводороды.
Отдельные представители
Акриловую кислоту получают из этилена (через хлоргидрин или оксид этилена), гидролизом акрилонитрила или окислением пропилена, что более эффективно. В технике используются производные акриловой кислоты – ее эфиры, особенно метиловый (метилакрилат). Метилакрилат легко полимеризуется с образованием прозрачных стекловидных веществ, поэтому его применяют в производстве органического стекла и других ценных полимеров.
Метакриловая кислота и ее эфиры получают в больших масштабах методами, сходными с методами синтеза акриловой кислоты и ее эфиров. Исходным продуктом является ацетон. Из него получают ацетонциангидрин, который затем подвергают дегидратации и омылению с образованием метакриловой кислоты. Этерификацией метиловым спиртом получают метилметакрилат, который при полимеризации или сополимеризации образует стекловидные полимеры (органические стекла) с весьма ценными техническими свойствами.
НЕНАСЫЩЕННЫЕ ДВУХОСНОВНЫЕ
KAPБОHOBЫE КИСЛОТЫ
Наиболее простые ненасыщенные двухосновные кислоты –
фумаровая и малеиновая – имеют одну и ту же структурную формулу, но разные пространственные конфигурации. Фумаровая кислота – транс-, а малеиновая – цис-изомер:

Эти кислоты отличаются по физическим свойствам. Фумаровая кислота имеет т. пл. 287-288°С, плохо растворима в воде, а малеиновая плавится при 130°С, очень хорошо растворима в воде.
Малеиновая кислота значительно сильнее фумаровой, их константы диссоциации соответственно равны 117∙10-2 и 9,3∙10-2.
Обе кислоты получаются при нагреве яблочной кислоты, образование того или иного изомера зависит от режима нагревания:
НООС-СН2-СНОН-СООН ® НООС-СН=СН-СООН + Н2О
В промышленности малеиновую кислоту получают каталитическим окислением бензола или нафталина кислородом воздуха.
Эти кислоты идентично ведут себя в реакциях присоединения по двойной связи водорода, галогенов, галогеноводородов.
Обе кислоты способны образовывать соли, сложные эфиры, амиды и другие производные кислот. В отличие от фумаровой, малеиновая кислота легко образует циклический ангидрид:
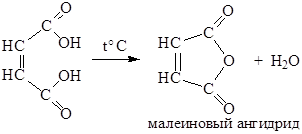
Малеиновый ангидрид служит реактивом для обнаружения 1,3-диеновых соединений: он легко вступает в реакцию диенового синтеза. В последние годы он приобрел широкое применение в производстве полиэфирных смол, а также для получения сополимеров (со стиролом, акриловым и метакриловым эфирами).
Малеиновая кислота под действием брома, йода, азотистой кислоты легко переходит в более устойчивую фумаровую кислоту. Обратный переход осуществляется под действием ультрафиолетовых лучей.
Лекция 23. МОНОКАРБОНОВЫЕ КИСЛОТЫ
АРОМАТИЧЕСКОГО РЯДА
Монокарбоновые кислоты, изомерия, номенклатура. Способы получения: из ароматических углеводородов, спиртов, альдегидов, кетонов, из тригалогенпроизводных и нитрилов, реакцией Канниццаро, реакцией ацилирования, реакцией Гриньяра. Физические свойства. Химические свойства. Уравнение Гаммета. Функциональные производные ароматических кислот. Отдельные представители.
Ароматическими карбоновыми кислотами называются производные бензола, содержащие карбоксильные группы, непосредственно связанные с ароматическим ядром. Кислоты, содержащие карбоксильные группы в боковой цепи, рассматриваются как жирноароматические. По количеству карбоксильных групп ароматические кислоты делятся на моно-, дикарбоновые и т.д. Название кислоты производится от ароматического углеводорода (бензойная кислота, п-толуиловая кислота).
Способы получения
Методы получения ароматических карбоновых кислот можно разделить на две группы: методы, основанные на превращении функциональных групп, и методы, основанные на введении карбоксильной группы.
1. Превращение функциональных групп
1.1. Окисление ароматических углеводородов. Для синтеза ароматических кислот наиболее подходят метильные гомологи бензола, радикально-цепное окисление которых протекает через стадии первичного гидропероксида и альдегида:

Жидкофазным окислением метилбензолов кислородом воздуха в промышленности получают моно– и дикарбоновые ароматические кислоты.
Окисление можно проводить перманганатом калия в кислой среде:
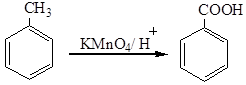
1.2. Окисление спиртов, альдегидов и кетонов. Ароматические спирты, альдегиды и кетоны окисляются легче, чем углеводороды. В качестве окислителя может выступать щелочной раствор перманганата калия, ароматические альдегиды окисляются аммиачным раствором оксида серебра:
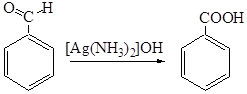
Окисление кетонов обычно ведут с помощью гипохлоритов (галоформная реакция):

1.3. Реакция Канниццаро:

1.4. Гидролиз галогенпроизводных. Этот способ широко применяется в технике. При хлорировании толуола получают три вида галогенпроизводных: хлористый бензил для производства бензилового спирта; хлористый бензилиден – для получения бензальдегида; бензотрихлорид перерабатывается на бензойную кислоту.

Гидролиз нитрилов

2. Введение карбоксильной группы в ароматическое ядро
2.1. Применение фосгена (боевое отравляющее вещество!) дает возможность получить хлорангидрид кислоты, а затем кислоту (или ряд ее производных):
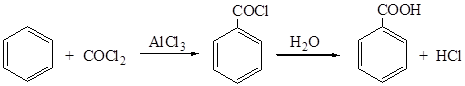
Реакция протекает по механизму электрофильного ароматического замещения, катализируемого кислотами Льюиса.