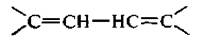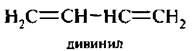|
|
Строение циклоалканов
Циклоалканы представляют собой в определенной степени жесткие структуры.
Для циклоалканов характерны следующие виды напряжений:
1) торсионное (Питцеровское) напряжение – связано со взаимодействием химических связей в заслоненной или частично заслоненной конформациях;
2) напряжение Ван-дер-Ваальса – обусловлено взаимным отталкиванием заместителей при сближении на расстояние, близкое сумме их ван-дер-ваальсовых радиусов;
3) угловое (Байеровское) напряжение – присуще отдельным циклоалканам и связано с отклонением валентных углов между углерод-углеродными связями в цикле от нормального (тетраэдрического) значения.
Теория напряжения циклов была предложена немецким химиком-органиком А. Байером в 1885 г. Согласно этой теории циклоалканы представляют собой плоские многоугольники. Единственным фактором, определяющим прочность цикла, считалось наряжение, вызванное отклонением внутренних валентных углов цикла по сравнению с тетраэдрическим углом.
Если рассматривать форму циклоалканов в виде простых геомет-рических фигур, имеющих плоское строение, то можно отметить, что при переходе от одного цикла к другому происходит изменение валентного угла.
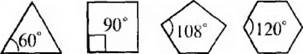
Чем значительнее отклонение, тем выше угловое напряжение и менее устойчивникл.
В соответствии с вышеприведенным, трехчленный цикл менее устойчив, чем четырехчленный, а последний – менее устойчив, чем пя~ тичленный. Эти представления подтверждались накопленным к тому времени экспериментальным материалом. Однако для шестичлеиного цикла экспериментальные данные вступали в противоречия с теорией. Шестичленные циклы (внутренний угол 120°), имеющие значительное отклонение валентных углов от тетраэдрического, оказались устойчивее пятичленных, в которых внутренние углы наиболее близки к тетраэдрическим.
Причиной несоответствия теории Байера с экспериментальным материалом явилось ошибочное представление о плоском строении циклов, В действительности же циклоалканы (исключая циклопропан) не имеют плоского строения.
Пространственное строение циклоалканов определяется разной конформационной подвижностью углеродных атомов, зависящей от числа звеньев в цикле, Молекула любого циклоалкана стремится принять в пространстве такую форму (конформацию), в которой сумма углового, торсионного и ван-дер-ваальсового напряжений была бы минимальной.
Наиболее жесткую структуру имеет циклопропан. В соответствии с правилами геометрии три точки всегда лежат в одной плоскости. Именно поэтому молекула циклопропана имеет плоское строение. Атомы водорода в данной молекуле находятся в заслоненной конформации, что и обуславливает сильное торсионное напряжение. Свободное вращение относительно углерод-углеродных связей невозможно. Внутренние валентные углы в молекуле циклопропана сильно отклонены от тетраэдрического значения, в результате чего и возникает большое угловое напряжение. Искажение валентных углов при 5/^-гибридизации орбиталей углеродных атомов должно составлять α = (109°28' - 60°):2 = 24*44'.
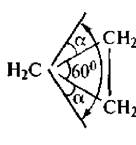
В действительности в молекуле циклопропана валентный угол равен 106°. Согласно квантовохимическнм представлениям изменение угла является результатом изменения гибридизации атомов углерода. Гибридизация орбиталей в молекуле циклопропана ближе к sp2-гибридизации алкенов, чем к sp3-гибридизации алканов (промежуточное положение).
Вследствие взаимного отталкивания электронных облаков углерод-углеродных связей максимальная электронная плотность перекрывающихся орбиталей атомов углерода в молекуле циклопропана расположена не по прямой, соединяющей центры связываемых атомов, а за пределами треугольника молекулы.
Образующиеся связи называют «банановыми» или τ-(греч. «тау») связями. Они занимают промежуточное положение между σ и π-связями. Образование τ-связей выгодно, так как валентные углы увеличиваются до 106° (вместо теоретически рассчитанных 60°) и снижается угловое напряжение молекулы.
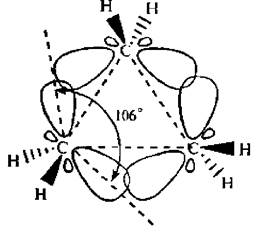
Рис. 7.1. Образование «банановых» связей в молекуле циклопропана
Четырехчленный цикл, в отличие от трехчленного, все же обладает незначительной гибкостью. Валентные углы искажены меньше, чем в трехчленном цикле, несколько ниже и угловое напряжение. Один из углерод ных атомов циклобутана выходит из плоскости трех атомов на угол 25–30% что приводит к уменьшению торсионного напряжения цикла.
В пятичленном цикле практически отсутствует угловое напряжение (отклонение внутренних валентных углов от тетраэдрического составляет менее 1°). Однако в плоском пятичленном цикле связи С–Н находятся в заслонен ной конформаций, что обуславливает значительное торсионное напряжение. Каждый из пяти углеродных атомов циклопента-на, стремясь уменьшить торсионное напряжение в цикле, поочередно выходит из плоскости, в которой расположены четыре оставшихся атома углерода. Кольцо находится в непрерывном волнообразном движении – псевдоврашении. Эта неплоская осциллирующая структура называется конформацией «конверта». В конформаций «конверта» угловое напряжение увеличивается, однако это в полной мере компенсируется снижением торсионного напряжения молекулы.
Если представить шестичленный цикл плоским, то его внутренние валентные углы должны быть равными 120°, Это обусловило бы значительное угловое напряжение. Следует отметить, что в плоской структуре появляются взаимодействия, связанные с заслонением С–Н-связей, то есть торсионное напряжение.
Однако же циклогексан не является плоской структурой и существует без углового напряжения, так как все валентные углы в нем тет-раэдрические (109*28').
До недавнего времени считали, что наиболее устойчивыми структурами циклогексана являются две изомерные конформации, взаимопревращающиеся друг в друга за счет поворота вокруг σ-связей без их разрыва: «кресла» С (от англ. chair– кресло) и «ванны» В (от англ. bоаt- лодка).

Более устойчивой является конформация «кресла», так как лишена торсионного напряжения (все атомы углерода и водорода находятся в заторможенной конформации). В конформации «ванны» происходит заслонение связей, расположенных вдоль двух параллельных боковых сторон молекулы, что обуславливает торсионное напряжение.
В настоящее время с помощью физико-химических методов исследования установлено, что циклогексан может существовать в различных конформациях: «кресло», твист-форма (искаженная ванна), «полукресло», «ванна». Второй по устойчивости является твист-форма.
Она образуется в результате «скручивания» конформации «ванны» в продольном направлении, что уменьшает напряжение в цикле,
В обычных условиях преобладающая часть молекул циклогексана (99,9 %) существует в конформации «кресла». В результате вращения вокруг углерод-углеродных связей одна конформация «кресла» переходит в другую, энергетически равноценную, форму кресла. Такой процесс называют инверсией цикла.

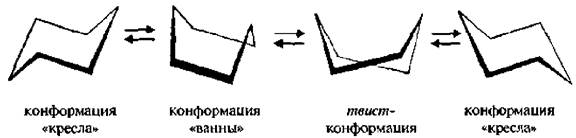
Две конформации «кресла» могут взаимно превращаться как с промежуточным образованием конформации «ванны», твист-конформации, так и без прохождения через конформацию «ванны».
Изучая пространственное строение циклогексана, было установлено, что шесть С–Н связей расположены впольоси симметрии молекулы, а другие шесть – под углом 109°28'. Связи, параллельные оси симметрии, называют аксиальными (обозначают символом «а»), а расположенные радиально – называют экваториальными (обозначают символом «е»). Каждый атом углерода имеет одну (~100 000 раз в секунду при 25° C) все экваториально связанные атомы водорода становятся аксиальными, а все аксиально связанные – экваториальными. Взаимопревращения в циклогексане протекают настолько быстро, что все атомы водорода циклогексана становятся эквивалентными.
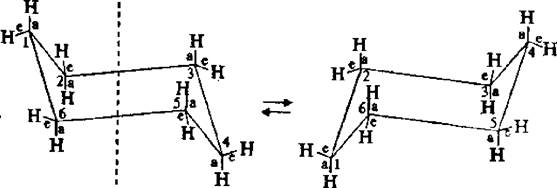
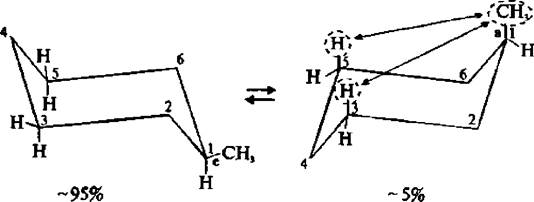
Две конформации «кресла» монозамещенного циклогексана энергетически неравноценны. Более стабильной является конформация с экваториальным положением заместителя. Аксиальное положение заместителя для циклогексана менее выгодно, так как возникает стерическое отталкивание, обусловленное взаимодействием заместителя с аксиально расположенными атомами водорода в положении 3 и 5.
Химические свойства циклоалканов
Для циклоалканов характерны реакции свободно радикального замещения (SR).
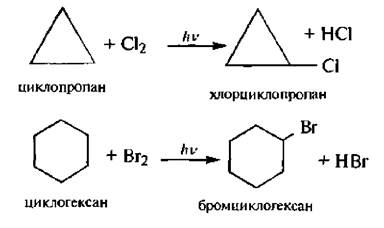
Циклоалканы с малыми циклами проявляют своеобразные химические свойства, связанные с особенностями их строения. Из-за значительного углового и торсионного напряжения трехчленный и, в меньшей степени, четырехчленный циклы являются неустойчивыми. Именно поэтому для циклопропана и циклобутана наряду с реакциями замещения характерны реакции присоединения, сопровождающиеся раскрытием цикла.
1. Гидрировиние
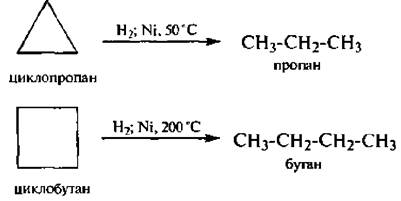
2. Галогенирование
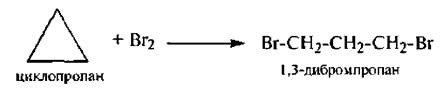
Следует отметить, что с бромом циклобутан вступает в реакцию замещения SR.
3. Гидрогалогеицрование

Представляет интерес реакция присоединения галогеноводородов к алкилзамешенным циклопропана, протекающая в соответствии с правилом Марковникова:
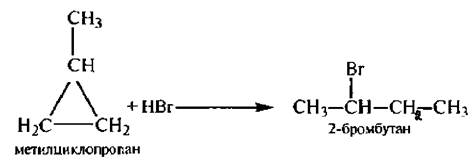
Однако циклобутан не реагирует с галогеноводородами.
Для циклоалканов и их производных характерны реакции сужения и расширения циклов. Данные реакции являются каталитическими и протекают в присутствии кислот Льюиса:

В связи с низкой реакционной способностью и отсутствием функциональных групп идентификация алканов с помощью каких-либо аналитических реакций невозможна. Прежде всего используют физико-химические константы (температуры кипения, плавления; коэффициент преломления, удельное вращение – для оптически активных жидких циклоалканов и др.); определяют процентное содержание углерода и водорода путем сжигания, молекулярную массу и др.; данные физических (инструментальных) методов исследования (ИК-, ПМР-спектроскопии и масс-спектрометрии).
8. АЛКЕНЫ (ЭТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ, ОЛЕФИНЫ)
Углеводороды алифатического ряда, содержащие одну двойную связь, называют алкенами.
Двойная связь 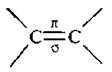 состоит из σ-связи, которая образована sp2-гибридизованными атомными орбиталями (АО) атома углерода и π-связи, образованной негибридизованными р-орбиталями. Строение двойной связи более подробно было рассмотрено ранее. Общая формула алкенов CnH2n.
состоит из σ-связи, которая образована sp2-гибридизованными атомными орбиталями (АО) атома углерода и π-связи, образованной негибридизованными р-орбиталями. Строение двойной связи более подробно было рассмотрено ранее. Общая формула алкенов CnH2n.
Номенклатура
Простейшим представителем углеводородов ряда этилена является сам этилен, или этен: С2Н4, Н2С=СН2. Названия алкенов по заместительной номенклатуре И ЮПАК образуются путем замещения суффикса -ан в названии предельного углеводорода на -ен, положение двойной связи указывается цифрой, при этом нумерация начинается с того конца цепи, к которому ближе расположена двойная связь:
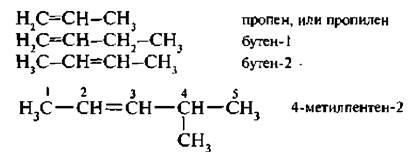
Для низших членов гомологического ряда алкенов более употребимы тривиальные названия – этилен, пропилен, для остальных членов гомологического ряда применяют заместительную номенклатуру.
Иногда используют рациональную номенклатуру. По этой номенклатуре углеводород рассматривают как производное этилена, в котором атомы водорода замещены на радикалы.
Например:
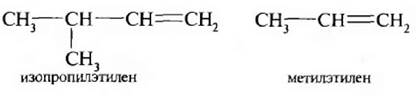
Если в молекуле этилена два атома водорода замещены на радикалы, то алкены рассматривают как симметричные или несимметричные.
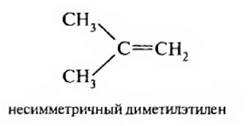
Название одновалентных радикалов этого ряда углеводородов получают добавлением к названию алкена суффикса -ил, атом углерода со свободной валентностью должен иметь наименьший номер, например:
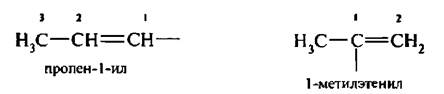
Для некоторых радикалов используются тривиальные названия:

Изомерия
Для алкенов характерна изомерия углеродного скелета, изомерия положения двойной связи и геометрическая (цис-, транс-) изомерия;
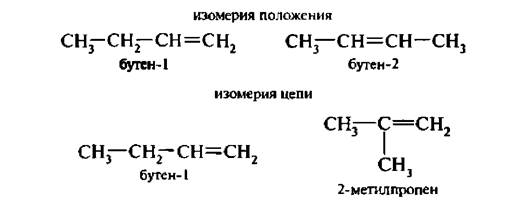
Бутен-2 существует в виде двух пространственных изомеров:

Если у атомов углерода, связанных двойной связью, имеется три или четыре разных заместителя, используют Е, Z-систему обозначении конфигурации геометрических изомеров.
Способы получения
1. Природные источники (нефть, природный газ).
2. Крекинг высших алканов, то есть термическое разложение предельных углеводородов с образованием низкомолекулярных предельных и непредельных соединений.
3. Дегидратация предельных одноатомных спиртое. Алкены легко могут быть получены дегидратацией спиртов. В лабораторных условиях в качестве водоотнимающего средства обычно используют серную или фосфорную кислоту.
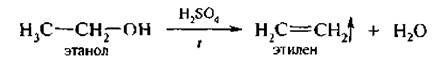
В промышленности применяют оксид алюминия. Пары пропилового спирта пропускают над катализатором при температуре 300–400 *С
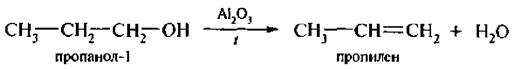
Реакция протекает на границе раздела между твердой фазой и газообразной (гетерогенный катализ).
Отщетение воды от спирта с разветвленной структурой подчиняется правилу А. Зайцева (1875 г.): приобразовании молекулы воды водород отщепляется от наименее гидрогенизированного атома углерода, находящегося в β-положении по отношению кОН-группе.
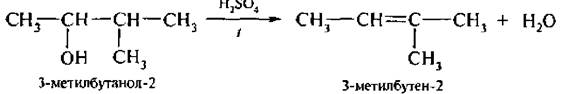
4. Отщепление галогеноводородов от галогеналканов. При действии спиртового раствора щелочи на моногалогенопроизводные отщепляется галогеноводород и образуются алкены.
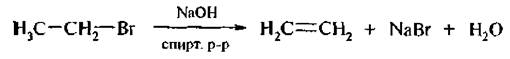
5. Дегалогенирование дигалогеналканов. Вицинальные дигалогеналканы (с атомами галогена у соседних атомов углерода) при нагревании c Zn или Mg в водноспиртовом растворе отщепляют два атома галогена, образуя алкены:

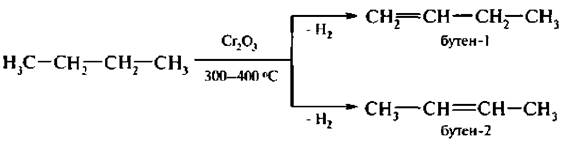
6. Дегидрирование алканов. Это промышленный метод получения алкенов. Реакцию проводят при температуре не выше 600 °С во избежание разрыва С-С связей (крекинг). В качестве катализатора используют мелкораздробленный никель, оксид хрома (III) Сr2O3 и др.
Физические свойства
Первые представители гомологического ряда алкенов (С2–С4) – это газы, дальше – (C5–С17) жидкости и твердые вешества. С увеличением молекулярной массы увеличивается их температура плавления, температура кипения, удельный вес
Алкены с нормальным строением кипят при более высокой температуре, чем их разветвленные изомеры. Температура кипения цис-изомеров выше, чем транс-изомеров, а температура плавления – наоборот.
Алкены практически нерастворимы в воде, сами являются хорошими растворителями. Они горят более коптящим пламенем, чем алканы, что объясняется большим процентом содержания углерода.
Химические свойства
Химические свойства алкенов обусловлены наличием двойной С=С-связи (углерод-углеродной).
Двойная связь 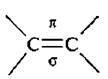 значительно короче (0,134 нм) простой σ-связи и прочнее. Энергия этой связи 611 кДж/моль, на разрыв σ-связи приходится 339,6 кДж/моль. тогда энергия разрыва л-связи будет равна: 611 – 339 = 272 кДж/моль, то есть энергия π-связи невелика. Этим объясняется легкость, с которой непредельные углеводороды вступают в реакции присоединения.
значительно короче (0,134 нм) простой σ-связи и прочнее. Энергия этой связи 611 кДж/моль, на разрыв σ-связи приходится 339,6 кДж/моль. тогда энергия разрыва л-связи будет равна: 611 – 339 = 272 кДж/моль, то есть энергия π-связи невелика. Этим объясняется легкость, с которой непредельные углеводороды вступают в реакции присоединения.
В свою очередь двойная связь влияет на реакционную способность связей С–Н у соседнего с ней sp3-гибридизированного атома углерода (α-атом) (благодаря σ,π-сопряжению). Атомы водорода приобретают подвижность и способность вступать в реакции замещения (SR).
Для алкенов характерны также реакции окисления, восстановления и полимеризации.
1. Гидрогенизация (гидрирование) – присоединение водорода протекает в присутствии катализаторов (тонкоизмельченных Pt, Pd или Ni).
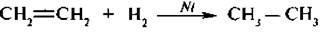
2. Присоединение галогенов (галогенирование). Алкены легко присоединяют хлор и бром, труднее – йод, в результате образуются вицинальные дигалогенопроизводные алканов.
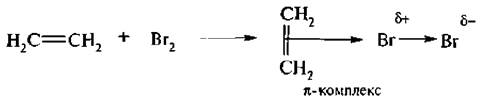
Электронодефицитный атом брома забирает пару электронов π-связи на образование σ-связи с атомом углерода, в результате образуется σ-комплекс:
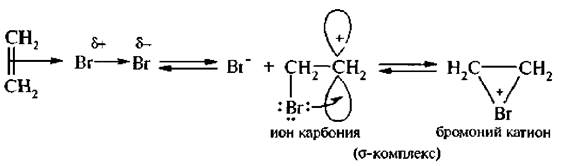
σ-Комплекс представляет собой равновесную систему, состоящую из карбкатиона и бромоний-иона.
Взаимодействие σ-комплекса с бромид-ионом происходит стерео-селективно, то есть бромид-ион атакует σ-комплекс с противоположной стороны от имеющегося галогена. Такое присоединение называется транс-присоединением.
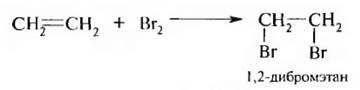
Присоединение происходит по элекгрофильному механизму – АЕ (присоединение электрофильное). Под влиянием π-электронной плотности двойной связи молекула брома поляризуется, при этом образуется π-комплекс:
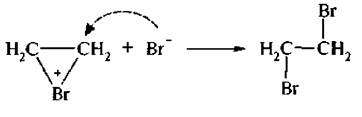
Эта реакция имеет аналитическое значение для качественного и количественного определения соединений, содержащих двойную углерод-углеродную связь.
Направление реакции галогенирования может изменяться в зависимости от условий реакции. Так, алкены с галогенирующими реагентами (хлором, N-бромсукцин имидом) в присутствии инициаторов процесса образования свободных радикалов (пероксиды, температура, УФ-свет) вступают в реакцию свободнорадикального замещения. При этом атом водорода у атома углерода в α-положении к двойной связи замещается на галоген. Такое замещение получило название аллильного.
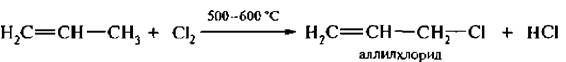
Реакция идет через образование аллильных радикалов

которые являются более устойчивыми по сравнению с обычными алкильными.
3. Присоединение галогеноводородов (гидрогалогенирование). Алкены вступают в реакцию присоединения со всеми галогеноводородами, В случае этилена или симметричных алкенов образуется один продукт реакции независимо оттого, к какому атому углерода присоединяется водород или галоген:
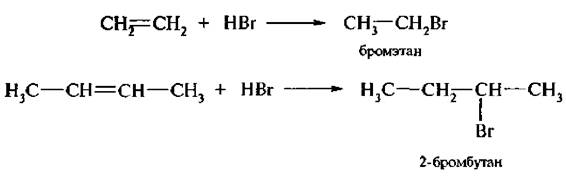
Если галогеноводород присоединяется к несимметричному алкену, то во время реакции могут образоваться два продукта, например:
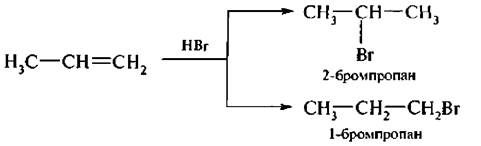
В 1869 г, русский химик В. В. Марковников на основании экспериментальных данных установил закономерность в присоединении галогеноводородов и родственных им соединений к несимметричным алкенам, известную под названием правила Марковникова. Его сущность в следующем:
прн взаимодействии галогеноводоров н родственных им соединений с несимметричными алкенами атом водорода присоединяется к более гидрогенизированному атому углерода, т. е. к атому углерода, содержащему большее число атомов водорода.
Это эмпирическое правило, а теперь, используя электронные представления, дадим пояснения к нему.
Направленность присоединения определяется поляризацией алкена в нереагирующем состоянии. Вследствие +I-эффскта и σ,π-сопряжения со стороны алкильных групп π-электронная плотность двойной связи смещена к более гидрогенизированному атому углерода, что определяет наиболее вероятное место присоединения протона.
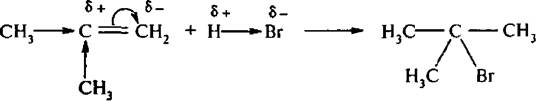
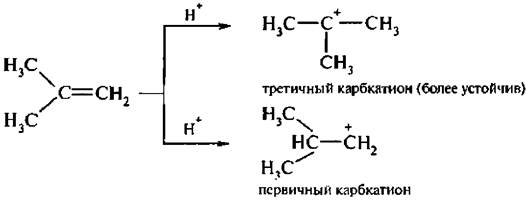
Кроме того, из двух возможных вариантов присоединения протона преимущественно реализуется тот, при котором в качестве промежуточного продукта присоединения образуется более устойчивый карбкатион:
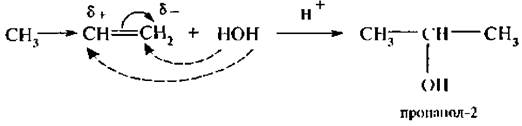
4. Присоединение воды (гидратация). Гидратация алкенов идет в присутствии минеральных кислот, чаше всего серной, и приводит к образованию спиртов:
Механизм реакции следующий:
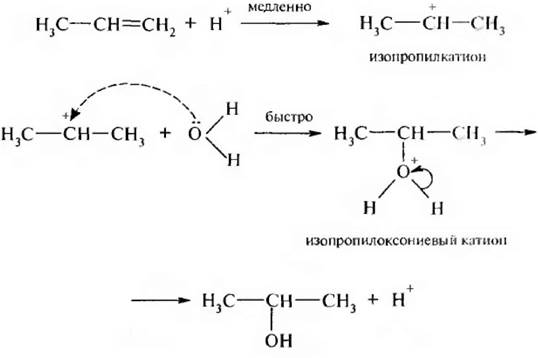
5. Присоединение гипогалогенных кислот (гипогалогенирование). Гипогалогенные кислоты (HOCl, НОВr, HOI) присоединяются к алкенам по двойной связи с образованием галогенгидринов. Механизм реакции электрофильный:
j
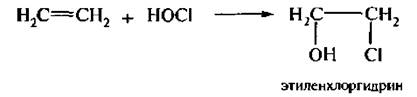
6. Озонирование алкенов. При взаимодействии алкенов с озоном образуются перекисные соединения, которые называются озонидами. При обработке цинком в уксусной кислоте они разрушаются с образованием альдегидов или кетонов в зависимости от строения алкена.
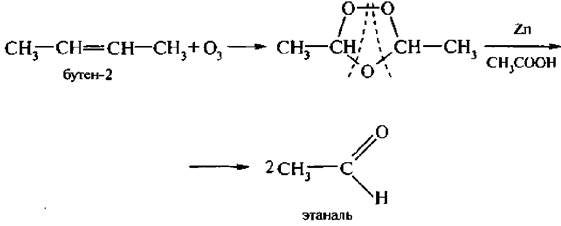
Сопоставляя продукты окисления, можно судить о наличии и положении двойной связи в этиленовом углеводороде.
7. Окисление раствором калия перманганата (реакция Вагнера, 1888г.) – гидроксилирование. Большое значение имеет реакция окисления алкенов КМnO4, которая известна как реакция Е. Вагнера. При взаимодействии алкенов с разбавленным водным раствором КМnO4 в слабощелочной или нейтральной среде образуются двухатомные спирты (гликоли):
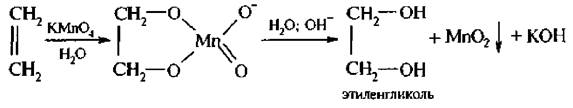
Эта реакция является качественной на кратные связи, по обесцвечиванию раствора перманганата калия можно судить о непредельности соединения.
8. Полимеризация алкенов. Полимеризация является важным свойством этиленовых углеводородов. Полимеризация – это образование высокомолекулярных соединений (полимеров) из низкомолекулярных (мономеров) в результате соединения молекул мономера.
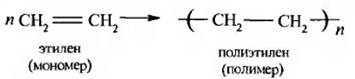
Группа –(–СН2-СН2–)--это элементарное звено полимера, то есть элементарный состав полимера не отличается от состава мономера.
9. АЛКАДИЕНЫ (ДИЕНОВЫЕ УГЛЕВОДОРОДЫ, ДИОЛЕФИНЫ)
Диеновые углеводороды – это углеводороды» содержащие в своей структуре две двойные связи. Общая формула – СnН2n.
Простейшим представителем алкадиенов является аллен, или пропадиен Н2С=С=СН2.
Названия алкадиенов по заместительной номенклатуре ИЮПАК образуют путем прибавления к корню предельного углеводорода суффикса -диен с указанием положения каждой из двойной связи. Например:
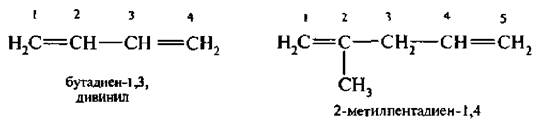
Для некоторых алкадиенов сохранились тривиальные названия.
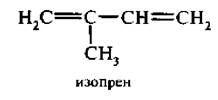
В зависимости от взаимного расположения двойных связей алкадиены делятся на три группы.
1. Алкадиены с кумулированными двойными связями – алленовые углеводороды, В алленовых углеводородах двойные связи находятся в положении 1,2.
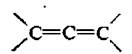
Представителем является аллен.
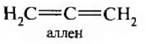
2. Алкаднены с изолированными двойными связями. Двойные связи отделены друг от друга двумя и большим числом простых связей.
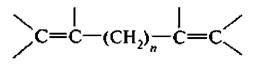
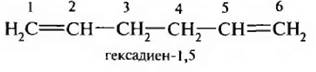
3. Алкалиены с сопряженными, конъюгяроваиными двойными связями. Двойные связи разделяются одной простой связью. Первым представителем этого ряда является дивинил, или бутадиен-1,3.