 |
|
Получения железного порошка восстановлением его оксидов твердым углеродом. Теоретические аспекты.
Т>572°С Fe2O3+СО→ Fe3О4+ СО2+Q
Fe3О4+СО→ FexО+ СО2-Q
FexО + СО → Fe+ СО2+Q
Т<572°С Fe2O3+ СО → Fe3О4+ СО2+Q
Fe3О4+ СО → Fe+ СО2+Q
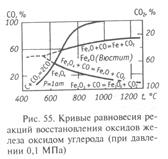 Практически восстановление оксидов железа обеспечивает СО, образующийся при окислении углерода 2С + О2 = 2СО. С увеличением температуры процесса восстановления содержание СО2 в равновесной смеси СО + СО2 снижается и при температурах выше 900 0С становится исчезающе малым.
Практически восстановление оксидов железа обеспечивает СО, образующийся при окислении углерода 2С + О2 = 2СО. С увеличением температуры процесса восстановления содержание СО2 в равновесной смеси СО + СО2 снижается и при температурах выше 900 0С становится исчезающе малым.
Равновесная кривая реакции 2С + О2 = 2СО пересекает равновесную кривую реакции образования Fe при 690 0С, а реакции образования FexО при 650 0С. Эти точки пересечения являются единственными равновесными точками для указанных реакций. Поэтому процесс восстановления Fe3O4 при температуре выше 650 0С и FeXO при температуре выше 690 0С идет до конца, т.е. до исчезновения углерода или соответствующего оксида железа. Практически производство железного порошка возможно только при температуре выше 690 0С и концентрации СО не менее 60%.
Твёрдый углерод в процессе восстановления образует с железом твердые растворы переменной концентрации, а также карбиды, в частности Fe3C по реакции Fe3C + СО2 → 3 Fe + 2СО. Присутствие Fe3C может изменять равновесный состав газовой фазы системы Fe-O-C. Углерод при растворении в железе снижает свою активность, а активность углерода, входящего в состав Fe3C, выше, чем активность графита; поэтому равновесное содержание СО, образующегося по реакции, выше равновесной концентрации СО для реакции Будуара. Образование Fe3C и твердых растворов углерода в железе загрязняет железные порошки углеродом, что осложняет проведение последующих операций прессования и спекания заготовок из них или смесей на их основе.
31. Практика получения железного порошка восстановлением оксидов твердым углеродом (на примере технологии Höganas и СМЗ).
Этот способ был запатентован в 1911 г и применен в промышленной практике шведской фирмой "Хоганес" (Högönas). Сырьём служит гематит, восстановитель – кокс с добавлением известняка для связывания серы из кокса.
Шихта: оксидного сырья 60-69%, кокса 25-33%, известняка 6-7%. Загрузка послойная (кокс + известняк).
Аналогичное производство было налажено в нашей стране в 1951-52 гг. на Сулинском металлургическом заводе (СМЗ). Но в качестве сырья используется прокатная окалина, восстановитель – термоштыб + известняк. Но восстановительную смесь в тигли (капсели) засыпают не послойно, а вертикальными кольцевыми слоями.
После загрузки тигли ставят на вагонетку и направляют в туннельную печь, обдуваемую природным газом (что сказывается на стоимости порошка – дорожает). Расход газа 430-480 м3/т.порошка.
Длина печи 141 м. 50 см. Рабочая зона – 132 м. делится на:
- зона нагрева 30м.
- зона выдержки 66м., из них 55 м. – максимальная Т=1170-1200°С
- зона охлаждения 36м.
Общая продолжительность процесса 88 ч, из них:
- нагрев 20ч.
- Выдержка 40 ч.
- охлаждение 28ч.
Производительность 2т/час.
После процесса в губке:
- захваченный тв. углерод
- углерод и кислород в порошке.
Избавление: вагонетки с капселями без крышек загоняются в туннельную печь с Т=750-800°С для самообезуглероживающего отжига в течение 22 ч. Углерод горит за счёт кислорода в печи и в порошке. Затем железную губку выгружают в виде трубы и разрезают на части размером до 30 мм. дискозубчатой дробилкой, затем направляют на двустадийный размол в стержневых мельницах и разделяют порошок магнитной сепарацией.
В результате получается порошок низкого качества (4 состав). Для улучшения качества используют восстановительный отжиг в конвейерных печах в водороде при 800-900°С с последующим дроблением, измельчением, рассевом и усреднением, но при этом увеличивается стоимость порошка.
Обозначение железного порошка включает указание на способ его получения ("В" – восстановленный), марку по химсоставу (например, 2 или 4), предельную крупность частиц в микрометрах (например, 160) и среднюю насыпную плотность (например, 2,4 г/см3); пример обозначения ПЖВ2.160.24.
Железные порошки могут быть очищены от наиболее нежелательных примесей SiO2 и MnO (ухудшают прессуемость порошков и стойкость прессформ) гидрометаллургической обработкой смесью соляной и плавиковой кислот HCl:HF=10:1.
SiO2 + 4HF = SiF4↑ + H2О
MnO + 2HCl = MnCl2 + H2O
Чтобы смесь не разъела порошок вводят ингибитор коррозии типа "УНИКОЛ" (подавляет коррозию железа и снижает расход кислот).
Затем порошок сушат и снова отжигают в водороде (1000°С)
Длина технологической цепочки очень большая.