 |
|
Часть 1. Простое вещество.
V группа, главная подгруппа.
| Общая электронная формула | ns2np3 |
| Азот, фосфор, мышьяк | неметаллы |
| Сурьма и висмут | металлы |
| Электроотрицательности: | N - 3 P - 2,2 As - 2,1 |
| Наиболее характерные степени окисления: | +5, +3, 0, -3. |
| Оксиды Э2O5 и Э2O3 | Кислотные оксиды. |
| Водородное соединение: | ЭН3 |
Азот
Часть 1. Простое вещество.
:N≡N:
Связь – ковалентная неполярная. В молекуле имеются одна сигма и две пи- связи.
| Степени окисления:
–3, 0, +1, +2, +3, +4, +5.
Электронная формула: 1s22s22p3
 2s 2p
Физические свойства:
Азот – газ без цвета и запаха, плохо растворим в воде.
2s 2p
Физические свойства:
Азот – газ без цвета и запаха, плохо растворим в воде.
|
| Получение азота: 1) разложение нитрита аммония: NH4NO2 -t→ N2 + 2H2O 2) горение аммиака: 4NH3 + 3O2 = 2N2 + 6H2O 3) В промышленности азот получают из воздуха. | Нахождение в природе: Азот является основной частью ВОЗДУХА (78% по объёму). В земной коре встречается в основном в виде нитратов. В живых организмах входит в состав аминокислот, белков и нуклеиновых кислот. |
Химические свойства:
1) из-за тройной связи азот очень малоактивен. При обычных условиях с кислородом не реагирует.
Реагирует с кислородом только при высокой температуре, электрическая дуга, 20000С (в природе – во время грозы):
N20 + O2 ⇄ 2N+2O - Q
2) Реагирует с металлами: литием при комнатной температуре, кальцием, натрием и магнием при нагревании:
N2 + 6Li = 2Li3N – нитрИД лития.
N2 + 3Ca -t→ Ca3N2
3) С водородом – при высоком давлении и в присутствии катализатора:
N2 + ЗН2 ⇄ 2NH3 (t,p,kat)
Часть2. Соединения азота(‑3)
1. Нитриды металлов:
твёрдые, легко гидролизующиеся вещества.
| Получение: N2 + 6Li = 2Li3N | Свойства: гидролизуются водой и кислотой. Ca3N2 + 6H2O =3Са(OH)2 +2NH3 Li3N + 4HCl = 3LiCl + NH4Cl |
2. АммиакNH3
Бесцветный газ с резким запахом, бесцветный, легче воздуха. Ядовит.
Аммиак очень хорошо растворим в воде, что объясняется образованием каждой молекулой аммиака четырех водородных связей с молекулами воды.
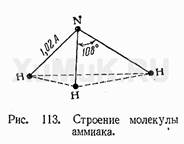
В молекуле аммиака – ковалентные полярные связи, атом азота находится в состоянии sp3-гибридизации.

Способы собирания газов:
А) Вытеснением воздуха для газов легче воздуха;
Б) Вытеснением воды (для газов, малорастворимых в воде).
В) Вытеснением воздуха для газов тяжелее воздуха.

Аммиак можно собирать только по методу (А), т.к. он легче воздуха и хорошо растворим в воде.
Свойства аммиака:
| 1.Молекула аммиака – частица-основание. Принимая протон, она превращается в ион аммония. Реакция может протекать как в водном растворе, так и в газовой фазе: |  :NH3 + H2O ⇄ NH4+ + OH- (в растворе);
:NH3 + H+ = NH4+ (в растворе);
:NH3(г) + HCl(г) = NH4Cl(кр) (в газ. фазе).
:NH3 + H2O ⇄ NH4+ + OH- (в растворе);
:NH3 + H+ = NH4+ (в растворе);
:NH3(г) + HCl(г) = NH4Cl(кр) (в газ. фазе).
|
| 2.Реагирует с кислотами, образуя СОЛИ АММОНИЯ: | NH3 + H2SO4 = NH4HSO4 – гидросульфат аммония 2NH3 + H2SO4 = (NH4)2SO4 – сульфат аммония. |
| 3. Реагирует с солями тяжелых металлов, образуя нерастворимые гидроксиды: | FeSO4 + NH3 + H2O = Fe(OH)2 + (NH4)2SO4 |
| 4. Соли и гидроксиды меди, никеля, серебра растворяются в избытке аммиака, образуя комплексные соединения – амминокомплексы: | 4NH3 + CuSO4 = [Cu(NH3)4]SO4 2NH3 • H2O + AgCl = [Ag(NH3)2]Cl + 2H2O 4NH3•H2O+Ag2O =2[Ag(NH3)2]OH+3H2O |
| 5. Аммиак горит на воздухе, образуя азот и воду. Если реакцию проводить в присутствии катализатора (Pt), то образуется NO: | 4NH3 + 3O2 = 2N2 + 6H2O (горение аммиака), 4NH3 + 5O2 = 4NO + 6H2O (каталитическое окисление). |
| 6. Аммиак способен восстанавливать не очень активные металлы из их оксидов: | 3CuO + 2NH3 = 3Cu + N2 + 3H2O |
| 7. Аммиак в реакциях является восстановителем | 2NH3 + 3Вr2 = N2 + 6HBr 2NH3 + 3H2O2 = N2 + 6H2O |
| 8. Жидкий аммиак способен реагировать с активными металлами. | 2NH3 + 2Na = 2NaNH2 + H2 |
Получение аммиака:
В промышленности:
N2 + 3Н2 (t, p, кат) ⇄ 2NH3
В лаборатории:
а) вытеснение щелочами из солей аммония 2NH4Cl+Са(OH)2 -t→CaCl2+ 2NH3+2Н2O
б) гидролиз нитридов: Ca3N2 + 6H2O = ЗСа(OH)2 + 2NH3