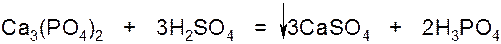|
|
Физические свойства
Фосфор P имеет несколько аллотропных модификаций: белый, красный, чёрный.
Получение фосфора P
Свободный фосфор P получают из природного фосфата кальция, накаливая его с песком (SiO2) и углём в электрической печи при высокой температуре:
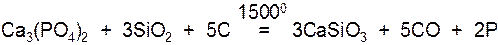
Химические свойства фосфора - P
Белый фосфор более реакционноспособный, чем красный. Он легко окисляется и самовоспламеняется на воздухе.
При окислении белый фосфор светится в темноте – происходит превращение химической энергии в световую.
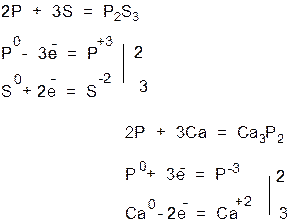
Соединения фосфора P с металлами называются фосфиды. Они легко разлагаются водой с образованием газа фосфина (PH3).
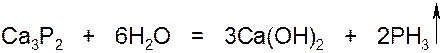
Фосфин - PH3
Может быть получен:
1.Кипячением белого фосфора с концентрированным раствором щёлочи:
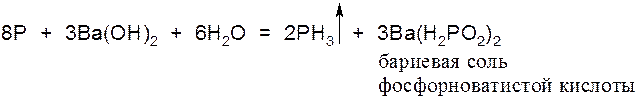
2.Действием соляной кислоты на фосфид кальция:
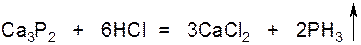
Фосфин PH3 -бесцветный газ с чесночным запахом, очень ядовит!!
Химические свойства фосфина PH3
1.При горении образуется фосфорный ангидрид и вода:
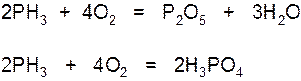
2.Фосфин соединяется с галогеноводородными кислотами, образуя соли фосфония:
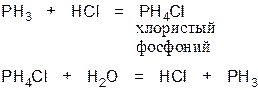
3.При пропускании хлора над расплавленным фосфором получают трёххлористый фосфор:
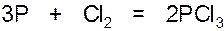
Под действием воды он полностью гидролизуется:
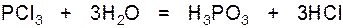
4.При большом избытке хлора образуется пятихлористый фосфор:

Оксиды и кислоты фосфора
Фосфор образует с кислородом три оксида:
P2O3 - фосфористый ангидрид – оксид фосфора (Ш);
P2O5 - фосфорный ангидрид – оксид фосфора (V);
(P2O4 - четырёхокись фосфора).
P2O3получают при медленном окислении фосфора (при недостатке кислорода):
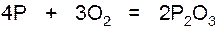
При действии холодной воды образуется фосфористая кислота – H3PO3.
P2O5 образуется при горении фосфора на воздухе (при избытке кислорода):
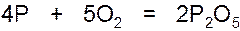
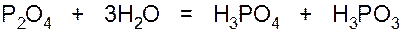
Кислоты
Фосфорный ангидрид P2O5, в зависимости от температуры может присоединить различное количество воды, образуя кислоты различного состава:
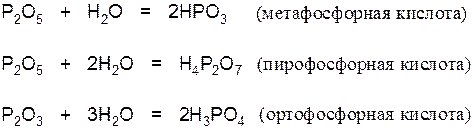
Наибольшее значение имеет ортофосфорная кислота – H3PO4.
Она может быть получена следующим образом:
1.Кипячением метафосфорной кислоты:
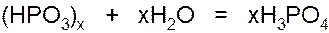
2.Окислением красного фосфора:
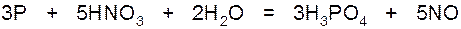
3.Действием серной кислоты на фосфат кальция: