 |
|
Приготування розчинів
МЕТОДИЧНІ ВКАЗІВКИ
ДО розв’язування задач НА ТЕМУ:
“РОЗЧИНИ”
Для студентів усіх спеціальностей
Дніпропетровськ
МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ
Національна гірнича академія України
МЕТОДИЧНІ ВКАЗІВКИ
до розв’язування задач за темою “Розчини”
для студентів усіх спеціальностей
Рекомендована до видання
науково-методичною радою академії
(протокол № 4 від 03.04.2000 р.)
Дніпропетровськ
МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ
Національна гірнича академія України
МЕТОДИЧНІ ВКАЗІВКИ
до самостійної роботи на тему:
“Розчини”
з дисципліни “Хімія”
для студентів напрямків підготовки
0903 “Гірництво”, 0707 “Геологія”, 0925 “Автоматизація та комп’ютерно-інтегровані технології”, 0708 “Екологія”, 0922 “Електромеханіки”, 0906 “Електротехніка”, 0902 “Інженерна механіка”
Рекомендовано до видання науково-методичною радою академії
(протокол № 4 від 03.04.2000 р.)
Дніпропетровськ
Методичні вказівки до розв’язування задач на тему: “Розчини” з дисципліни “Хімія” для студентів усіх спеціальностей / Упорядн.: П.О.Єгоров, О.Б.Нетяга, О.І.Темченко, І.Г.Романова. – Дніпропетровськ: НГА України, 2000. – 17 с.
Упорядники: П.О.Єгоров, проф.
О.Б. Нетяга, ст. викл.
О.І. Темченко, канд. техн. наук, доц.
І.Г. Романова, асист.
Відповідальний за випуск зав. кафедри хімії П.О. Єгоров, канд. хім. наук, проф.
ВСТУП
Розчини мають важливе значення в житті й практичній діяльності людини. Природна вода є складна багатокомпонентна система, в ній розчинені органічні та неорганічні речовини.
Величезна роль води в різноманітних геологічних процесах.
Розчини широко застосовуються при добуванні, збагаченні й переробці корисних копалин.
Студенти повинні знати:
1. Визначення понять: дисперсна фаза; дисперсійне середовище; істинний розчин; процентна, молярна, моляльна, нормальна концентрації та титр розчина.
2. Закони Вант-Гоффа і Рауля.
Необхідно також вміти:
- обчислювати маси та об’єми розчинів і компонентів для приготування потрібної кількості розчину певної концентрації;
- перераховувати одну концентрацію в іншу;
- здійснювати обчислення з використанням законів Вант-Гоффа і Рауля.
Приготування розчинів
Для розв’язування задач даного розділу необхідно знати:
1. Що таке розчин?
2. Що має назву розчинника і розчиненої речовини?
3. Яка величина храктеризує склад розчину?
4. Визначення поняття “процентна” концентрація розчину.
5. Визначення поняття “молярна” концентрація розчину.
6. Чим відрізняється поняття “молярна” і “моляльна” концентрації розчинів?
7. Що таке титр розчину?
Тільки після твердого і ясного засвоєння всіх пойменованих понять можна приступати до розв’язування задач.
Розглянемо відповіді на ці питання.
Систему з двох (або більше) речовин, в якій одна (або декілька) речовин подрібнено і розподілено в іншій, називають дисперсною. Речовини, що утворюють в дисперсній системі суцільну фазу, називаються дисперсійним середовищем, а розподілені в середовищі – дисперсною фазою. Якщо дисперсійне середовище – рідина, то його називають розчинником, а дисперсну фазу – розчиненою речовиною. Наприклад, розчин цукру у воді: розчинник (дисперсійне середовище) – вода, розчинена речовина – цукор. Однорідні гомогенні системи називаються істинними розчинами, а часто просто розчинами. Ступінь подрібнення в справжньому (істинному) розчині молекулярна чи іонна, тобто, лінійні розміри часток не перевищують розмірів окремих молекул або іонів. Склад розчину характеризується його концентрацією. Концентрацією розчину називається вміст розчиненої речовини в певній масовій чи об’ємній кількості розчину. Існують різноманітні способи вираження концентрації розчинів, найважливіші серед яких:
процентна концентрація Ср;
молярна концентрація См;
нормальна концентрація СN;
моляльна концентрація Сg;
титр Т.
Перше ніж розглядати різні способи вираження складу розчинів, введемо ряд загальних позначень:
 р-ну – маса розчину, г;
р-ну – маса розчину, г;
 р-ну – маса одного літра розчину, г;
р-ну – маса одного літра розчину, г;
 р-ка – маса розчинника, г;
р-ка – маса розчинника, г;
 р.р-ни – маса розчиненої речовини, г;
р.р-ни – маса розчиненої речовини, г;
 р.р-ни – маса розчиненої речовини в 1 л розчину, г;
р.р-ни – маса розчиненої речовини в 1 л розчину, г;
 р.р-ни (1 кг) – маса розчиненої речовини, що припадає на 1 кг розчинника;
р.р-ни (1 кг) – маса розчиненої речовини, що припадає на 1 кг розчинника;
 р.р-ни – маса моль розчиненої речовини, г/моль;
р.р-ни – маса моль розчиненої речовини, г/моль;
 – кількість еквівалентів розчиненої речовини;
– кількість еквівалентів розчиненої речовини;
 – кількість еквівалентів розчиненої речовини в 1 л розчину;
– кількість еквівалентів розчиненої речовини в 1 л розчину;
 – кількість моль розчиненої речовини;
– кількість моль розчиненої речовини;
 – кількість моль розчиненої речовини в 1 л розчину;
– кількість моль розчиненої речовини в 1 л розчину;
 – густина розчину, г/мл;
– густина розчину, г/мл;
 – об’єм розчину, мл або л;
– об’єм розчину, мл або л;
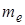 - маса еквівалента, г/моль.
- маса еквівалента, г/моль.
Процентна концентрація показує, скільки грамів розчиненої речовини знаходиться у 100 г розчину або скільки процентів від маси розчину припадає на долю розчиненої речовини.
Молярна концентрація дорівнює кількості моль розчиненої речовини, що міститься в 1 л розчину.








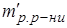

 |  | ||


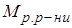







1л 1л




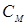 3М Na2SO4
3М Na2SO4
Рис. 1. Визначення молярної концентрації розчину в загальному вигляді
Конкретну молярну концентрацію розчину можна записати двома способами. Наприклад, якщо молярна концентрація розчину  дорівнює 3:
дорівнює 3:
– См  – 3 моль/л;
– 3 моль/л;
– 3М розчин  .
.
Нормальна концентрація розчину дорівнює кількості моль еквівалентів розчиненої речовини, що міститься в 1 л розчину.












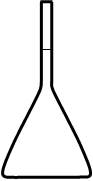
















1 л  1 л
1 л 



Рис. 2. Визначення нормальної концентрації розчину в загальному вигляді
Моляльна концентрація розчину дорівнює кількості моль речовини, розчиненої в 1000 г розчинника. Від молярної концентрації моляльна відрізняється тим, що перша розраховується на об’єм розчину (1 л), а остання – на масу розчинника (1000 г).
Підкреслюємо: моляльна концентрація – єдиний спосіб вираження складу розчину, що відноситься до чистого розчинника
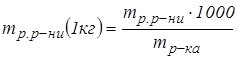 ,
,
 .
.
Приклад. 568 г  розчинено в 2 л води. Обчислити моляльну концентрацію розчину
розчинено в 2 л води. Обчислити моляльну концентрацію розчину
 л
л  г/мл;
г/мл;
 кг;
кг;
 г;
г;
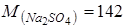 г/моль;
г/моль;
 моль.
моль.
Титр (Т) розчину дорівнює кількості грамів розчиненої речовини в 1 мл розчину.
Наприклад:  г/мл. Це означає, що в 1 мл розчину знаходиться 0,0021 г
г/мл. Це означає, що в 1 мл розчину знаходиться 0,0021 г  .
.