 |
|
Превращение ароматических гидроксисоединений в аминосоединения.
Замещение гидроксигруппы аминогруппой (реакция аминирования, аммонолиз) представляет интерес в том случае, когда амины не могут быть получены из соответствующих нитросоединений или галогензамещенных. Общее уравнение реакции выглядит следующим образом:
ArOH + NH3 ® ArNH2 + H2O
Для проведения этого процесса применяют аммиак в виде водного раствора (²аммиачная вода²) или легко диссоциирующие соли аммония (хлорид, ацетат, гидросульфит, карбонат). Возможно проведение парофазного процесса в условиях гетерогенного катализа (оксид алюминия, алюмосиликаты) при повышенной температуре.
Особенно большое значение замещение гидроксигруппы на аминогруппу имеет в нафталиновом ряду, в частности в случае производных 2-нафтола. Это связано с легкостью получения 2-нафтола, а также с тем, что 2-нафтиламин является очень сильным канцерогеном и работа с ним запрещена. Вместе с тем, ряд нафтиламинсульфокислот с аминогруппой в b-положении представляет значительный интерес в качестве азосоставляющих для получения красителей.
Аминирование нафтолов и гидроксинафталинсульфокислот осуществляют нагреванием их с водными растворами аммиака и сульфита аммония в автоклавах под давлением. Эта реакция носит название реакции Бухерера. Существуют различные точки зрения о возможном механизме этого процесса, однако можно считать четко установленным тот факт, что промежуточно образуются оксо- и иминосоединения. Одна из возможных схем выглядит следующим образом:
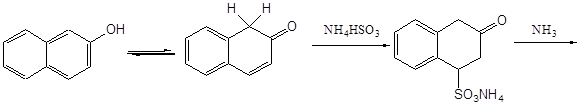

Реакция замещения гидроксигруппы аминогруппой в ряду нафталина имеет те же ограничения, что и процесс замещения аминогруппы гидроксигруппой. Сульфогруппа в мета-положении к гидроксигруппе препятствует замещению последненй на аминогруппу. В то же время сульфогруппа в первом положении нафталинового ядра способствует замещению гидроксигрупп, находящихся в положениях 2 и 4. Таким образом аммонолиз 4,6-дигидроксинафталин-2-сульфокислоты позволяет получить 6-амино-4-гидроксинафталин-2-сульфокислоту (Гамма-кислота).

В промышленности гамма-кислоту получают из Г-соли путем аммонолиза с последующим щелочным плавлением:
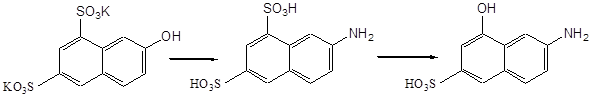
Исходя из 2-нафтола с использованием реакций сульфирования, аммонолиза и щелочного плавления получают изомерную кислоту – 7-амино-4-гидроксинафталин-2-сульфокислоту (И-кислота).
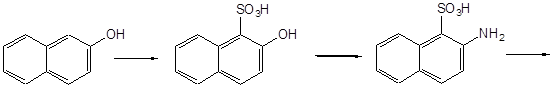

Реакция замещения гидроксигруппы на аминогруппу находит широкое применение в ряду антрахинона, в частности для получения 1,4-диаминоантрахинона из 1,4-дигидроксиантрахинона (хинизарина). Этот процесс протекает легче в присутствии восстановителя, дитионита натрия (Na2S2O4), который восстанавливает 1,4-дигидроксиантрахинон до соответствующего лейкосоединения, которое способно существовать в таутомерной оксо-форме.


Варьируя количество аммиака и хинизарина, можно заместить только одну гидроксигруппу и получить 1-амино-4-гидроксиантрахинон. Указанные выше соединения используются для получения антрахиноновых красителей.
Вместо аммиака в рассмотренных выше процессах возможно применение различных алифатических аминов. В этих случаях образуются соответствующие алкиламинопроизводные.
7.3. Контроль за процессами гидроксилирование и аминирования и методы предосторожности при проведении этих процессов.
Контроль за ходом рассмотренных выше процессов может осуществляться путем определения наличия или отсутствия в реакционной массе ароматического амина. Для этих целей используется реакция диазотирования. Возможно также использование любых приемлемых физико-химических методов контроля (хроматография).
Меры предосторожности при проведении процессов взаимного превращения амино- и гидроксисоединений связаны, в первую очередь, с высокой токсичностью ряда аминопроизводных, в частности производных b-нафтиламина. С точки зрения технологии следует учитывать, что большинство процессов проводится под давлением и при повышенной температуре, и в большинстве случаев возможно выделение аммиака.
Вопросы по теме ²Взаимные превращения амино- и гидроксисоединений²
1. К какому типу реакций относятся взаимные превращения ароматических амино- и гидроксисоединений?
2. Напишите схему таутомерных превращений в случае кетоенольной таутомерии и таутомерии енаминовых соединений.
3. Для каких рядов ароматических соединений наиболее часто используются реакции взаимного превращения амино- и гидроксисоединений.
4. Напишите возможный механизм реакции Бухерера.
5. Какие ограничения для проведения процесса взаимного превращения амино- и окси  соединений накладывает структура исходных субстратов?
соединений накладывает структура исходных субстратов?
6. Напишите схемы реакции и укажите условия проведения реакций, позволяющих получить следующие продукты:
- a-нафтиламин;
- хромотроповую кислоту
- оксикислоту Фрейнда
- кислоту Невиль-Винтера
- гамму-кислоту
- И-кислоту
- 1,4-диаминоантрахинон