 |
|
МКТ. Термодинамика. МФТИ
Сборник задач для абитуриентов. МКТ. Термодинамика. МФТИ
Http://www.fizportal.ru/sbornic-mkt-mfti
 Март 21st, 2010 |
Март 21st, 2010 |  fizportal.ru
fizportal.ru
МКТ. Термодинамика. МФТИ
257. В сосуде объема 1,1 л находятся 100 г адсорбента и водород при температуре t = −193 °С и давлении p = 0,2 amм. Адсорбент при этой температуре поглотил водород в количестве, по весу равном 1/50 веса самого адсорбента. Определить давление в сосуде, если его нагрели до t1 = 31 °С, когда все молекулы водорода покинули адсорбент. Плотность адсорбента 1 г/см3. [p1 = (1/50)maRT1/(M(V − Va)) + pT1/T ≈ 25,35 атм]
258. В сосуде находится смесь азота и водорода. При температуре T, когда азот полностью диссоциирован на атомы, а диссоциацией водорода еще можно пренебречь, давление равно p. При температуре 2T когда оба газа полностью диссоциированы, давление в сосуде 3p. Каково отношение чисел грамм-атомов азота и водорода в смеси? [1/2]
258. В стальном баллоне содержится 0,2 г водорода и 3,2 г кислорода при температуре 27 °С. Водород соединяется с кислородом, и после того, как реакция закончилась, давление внутри баллона увеличилось в три раза. Какова будет при этом температура внутри баллона? [решение]
259. Баллон с гелием при давлении гелия в 65 атм. при температуре −3 °Свесит 21 кг, а при давлении в 20 атм. при той же температуре весит 20 кг. Сколько гелия содержал баллон при начальном давлении 150 атм. и температура 27 °С? [m = ΔmpT1/(T2(p1 − p2)) = 3 кг]
260. На VT-диаграмме изображен замкнутый процесс (цикл), который совершает некоторая масса азота (рис.). Известно, что минимальное давление газа в этом процессе pmin = 3,28 атм. Определить массу газа и 1-го давление p1 точке 1. Величины T1, Т2, V1 и V2 указаны на рисунке. [m = 56 г, p1 = V2T1pmin/(V1T2) ≈ 4,92 атм]

261. Сосуд емкостью V = 10 л откачивается насосом, имеющим производительность α = 100 л/мин. До какого наилучшего вакуума может быть откачан сосуд, если из-за имеющейся в нем течи давление в откаченном сосуде, поднимается на Δp = 1 мм рт. ст. за время t = 1 час 40 мин (при остановленном насосе)? Температуру воздуха в сосуде считать неизменной.
Примечание. Производительность вакуумных насосов принято характеризовать объемом газа, который удаляется из откачиваемого сосуда в 1 c. [p = V•Δp/(αt) = 10−3 мм рт. ст.]
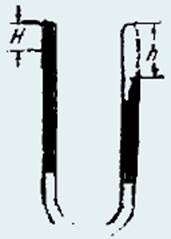
262. На рисунке изображена одна из простейших конструкций термометра, «запоминающего» максимальную температуру, до которой нагревали прибор во время опыта. Длинная U образная трубка, запаянная с одного конца заполнена при температуре Тo = 273 K ртутью, как показано на рисунке. В правом колене над ртутью находится некоторое количество воздуха, высота столбика которого h = 24 см. При нагревании прибора воздух, расширяясь, вытесняет часть ртути. После охлаждения до первоначальной температуры Тo уровень ртути в левом открытом колене понизился на H = 6 см. Определить температуру, до которой нагревался прибор Атмосферное давление pa = 760 мм рт. ст. Давлением паров ртути и ее тепловым расширением пренебречь. [T ≈ 375 К]
263. Водород, содержащийся в баллоне объемом V = 100 л под давлением p = 100 атм., используется для наполнения метеорологических шаров − зондов, имеющих мягкую оболочку. Каждый шар − зонд должен иметь подъемную силу F = 2 кН. Сколько шаров можно наполнить водородом из одного баллона? Температура воздуха В баллоне и шарах равна температуре окружающего воздуха T =300 К. Молекулярный вес воздуха принять равным 29. [n = 5]
264. Когда количество водяных паров в воздухе больше (и во сколько раз) − после месяца затяжных дождей с мокрым снегом в ноябре при 0 °С и относительной влажности 95 % или после месяца сухой жары в июле при 35 °С н влажности 40 %? Давление насыщенного пара при 0 °С − 4,6 мм рт. ст., при 35 °С − 42 мм рт. ст. [mVII/mXI = 3,5]
265. В вертикально расположенном сосуде сечения S. закрытом поршнем массы m, находится воздух. Когда на поршень положили свинцовую болванку массы М, расстояние его от дна цилиндра уменьшилось в n раз. Во сколько раз изменилась температура воздуха в цилиндре? Внешнее давление равно po. [T2/T1 = (1/n)(po + (m + M)g/S)/(po + mg/S)]
266. Электрический утюг с терморегулятором, установленным в положение «шерсть», нагревается до температуры t1 = 140 °С. При этом в установившемся режиме регулятор включает утюг на время τ = 30 с через промежутки времени T1 = 5 мин. В положении «лен» утюг включается на те же 30 с через более короткие промежутки времени T2 = 3 мин. Определите температуру утюга при регуляторе, установленном в положение «лен». Температурной зависимостью сопротивления нагревателя пренебречь Температура в комнате to = 20 °C. [решение]
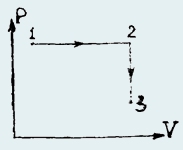
267. Один моль идеального газа переводят из состояния 1 в состояние 3 по изохоре 1 − 2 и, затем по изобаре 2 − 3 (рис.). На изохоре газу сообщается такое же количество тепла Q = 3675 Дж, какое выделяется на изобаре. Найти конечную температуру газа, если его начальная температура to = 27 °С. Теплоемкость газа CV = 21 Дж/(моль•град). [t = to + Δt = to + Q/CV − Q/(CV + R) ≈ 76 °C]

268. В проточном калориметре исследуемый газ пропускают по трубопроводу с нагревателем (см. рис.). Газ поступает в калориметрах при температуре t1 = 20 °С. При мощности нагревателя W1 = 1 кВт и расходе газа M1 = 540 кг/ч температура его t2 за нагревателем оказалась такой же, как и при мощности нагревателя W2 = 2 кВт и расходе газа M2 = 720 кг/ч. Найти температуру газа t2 если его теплоемкость при постоянном объеме 21 Дж/(моль•К), а молекулярная масса равна 29. Давление воздуха в трубопроводе принять неизменным. [t2 = t1 + μ(W2 − W1)/((CV + R)(μ2 − μ1)); t2 ≈ 39,8 °C]

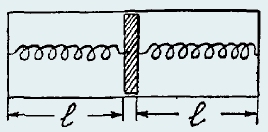
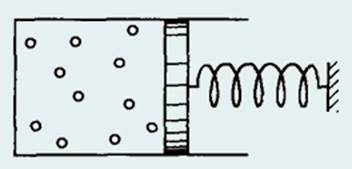
269. В сосуде длиной 2l = 2 м поршень соединен с днищами пружинами жесткостью k = 1493 Н/м каждая (рис.). Вначале в сосуде вакуум, пружины в ненапряженном состоянии. На какое расстояние переместится поршень, если в одну частей сосуда ввести 28 г азота? Температура поддерживаете равной T = 273 К. [x = (l/2)(√{1 + 2RT/(kl2)} − 1) = 0,5 м]
270. Баллончик для приготовления газированной воды имеет объем V = 5 см3 и содержит углекислый газ под давлением p = 15 атм. Можно ли на технических весах с точностью взвешивания 10 мг заметить разницу в весе полного и «пустого» баллончиков? [Δm = moV(p − po)/(poVo) > 0,01 г[ ]решение]
271. Цилиндрический сосуд разделен на две части теплоизолирующим поршнем, связанным с каждым днищем пружиной. Вначале азот, заполняющий левую часть сосуда, и гелий, заполняющий правую часть, находятся при одинаковой температуре To. При этом поршень делит сосуд пополам, а обе пружины находятся в ненапряженном состоянии. Когда азот нагрели до температуры Т1, он занял 3/4 сосуда. При какой температуре Тx, азот займет 7/8 сосуда? Температура гелия поддерживается равной Tо. [Tx = (7/4)(T1 + To)]
272. В расположенном горизонтально теплоизолированном цилиндре может перемещаться поршень, слева от которого находится идеальный газ, а справа − вакуум (рис.). Между поршнем и дном цилиндра расположена пружина. В начальный момент поршень закреплен, а пружина находится в недеформированном состоянии. Затем поршень освобождают. После установления равновесия объем, занимаемый газом, оказался в два раза больше начального, а температура − равной (10/11) от начальной. Определить молярную теплоемкость газа при постоянном объеме. [решение]

273. Одной из причин понижения температуры в атмосфере с высотой является расширение воздуха в восходящих потоках без теплообмена с окружающей средой. Считая воздух идеальным газом, найти понижение температуры на каждые 100 м высоты. При расчете изменением давления в атмосфере на 100 м высоты пренебречь. Молярную теплоемкость воздуха при постоянном объеме принять равной CV = 21 Дж/(моль•К). Молекулярную массу воздуха считать равной 29. [ΔT = −1 °C]
274. Два сосуда заполнены одинаковым газом и сообщаются при помощи узкой трубки. Отношение объемов сосудов n = (V1/V2) = 2. Первоначально газ в большем из сосудов имел температуру T = 300 K. В результате перемешивания происходит выравнивание температур. Найти первоначальную температуру газа во втором сосуде, если конечная температура T = 350 К. Теплообменом со стенками пренебречь. [T2 = 525 К]
275. Воздушный резиновый шарик надувают в комнате ртом при температуре 22 °С. На сколько изменится объем шарика, если вынести его на улицу, где температура 1 °С? Считать, что водяной пар в воздушном шарике находится в насыщенном состоянии. Давление насыщенного пара при температуре 22 °С − 20 мм рт. ст. при температуре 1 °С − 5 мм. рт. ст. Внешнее давление 760 мм рт. ст. Давлением резиновых стенок шарика пренебречь. [V2/V1 = (po − pн1)T2/((po − pн2)T1) = 0,91]
276. В расположенном вертикально эвакуированном теплоизолированном цилиндре может перемещаться массивный поршень. В начальный момент поршень закрепляют и нижнюю часть цилиндра заполняют идеальным газом. Затем поршень освобождается. После установления равновесия объем, занимаемый газом, оказался в 2 раза меньше первоначального. Во сколько раз изменилась температура газа? Молярную теплоемкость газа при постоянном объеме CV принять равной (5/2)R, где R − универсальная газовая постоянная. [T2/T1 = 5/3]
277. Воздух, выдыхаемый человеком, содержит такое количество влаги, что при температуре 22 °С водяной пар в нем становится насыщенным. Воздушный шарик надувают в комнате ртом при температуре 22 °С. Какая доля водяного пара, содержащегося в шарике, сконденсируется, если шарик вынести на улицу, где температура воздуха 1 °С. Внешнее давление 760 мм рт. ст. Давление насыщенных паров воды при температуре 22 °С − 20 мм рт. ст., а при 1 °С − 5 мм рт. ст. Давлением стенок шарика пренебречь. [m2H/m1H = 0,245]
278. Какое количество тепла необходимо подвести молю идеального газа при нагревании его на 1 °С в тепловом процессе, в котором давление р и объем газа V связаны соотношением p = αV, где α − некоторая постоянная. Молярную теплоемкость газа при постоянном объеме принять равной (5/2)R (R − универсальная газовая постоянная). [ΔQ = (CV + R/2)Δt = 25 Дж]
279. В закрытом баке объемом V = 10 л содержится небольшое количество бензина (mo = 0,1 г). Вычислить давление в баке после быстрого сгорания бензина, если первоначальное давление и температура в баке равны соответственно 1 атм и 300 К. Теплоемкость газов в баке после сгорания 5 кал/(моль•K). Теплотворная способность бензина q = 104 кал/г. Универсальная газовая постоянная R = 2 кал/(моль•K). [p = 2,7 атм]
280. Цилиндр, закрытый сверху поршнем, соединен короткой тонкой трубкой с откачанным сосудом (см. рис.). При закрытом кране под поршень вводится некоторое количество газа. Объем, занимаемый этим газом в цилиндре, равен объему нижнего сосуда. Какая часть газа останется в цилиндре после того, как кран открыли? Температура газа в цилиндре поддерживается равной −173 °С, а в сосуде +127 °С. [Mцил/M = 3/4]

281. В цилиндрической трубке заполненной кислородом, содержатся M = 75 мг магния. Одни конец трубки запаян, а другой опущен в сосуд с водой (рис.). На какую высоту поднимется вода в трубке, если весь магний окислится (Mg + O2 → MgO). Объемом магния и его окиси пренебречь. Внешнее давление принять равным po = 105 H/м2, температуру t = 27 °С. Сечение трубки S = 4 см2. Молекулярная масса магния 24.
Указание. При решении задачи давление водяного столба считать пренебрежимо малым по сравнению с атмосферным. Изменением уровня воды в сосуде пренебречь. [h = MRT/(2μpoS) = 9,7 см]

282. В цилиндре под легким поршнем находится 14 г азота при 27 °С Какое количество теплоты необходимо ему сообщить при изотермическом увеличении объема на 4 %? Относительная молекулярная масса азота равна 28. [решение]
Указание. При небольших изменениях объема ΔV/V << 1 воспользоваться приближенной формулой (1 + ΔV/V)−1 ≈ 1 − ΔV/V.
283. В цилиндре под легким поршнем находятся 58 г воздуха при 0 °С. Внешнее давление равно 760 мм рт. ст. Какую работу надо совершить, надавливая на поршень, чтобы изотермически изменить объем воздуха на 1 %. Молекулярную массу воздуха принять равной 29.
Указание. При небольших изменениях объема ΔV/V << 1, воспользоваться приближенной формулой (1 + ΔV/V)−1 = 1 − ΔV/V. [A = (m/(2μ))RT(ΔV/Vo)2 = 0,23 Дж]
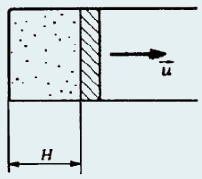
284. В цилиндрическом сосуде, закрытом поршнем, находится разреженный газ, все молекулы которого имеют равные по абсолютной величине скорости v = 200 м/с. Первоначально поршень отстоит от дна сосуда на расстоянии H = 50 см (рис.). Затем его быстро, со скоростью u = 25 м/с, смещают направо на расстояние (3/5)H. Определить, в каком интервале будут находиться скорости молекул газа. Столкновения молекул со стенками и поршнем считать абсолютно упругими. [решение]
285. В герметичном сосуде объемом V = 5,6 л содержится воздух при давлении p = 760 мм рт. ст. Какое давление установится в сосуде, если воздуху сообщить Q = 1430 Дж тепла? Молярную теплоемкость воздуха при постоянном объеме принять равной СV = 21 Дж/(моль•град). [решение]
286. В сосуде объема V = 1 л находится 1 г трития (изотопа водорода с атомным весом A = 3). За 12 лет половина ядер трития превращается в ядра гелия. Найти давление в сосуде в конце этого срока. Температура газа поддерживается равной t = 27 °C. [p = 6,15 атм]
287. В откачанном сосуде емкостью V = 1 л находится 1 г гидрида урана UH3. При нагреве до температуры t = 400 °С гидрид полностью разлагается на уран и водород. Найти давление водорода в сосуда при этой температуре. Атомный вес урана. А = 238. [p = 0,35 атм]
288. Электрический утюг с терморегулятором, установленным в положение «шерсть», нагревается до температуры t1 = 140 °C. При этом в установившемся режиме регулятор включает утюг на время τ = 30 с, через промежутки времени Tx = 5 мин. В положении «лен» утюг включается на те же 30 с, через более короткие промежутки времени T2 = 3 мин. Определить температуру утюга при регуляторе, установленном в положение «лен». Температурной зависимостью сопротивления нагревателя пренебречь. Температура в комнате t = 20 °С. [t2 = 220 °С]
289. В цилиндре объема V под невесомым поршнем находится n молей одноатомного идеального газа. На поршень положили груз массы М, в результате чего поршень переместился на расстояние Н. Определить температуру газа, установившуюся после перемещения поршня. Атмосферное давление равно po, стенки цилиндра и поршень теплонепроницаемы. Сечение цилиндра S. [T = (po + Mg/S)(V − SH)/(nR)]
290. Один моль идеального газа, первоначально находившийся при нормальных условиях, переводят в состояние с вдвое большими объемом и давлением. Процесс перевода слагается из двух участков − изобары и изохоры. Какое количество тепла подведено к газу? Теплоемкость газа СV =21 Дж/(моль•К). [Q = 20 кДж]
291. В интервале температур между 20 и 30° давление насыщенных паров воды меняется на 6 %на каждом градусе. На сколько градусов должна понизиться температура в указанном интервале, чтобы выпала роса, если влажность воздуха составляет 96 %. [Δt = 0,66°]
292. Аквалангист затратил время t = 10 мин на осмотр повреждения подводной части корабля. За это время давление в баллоне акваланга, первоначально равное 150 атм., упало на 20 %. После этого аквалангист приступил к ремонтным работам, и расход воздуха возрос в 1,5 раза. Через какое время после погружения аквалангист должен закончить работы, если давление не должно упасть ниже 30 атм.? [τ = 30 мин]
293. В цилиндрический сосуд с площадью сечения S1 = 200 см2 и высотой h1 = 30 см налит объем V = 4 л воды. В сосуд опускают стержень сечения S2 = 100 см2, высота которого равна высоте сосуда. Какую минимальную массу должен иметь стержень, чтобы он опустился до дна сосуда? [mmin = ρвh1S2 = 3 кг (здесь ρв = 103 кг/м3 − плотность воды]
294. Спутник сечения S = 1 м2 движется с первой космической скоростью v = 7,8 км/с по околоземной орбите. Атмосферное давление на высоте орбиты (200 км) равно p = 1,37•10−4 Н/м2, температура T = 1226 К. Определить число соударений спутника с молекулами воздуха за 1 секунду. [N = NopSv/(RT) ≈ 6•1019 c−1]
Примечание. При решении задачи предполагалось, что молекулы воздуха неподвижны. Это предположение справедливо, так как средняя квадратичная скорость молекул воздуха много меньше скорости спутника.
295. При погружении в тень Земли спутника абсолютная температура внутри его, вначале равная 300 K, упала на 1 %. из-за чего давление понизилось на Δр = 8 мм рт.ст. Определить массу воздуха в спутнике, если его объем V = 10 м3. Молекулярный вес воздуха μ = 29. [m = 11,1 кг]
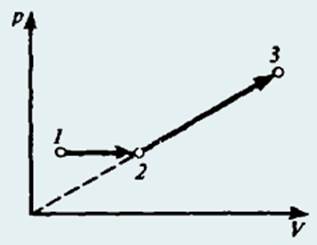
296. Состояние одного моля идеального газа изменялось по изобаре 1 − 2, а затем по изохоре 2 − 3 (рис.). При этом газом совершена работа A. Отношение давлений в состояниях 2 и 3 задано: p2/p3 = k. Известно, что температура в конечном состоянии 3 равна температуре в состоянии 1. Определить эту температуру. [T1 = A/(R(k − 1))]
297. В одном из современных проектов управляемого дирижабля предлагается тепло, выделяющееся при работе двигателя, использовать для нагрева газа, наполняющего баллон дирижабля. Определить величину дополнительного груза, который может поднять дирижабль с баллоном объема V = 1,3•106 м3. Баллон наполнен гелием. Температура за счет нагрева повышается от значения T1 = 300 К до T2 = 400 К. Давление газа в обоих случаях равно нормальному p = 105 Н/м2. [Δmg = (μρVg/R)(1/T1 − 1/T2) = 50m]
298. При подводных работах раньше применялся кессон («подводный колокол») − резервуар, в который по шлангу подавался воздух, вытесняющий воду (рис.). Какое время понадобится для вытеснения воды из насоса, опущенного на глубину H = 20 см? Кессон представляет собой куб с ребром l = 2 м. Компрессор забирает в минуту объем V = 1000 л атмосферного воздуха p = 105 H/м2. [t = 24 мин]

299. Состояние одного моля идеального газа изменялось вначале по изохоре 1 − 2, а затем по изобаре 2 − 3 (рис.). При этом газом совершена работа A. Известно, что температура в конечном состоянии 3 равна начальной температуре Т. Определить отношение давлений в состояниях 1 и 2 − p1/p2. [p1/p2 = RT/(RT − A)]

300. В запаянной с одного конца горизонтально лежащей трубке находится воздух с относительной влажностью ro = 0,8, отделенный от атмосферы каплей ртути длиной l = 7,6 см. Какой станет относительная влажность воздуха r, если трубку поставить вертикально открытым концом вниз? Температура поддерживается постоянной внешнее атмосферное давление p = 760 мм рт. ст. ртуть, из трубки при ее переворачивании не выливается. [r = ro(1 − l/p) = 0,72] [решение]
301. Приготовление пищи в кастрюле-скороварке ведется при температуре 08 °С и повышенном давлении. Какая часть воды испарится после разгерметизации скороварки? Удельная теплоемкость воды c = 1 кал/(г•град), удельная теплота парообразования L = 539 кал/г. Теплообменом за время установления равновесия пренебречь. [mn/mв = cΔ/L = 8/539 ≈ 0,015 = 1,5 %]
302. Приготовление пищи в кастрюле-скороварке идет при температуре t = 120 °С. При такой температуре давление насыщенных водяных паров равно p1 = 2 атм. Во сколько раз плотность пара в таких условиях больше, чем над поверхностью кипящей воды в открытой кастрюле? [ρ1/ρo = p1To/(poT1) ≈ 1,9]
303. В камере сгорания реактивного двигателя объема V = 0,1 м3 при температуре T = 2000 К давление равно p = 2•106 Н/м2. Расход топлива M = 30 кг/с, средняя молярная масса продуктов сгорания μ = 21 кг/кмоль. Определить время пребывания порции топлива в камере сгорания. [t = μpV/(RTM) = 8,35•10−3 c]
304. В цилиндре под поршнем содержится n = 0,5 моля воздуха при температуре To = 300 K. Во сколько раз увеличится объем газа при сообщении ему количества теплоты Q = 13,2 кДж? Молярная теплоемкость воздуха при постоянном давлении Сp = 29,1 Дж/(моль•К). [V/Vo = Q/(nCpTo) + 1 ≈ 4]
305. Лазерные трубки объемом Vo = 60 см3 должны заполняться смесью гелия и неона в молярном отношении 5:1 при общем давлении po = 6 мм рт. ст. Имеются баллоны этик газов, каждый объемом VC = 2 л. Давление в баллоне гелия p1 = 50 мм рт. ст, неона − p2 = 200 мм рт. ст. Какое число трубок можно заполнить? [n = 6p1V/(5poVo) = 333. Указание. Количество заполненных трубок лимитируется гелием]
306. В горизонтально расположенном цилиндре сечением S находится массивный поршень (рис.). В начальный момент поршень удерживается на расстоянии lo от дна сосуда, для чего к нему пришлось приложить силу F. После прекращения действия силы F поршень начинает двигаться без трения. На каком расстоянии от дна поршень будет иметь наибольшую скорость? Процесс считать изотермическим. Внешнее давление равно po. [l = lo(po + F/S)/po. Указание. Скорость поршня будет максимальной в тот момент, когда давление воздуха в цилиндре станет равным атмосферному давлению]

307. Из баллона объемом V1 = 200 л, содержащего гелий при температуре T1 =273 К под давлением p1 =2•106 Н/м2, израсходовали часть газа, занявшего при нормальных условиях объем V2 = 1000 л. При повторном измерении давления в баллоне получено значение p2 = 1,4•106 Н/м2. При какой температуре проведено это намерение? [T2 = p2V1/(p1V1/(RT1) − V2/Vo)R ≈ 254,8 K (здесь Vo = 22,4 л − объем занимаемый одним молем газа при нормальных условиях)]
308. Одинаковые по массе количества водорода (μ(H2) = 2 г/моль) и гелия (μ(He) = 4 г/моль) поместили в сосуд объемом V1, который отделен от пустого сосуда объемом V2 полупроницаемой перегородкой, свободно пропускающей молекулы водорода и не пропускающей гелий. После установления равновесия давление в первом сосуде упало в 2 раза.
Определите V3/V1. Температура постоянна. [решение]
309. Герметичный шар-зонд, изготовленный из нерастягивающегося материала, должен поднять аппаратуру массой M = 10 кг на высоту около 5,5 км, где плотность воздуха (μв = 29 г/моль) вдвое меньше, чем у поверхности Земли. Шар наполняют гелием (μHe = 4 г/моль) при внешних условиях (температура T = 300 К, давление p = 1 атм.). Объем шара V = 100 м3. Определите массу квадратного метра материала оболочки шара. Универсальная газовая постоянная R = 8,3 Дж/(моль•К). [m = ((1/(2μ) − μHe)pV/(RT) − M)/(4π(3V/(4π)2/3)) ≈ 0,3 кг/м2]
310. С какой максимальной силой прижимается к телу человека банка (применяемая в медицинской практике для лечения), если диаметр ее отверстия D = 4 см? В момент прикладывания банки к телу воздух в ней прогрет до температуры t = 80 °С, а температура окружающего воздуха to = 20 °С. Атмосферное давление po = 105 Па. Изменением объема воздуха в банке (из-за втягивания кожи) пренебречь. [Fmax = πD2ΔTpo/(4To) ≈ 26 H]
311. Моль идеального газа нагревается при постоянном давлении, а затем при постоянном объеме переводится в состояние с температурой, равной начальной температуре To = 300 К. Оказалось, что в итоге газу передано количество теплоты Q = 5000 Дж. Во сколько раз изменился объем, занимаемый газом? Универсальная газовая постоянная R = 8,31 Дж/(моль•К). [решение]
312. Кристаллическая решетка железа при комнатной температуре − кубическая объемно центрированная. Это означает, что элементарной ячейкой является куб, во всех вершинах которого, а также в центре − на пересечении пространственных диагоналей − находятся атомы железа. Сколько атомов приходится на объем, равным объему одной элементарной ячейки в кристалле железа? Определите минимальное расстояние между атомами железа в кристалле, зная его молярную массу M = 56 кг/кмоль и плотность ρ = 7870 кг/м3. Постоянная Авогадро NA = 6•1023 кмоль−1. [решение]
313. В теплоизолированный сосуд объемом V = 22,4 дм3, содержащий n1 = 1 моль водород при температуре T1 = 200 К, добавляют m2 = 4 г водорода. После установлении равновесия давление в сосуде оказалось равным p = 3 × 105 Па. Определите первоначальную температуру добавленного водорода. [T2 = (pV/R − n1T1)/(m2/μ) ≈ 310 K, M = 2 г/моль − молярная масса водорода]
314. На рисунке изображена изотерма влажного воздуха. Давление воздуха в точках 1, 2 и 3 равно ρ1, ρ2 и ρ3 соответственно. Определите относительную влажность воздуха в этих точках. [решение]

315. В сосуде длиной L разделенном на три части легкими поршнями, находятся азот, водород и гелий (рис.). Материал, из которого изготовлен правый поршень, оказался проницаемым для водорода и гелия. Левый поршень проницаем только для водорода. Найдите смещения поршней после установления равновесия в системе. Первоначальные давления и температуры газов одинаковы, объем, занимаемый водородом, больше объемов азота и гелия и два раза. [Δl1 = L/4 (левый поршень расположится посередине сосуда). Δl2 = 0 (при достаточно большой скорости диффузии правый поршень практически не сдвинется с места).]

316. При изотермическом сжатии m = 9 г водяного пара при температуре T = 373 K его объем уменьшился в 3 раза, а давление возросло вдвое. Найдите начальный объем пара. [решение]
317. Моль идеального одноатомного газа с начальной температурой T = 600 K адиабатически увеличивает свой объем в 3 раза. Какую работу совершает при этом газ, если в тепловом процессе, при котором давление линейно изменяется с температурой (рис.), газу при расширении из того же начального в то же конечное состояние было подведено количество теплоты Q = l,9 кДж? R = 8,3 Дж/(моль•К). [A = (3/11)(4RT1 − 3Q) ≈ 3,9 кДж]
318. В тепловом процессе объем идеального газа изменяется с давлением по закону V = βp, где β − некоторая постоянная. Во сколько раз изменяется давление газа при уменьшении температуры от T1 = 450 K до T2 = 200 K? [p1/p2 = √{T1/T2} = 1,5]
319. Два теплоизолированных баллона соединены трубкой, перекрытой вентилем. В первом баллоне объемом V1 = 500 л находится m1 = 16,8 кг азота под давлением p1 = 3•105 Па; во втором баллоне объемом V2 = 250 л находится m2 = l,2 кг аргона под давлением p2 = 5•105 Па. Какие давление и температура установятся в баллонах, если открыть вентиль? Теплоемкость моля азота C1 = (5/2)R, его молярная масса М1 = 28 г/моль; теплоемкость моля аргона C2 = (3/2)R, молярная масса M2 = 40 г/моль; газовая постоянная R = 8,31 Дж/(моль•К). [решение]
320. В последние годы популярность приобретает катание на воздушных шарах. Воздух в таком шаре нагревается с помощью газового факела, расположенного у отверстия в нижней части шара. Какую температуру должен иметь воздух в шаре, чтобы поднять двух человек? Масса людей, оболочки шара, корзины и баллона с газом составляет m = 420 кг, диаметр шара D = 20 м, температура окружающего воздуха to = +17 °С, средняя молярная масса воздуха М = 29 г/моль, универсальная газовая постоянная R = 8,31 Дж/(моль•К), атмосферное давление p = 105 Па. [решение]
321. Один моль одноатомного идеального газа совершает замкнутый цикл, состоящий из процесса с линейной зависимостью давления от объема, изохоры и изобары (рис.). Найдите количество теплоты, подведенное к газу на участках цикла, где температура газа растет. Температура газа в состояниях 1 и 2 равна T1 = 300 К, отношение объемов на изобаре V3/V1 = 5/2, направление обхода цикла указано стрелками. Универсальная газовая постоянная R = 8,31 Дж/(моль•К). [решение]

322. В цилиндрическом сосуде, разделенном свободно перемещающимся поршнем на две части, в каждой части находится по одному молю идеального одноатомного газа (рис.). Температура газа в левой части сосуда поддерживается постоянной. Найдите теплоемкость газа в правой части сосуда при таком положении поршня, когда он делит сосуд пополам. Поршень тепла не проводит. [решение]

20(322). В цилиндрическом сосуде, разделенном свободно перемещающимся поршнем на две части, в каждой части находится по одному молю идеального одноатомного газа (рис.). Температура газа в левой части сосуда поддерживается постоянной. Найдите теплоемкость газа в правой части сосуда при таком положении поршня, когда он делит сосуд пополам. Поршень тепла не проводит.

Решение.
Состояние 1 моля идеального газа в правой части сосуда в начальный момент описывается уравнением Менделеева − Клапейрона:
p1V1 = RT1.
Здесь и в дальнейшем индекс «1» будет относиться к параметрам газа в правой части сосуда, а «2» − в левой.
Когда мы подведем к правой части сосуда небольшое количество теплоты ΔQ, параметры газа изменятся, но по-прежнему будут удовлетворять уравнению состояния:
(p1 + Δp1)(V1 + ΔV1) = R(T1 + ΔT1).
Вычитая почленно одно равенство из другого, получим:
p1ΔV1 + V1Δp1 + Δp1ΔV1 = RΔT1.
Как обычно, предполагая, что в проводимом нами процессе все параметры газа изменяются на малую величину
ΔT1 << T1, Δp1 << p1, ΔV1 << V1,
мы можем пренебречь малым членом Δp1ΔV1 по сравнению с другими и записать:
p1ΔV1 + V1Δp1 = RΔT1. (1)
Аналогичное выражение мы можем получить и для 1 моля газа в левой части сосуда:
p2ΔV2 + V2Δp2 = 0. (2)
По определению теплоемкость
C = ΔQ/ΔT.
Используя первое начало термодинамики, для газа в правой части сосуда можно записать:
ΔQ = CΔT1 = ΔU1 + p1ΔV1,
или
CΔT1 = (3/2)RΔT1 + p1ΔV1.
Поскольку давления в обеих частях сосуда все время остаются равными:
p1 = p2 = p и Δp1 = Δp2 = Δp,
а изменения объемов связаны очевидным соотношением
ΔV1 = −ΔV2
из равенств (1) и (2) легко получить, что
p1ΔV1 = RΔT1/(1 + V1/V2),
и, следовательно.
C = (3/2)R + R/(1 + V1/V2).
В момент, когда поршень делит сосуд пополам, V1 = V2, откуда
C = (3/2)R + R/2 = 2R.
323. Идеальный газ расширяется до удвоенного объема в процессе 1 − 2 с линейной зависимостью давления от объема (рис.). Затем его изобарически сжимают в процессе 2 – 3 до первоначального объема. Найдите отношение работ, совершенных газом в процессах расширения и сжатия. Известно, что температуры в состояниях 1 и 2 одинаковы. [решение]

324. КПД тепловой машины, работающей по циклу, состоящему из изотермы 1 − 2, изохоры 2 − 3 и адиабаты 3 − 1 (рис.), равен η, разность максимальной и минимальной температур газа в цикле равна ΔT. Найдите работу, совершенную ? молями одноатомного идеального газа в изотермическом процессе. [A12 = 3νRΔT/(2(1 − η)). Указание. Газ получает тепло только на участке 1 − 2, а совершает работу на участке 1 − 2 и 3 − 1, так, что η = (A12 + A31)/Q12, при этом Q12 = A12, а A31 = −3νRΔT/2.]

325. В калориметр, содержащий m1 = 2 кг льда при температуре t1 = −5 °С добавили m2 = 200 г воды при температуре t2 = +5 °С. Сколько льда будет в калориметре после установления равновесия? Удельная теплоемкость льда с1 = 2,1•103 Дж/(кг•К), воды с2 = 4,2•103 Дж/(кг•К), удельная теплота плавления льда λ = 3,34•105 Дж/кг. [m1/ = m1 + (−c1m1t1 − c2m2t2)/λ = 2,05 кг. Указание. В состоянии равновесия температура смеси равна 0 °С]
326. Трубка длиной l = 1,1 м, герметично закрытая с одного конца, опускается открытым концом в воду и плавает в вертикальном положении, что обеспечивается незначительными внешними боковыми усилиями. Трубку притопили, опустив ее закрытый конец до поверхности воды, и удерживают в новом вертикальном положении. Найдите высоту слоя воды, находящейся в трубке. Атмосферное давление принять равным давлению, создаваемому слоем воды высотой ho = 10 м. Давлением насыщенного пары воды при температуре опыта пренебречь. [x = 0,1 м Указание. Воспользуйтесь законом Бойля − Мариотта, а также тем, что атмосферное давление po = ρgho, ρ − плотность воды]
327. Найдите работу, совершаемую молем идеального газа в цикле, состоящем из двух участков линейной зависимости давления от объема и изохоры (рис.). Точки 1 и 3 лежат на прямой, проходящей через начало координат. Температуры в точках 2 и 3 одинаковы. Считать заданными температуры Т1 и Т2 в точках 1 и 2. [A = A31 + A23 = −R(T2 − T1)/2 + R√{T2/T1}(T2 − T1)/2 = R(T2 − T1)(√{T2/T1} − 1)/2]

328. Резиновый шарик массой m = 2 г задувается гелием при температуре t = 17 °С. При достижении в шарике давленияp = 1,1 атм он лопается. Какая масса гелия была в шарике, если перед тем, как лопнуть, он имел сферическую форму? Известно, что резиновая пленка рвется при толщине δ = 2•10−3 см. Плотность резины ρ = 1,1 г/см3, молярная масса гелия М = 4 г/моль, универсальная газовая постоянная R = 8,31 Дж/(моль•К). [решение]
329. В цилиндре под поршнем находится смесь ν молей жидкости и ν молей ее насыщенного пара при температуре To. При медленном изобарическом нагреве содержимого цилиндра к нему подвели количество теплоты Q, и температура внутри цилиндра увеличилась на ΔT. Найдите изменение внутренней энергии содержимого цилиндра. Объемом жидкости можно пренебречь. [решение]
330. Моль идеального одноатомного газа расширяется сначала в изобарическом процессе, а затем в процессе с линейной зависимостью давления от объема (рис.). Известно, что V2/V3 = V3/V2, а прямая 2 − 3 проходит через начало координат. Найдите отношение объемов V2/V1, если количество теплоты Q12, подведенное к газу на участке 1 − 2, в четыре раза меньше работы A23, совершенной газом на участке 2 − 3. [решение]
331. Цилиндрический колокол для подводных работ высотой h = 2 м опускается вверх дном с борта катера на дно водоема глубиной H = 3 м. Найдите толщину воздушной подушки, образовавшейся у «потолка» колокола к моменту его касания дна водоема. Температуру считайте постоянной. [решение]
332. Гелий (Не) и водород (Н2) находятся в теплоизолированном цилиндре под поршнем. Объем, занимаемый смесью газов, Vo = 1 л, давление po = 37 атм. При адиабатическом расширении смеси относительное уменьшение температуры составило 75 %. Найдите работу, совершенную при этом смесью газов, если масса водорода в 1,5 раза больше массы гелия. Внутренняя энергия моля гелия равна U1 = (3/2)RT, водорода − U2 = (5/2)RT, где T − абсолютная температура. R − газовая постоянная. Молярные массы гелия и водорода равны соответственно M1 = 4 г/моль и M2 = 2 г/моль. [решение]
333. Легкая подвижная перегородка делит герметичный теплопроводящий сосуд на две неравные части, в которых находится воздух при атмосферном давлении и комнатной температуре. В меньшую часть сосуда впрыснули легко испаряющуюся жидкость, давление насыщенного пара которой при комнатной температуре равно pn = 3,5 атм. Спустя некоторое время перегородка перестала двигаться, а жидкость почти вся испарилась. Объем части сосуда, в которой находятся воздух и пары, увеличился при этом вдвое по сравнению с первоначальным. Какую часть объема сосуда составляла вначале его меньшая часть? Объемом, занимаемым жидкостью в начале и в конце опыта, можно пренебречь. [решение]
(333). Легкая подвижная перегородка делит герметичный теплопроводящий сосуд на две неравные части, в которых находится воздух при атмосферном давлении и комнатной температуре. В меньшую часть сосуда впрыснули легко испаряющуюся жидкость, давление насыщенного пара которой при комнатной температуре равно pn = 3,5 атм. Спустя некоторое время перегородка перестала двигаться, а жидкость почти вся испарилась. Объем части сосуда, в которой находятся воздух и пары, увеличился при этом вдвое по сравнению с первоначальным. Какую часть объема сосуда составляла вначале его меньшая часть? Объемом, занимаемым жидкостью в начале и в конце опыта, можно пренебречь.
Решение.
В момент, когда перегородка перестала двигаться, давление паров равно давлению насыщенного пара pн.
Из условия механического равновесия перегородки в этот момент имеем
poV1/V1/ + pн = poV2/V2/,
где po = 1 атм − начальное атмосферное явление, V1 и V1/ − начальный и конечный объемы меньшей части сосуда, a V2 и V2/ − большей его части.
Обозначим
V1/ = α(V1 + V2), V1/ = 2α(V1 + V2).
Окончательно получим α = 3/7.
334. В модели «адиабатической» атмосферы температура воздуха меняется с высотой h по линейному закону T(h) = T(0) − 2Mgh/(7R), где T(0) − температура у поверхности Земли, М = 29 г/моль − средняя молярная масса воздуха, g = 9,8 м/с2 − ускорение свободного падения, R = 8,31 Дж/(моль•К) − газовая постоянная. В той же модели температура T(h) и плотность ρ(h) на высоте h связаны с температурой Т(0) и плотностью ρ(0) у поверхности Земли формулой T5(h)/ρ2(h) = T5(0)/ρ2(0). Найдите массу воздуха, содержащегося в объеме 1 литр на высоте Эльбруса h = 5,5 км. Воздух у поверхности Земли находится при нормальных условиях.
Указание: для x << 1 справедлива формула (1 − x)α = 1 − αx. [решение]
335. Мыльный пузырь надувается воздухом, температура которого выше комнатной. При диаметре пузыря d = 0,3 мм он начинает всплывать (в комнате). На сколько процентов температура воздуха в пузыре выше комнатной? Коэффициент поверхностного натяжения мыльного раствора ? = 0,038 Н/м. Силой тяжести пленки пренебречь. [решение]
336. Внутренняя энергия U неидеального газа зависит от температуры T и объема V по формуле U = cT − a/V, где c и a − заданные константы. Над таким газом из состояния с объемом V1 совершают замкнутый процесс (цикл), состояний из адиабаты 1 − 2, изотермы 2 − 3 и изохоры 3 − 1 (рис.). Найдите разность конечной и начальной температур газа в изохорическом процессе, если работа газа в адиабатическом процессе оказалась в η раз больше работы изотермического сжатия. Известно, что V2 = αV1, а суммарное количество теплоты, подведенное к газу за цикл, равно Q. [решение]
(336). Внутренняя энергия U неидеального газа зависит от температуры T и объема V по формуле U = cT − a/V, где c и a − заданные константы. Над таким газом из состояния с объемом V1 совершают замкнутый процесс (цикл), состояний из адиабаты 1 − 2, изотермы 2 − 3 и изохоры 3 − 1 (рис.). Найдите разность конечной и начальной температур газа в изохорическом процессе, если работа газа в адиабатическом процессе оказалась в η раз больше работы изотермического сжатия. Известно, что V2 = αV1, а суммарное количество теплоты, подведенное к газу за цикл, равно Q.
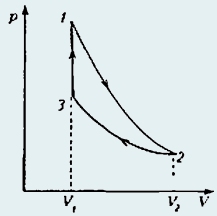
Решение.
Работа на адиабате равна изменению внутренней энергии газа:
A12 = −ΔU12 = −(ΔU13 + ΔU32) = c(T1 − T3) − (α − 1)a/(αV1).
К газу за цикл подводится количество теплоты
Q = A23 + ΔU23 + ΔU31 = −A12/β + A12.
Из этих равенств находим
T1 − T3 = (1/c)(βQ/(β − 1) + (α − 1)a/(αV1)).
337. Моль идеального газа переводится из состояния 1 в состояние 3 путем изобарического нагрева 1 − 2 и изохорического охлаждения 2 − 3 (рис. 1). На участке 1 − 2 газ совершает работу А = 1250 Дж. В процессе всего перехода 1 − 2 − 3 к газу подводится количество теплоты Q = 750 Дж. Найдите разность температур Т2 и T3. [решение]

338. В горизонтально расположенной трубке столбик ртути длиной l = 12 см запирает слой воздуха толщиной L = 35 см (рис.) Если трубку открытым концом повернуть один раз вниз, а другой вверх, то столбик ртути смещается. При этом разность величин этих смещений от начального горизонтального положения равна a = 2 см. Найдите величину наружного давления (в мм ртутного столба). [решение]

339. В переносном газовом баллоне объемом V = 5 л может поместиться не больше m = 2,2 кг жидкого пропана (С3Н8) под давлением p = 10 атм. и при температуре t = 27 oС. Сколько пропана в газообразном состоянии останется в баллоне, если из полного баллона израсходовать 80 % пропана? [решение]
340. В вакуумной теплоизолированный камере находятся два пузыря одинаковых размеров один из которых наполнен гелием, а другой водородом, оба до давления po. Найдите отношение давления, установившегося в камере после того, как пузыри лопнули, к начальному давлению газа в пузырях. Отношение температуры гелия к температуре водорода составляет T1/T2 = 0,6. Молярная теплоемкость гелия при постоянном объеме равна CV1 = (3/2)R, водорода − CV2 = (3/2)R, где R − газовая постоянная. Объем пузыря в 160 раз меньше объема камеры. Изменением поверхностной энергии пленок при разрыве пузырей пренебречь. [решение]
341. На диаграмме зависимости давления p от объема V для некоторой массы идеального газа (рис.) две изотермы пересекаются двумя изобарами в точках 1, 2, 3 и 4. Найдите отношение температур в точках 3 и 1, если отношение объемов в этих точках равно V3/V1 = α. Объемы газа в точках 2 и 4 равны. [T3/T1 = √{ α}]

342. Горизонтально расположенный закрытый цилиндрический сосуд с гладкими стенками разделен подвижным теплонепроницаемым поршнем на две части, в которых находятся различные идеальные газы с одной и той же температурой То = 300 К. Объем, занимаемый одним из газов, в α = 3 раза больше объема, занимаемого другим газом. Газ в большем объеме нагревают, и его объем увеличивается на β = 1/20 объема всего сосуда. На сколько увеличилась температура этого газа, если температура в другой части сосуда поддерживается постоянной и равной To? [ΔT = β(1 + α)2To/(α(1 − β(1 + β))) = 100 K]
343. В сосуде находятся водяной пар и вода при температуре 100 °С. В процессе изотермического расширения вода начинает испаряться. К моменту, когда она вся испарилась, объем пара увеличился в β = 10 раз. Найдите отношение объемов пара и воды в начале опыта. [решение]
344. Цикл для ν молей гелия состоит из двух участков линейной зависимости давления p от объема V и изохоры (рис.). В изохорическом процессе 1 − 2 газу сообщили количество теплоты Q, и его температура увеличилась в 4 раза. Температуры в состояниях 2 и 3 равны. Точки 1 и 3 на диаграмме p − V лежат на прямой, проходящей через начало координат 1) Найдите температуру в точке 1. 2) Найдите работу газа за цикл. [1) T1 = 2Q/(9νR); 2) A = Q/3]

344. Гелий в количестве ν = 2 моля расширяется в процессе с постоянной теплоемкостью C. В результате к газу подвели количество теплоты 3000 Дж и внутренняя энергия газа уменьшилась на 2490 Дж. 1) Чему равна работа, совершенная газом? 2) Определите теплоемкость C. [1) A = 5490 Дж; 2) C = −30 Дж/К]
345. Вода и водяной пар находятся в цилиндре под поршнем при температуре 110 °С. Вода занимает при этом 0,1 % объема цилиндра. При медленном изотермическом увеличении объема вода начинает испаряться. К моменту, когда она вся испарилась, пар совершил работу величиной A = 177 Дж, а объем, который он занимал, увеличился на ΔV = 1,25 л. Найти давление, при котором производился опыт. Сколько воды и пара было в цилиндре в начальном состоянии? [решение]
346. В цилиндре поршнем с пружиной (см. рис.) заперт водяной пар и вода, масса которой M = 1 г. Температура в цилиндре поддерживается постоянной и равной 100 °С. После того, как из цилиндра выпустили часть пара массой m = 7 г, поршень стал двигаться. После установления равновесия объем содержимого в цилиндре под поршнем оказался в 2 раза меньше первоначального. Какая масса пара была в цилиндре и какой объем он занимал в начале опыта? Внешнее давление отсутствует, недеформированная пружина соответствует положению поршня у дна цилиндра, трением между поршнем и стенками цилиндра пренебречь. [1) mп = (4/3)(m − M) = 8 г; 2) V = mпRT/(μpп) = 13,8 л]

347. Насыщенный водяной пар находится в цилиндре под поршнем при температуре 120 °С. При медленном изотермическом уменьшении объема цилиндра пар начинает конденсироваться. К моменту, когда сконденсировалось m = 5 г пара, объем, им занимаемый, уменьшился на ΔV = 4,5 л. Какая по величине работа была совершена внешней силой в этом процессе? Сколько пара было в цилиндре вначале, если в конце опыта вода занимала 0,5 % объема цилиндра? [1) A = (m/μ)RT = 907 Дж; 2) mп = m(1 + V/ΔV) = 6,1 г, где V − объем, занимаемый паром в конце опыта V = 1 л]
348. В цилиндре поршнем с пружиной (см. рис.) заперт водяной пар в объеме V1 = 4 л. Температура в цилиндре поддерживается постоянной и равной 100 °С. В цилиндр вспрыскивается 4 г воды и поршень начинает перемещаться. После установления равновесия часть воды испарилась, а объем цилиндра увеличился в 2 раза.
1) Какая масса пара была в цилиндре вначале?
2) Сколько воды испарилось к концу опыта?
Внешнее давление отсутствует, длина недеформированной пружины соответствует положению поршня у дна цилиндра.
[1) mп = μV1pп/(2RT) = 1,2 г (pn = 105 Па); 2) Испарилось Δm = 2μV1pп/(RT) − mп = 3,6 г] [решение]
349. Атмосфера Венеры состоит в основном из углекислого газа CO2, масса которого по некоторым оценкам составляет M = 6•1016 т. Чему равна плотность углекислого газа вблизи поверхности Венеры, если его температура T = 800 K? Радиус Венеры RЗ = 6300 км, а ускорение свободного падения g = 8,2 м/с2. Толщина атмосферы Венеры много меньше радиуса планеты. [ρ = μMg/(4πRЗ2RT) = 6,6 кг/м3]
350. По некоторым оценкам масса озона (O3) в атмосфере Венеры составляет α = 10−5 % от массы всей атмосферы. Какой толщины слой образовал бы озон, если бы он собрался вблизи поверхности планеты и имел бы при этом температуру и давление, равные температуре и давлению атмосферы у поверхности Венеры? Ускорение свободного падения у поверхности Венеры g = 8,2 м/с2, температура атмосферы T = 800 К. [h = αRT/(μg) << 1,7 мм]
351. Найти массу кислорода, содержащегося в атмосфере Земли. Известно, что температура воздуха вблизи поверхности Земли T = 290 K, радиус Земли R3 = 6370 км, а ускорение свободного падения g = 9,8 м/с2. Масса кислорода, содержащегося в одном литре воздуха, взятого у поверхности Земли, ρ = 0,26 г/л. Процентное содержание кислорода (по массе) в атмосфере Земли считать постоянным. Толщина атмосферы много меньше радиуса планеты. [m = 4πR32ρRT/(μg) ≈ 1018 кг]
352. Если бы озон (O3), содержащийся в атмосфере Земли, собрался бы у ее поверхности тонким слоем и имел бы температуру и давление, равные температуре и давлению атмосферы у поверхности Земли, то толщина этого слоя составила бы h = 3 мм. Найти массу m озона, содержащегося в атмосфере Земли. Радиус Земли R3 = 6370 км, температура атмосферы у поверхности 290 К и давление p = 1 атм. [m = 4πR32μph/(RT) ≈ 2,8•109 т]
353. Два моля гелия при постоянном давлении po = 10 Па охлаждаются на ΔT = 1 К, так что относительное уменьшение объема газа ΔV/Vo составляет η = 0,25 %.
1) На сколько литров уменьшился объем газа?
2) Найти начальную температуру газа. [1) ΔV = 2RΔT/po = 16,6•10−3 л; 2) T = ΔT/α = 400 K]
354. Моль гелия при постоянном объеме Vo = 200 л охладился на ΔT = 1 K так, что относительное уменьшение его давления Δp/po составило α = 0,2 %.
1) На сколько атмосфер уменьшилось давление газа?
2) Какова была начальная температура газа Тo? [1) Δp = RΔT/Vo ≈ 4,15•10−4 атм; 2) To = ΔT/α = 500 K]
355. Моль гелия нагревается при постоянном давлении po = 10 атм, так что относительное увеличение объема ΔV/Vo составил α = 0,5 %. На сколько градусов увеличилась температура газа ΔT, если начальная температура составляла Тo = 400 К? На сколько литров увеличился объем газа? [1) ΔT = Toα ≈ 2 K; 2) ΔV = RΔT/po = 16,6•10−3 л]
356. Моль гелия нагревается при постоянном объеме Vo = 400 л так, что относительное увеличение его давления составило Δp/po = α = 0,4 %.
1) На сколько градусов ΔT увеличилась температура газа, если его начальная температура Тo = 500 К?
2) На сколько атмосфер увеличилось давление газа?
[1) ΔT = Toα = 2 K; 2) Δp = RΔT/Vo = 4•10−4 атм]
357. Найти величину работы A, которую совершает моль гелия в замкнутом цикле, состоящем из адиабатического процесса 1 − 2, изобары 2 − 3 и изохоры 3 − 1. В адиабатическом процессе разность максимальной и минимальной температур газа равна ΔT. В изобарическом процессе от газа отвели количество тепла Q. [A = (3/2)RΔT − (2/5)Q]
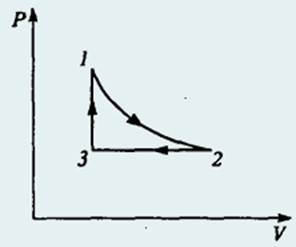
358. Моль гелия совершает работу величиной A в замкнутом цикле (см. рис.), состоящем из адиабаты 1 − 2, изотермы 2 − 3, изобары 3 − 1. Найти величину работы, совершенной в изотермическом процессе, если разность максимальной и мини