 |
|
Определение молярного расхода компонентов газовой смеси
Определение условий равновесия процесса
Определяем равновесные концентрации сероводорода в воде. Если поглощается труднорастворимый газ, то расчет равновесных концентраций ведут по закону Генри:
 , (4.1)
, (4.1)
где Õ – давление в абсорбере, Па;
E – константа растворимости, Па;
x* – равновесная концентрация H2S в воде, 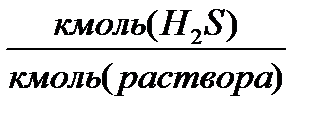 ;
;
у – концентрация H2S в воздухе,  .
.
E = 0,3394×106 мм рт. ст. = 49,108×106 Па при температуре абсорбции 17 °С.
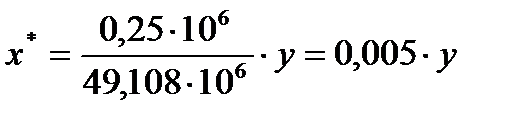 , (4.2)
, (4.2)
Начальная мольная концнтрация H2S рассчитывается по формуле
 , (4.3)
, (4.3)
где ун – содержание H2S в смеси в массовых долях

 .
.
Начальная мольная доля H2S рассчитывается по формуле
 , (4.4)
, (4.4)

Пересчет в массовую концнтрацию производится по формуле
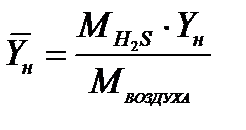 , (4.5)
, (4.5)
где М – молекулярные массы H2S и N2, кг/кмоль
 ,
, 
Величины равновесных концентраций в жидкости достаточно рассчитать для диапазона значений концентраций в газовой фазе от нуля до величины, которая в
1,2-1,5 раз превышает начальную концентрацию абсорбтива.

Для упрощения расчетов материального баланса необходимо сделать пересчет абсолютных концентраций в относительные. Связь между относительной концентрацией и абсолютной выражается следующей формулой :
 , (4.6)
, (4.6)
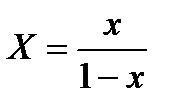 , (4.7)
, (4.7)
где у – абсолютная концентрация H2S в газовой фазе,  ;
;
Y – относительная концентрация H2S в газовой фазе,  ;
;
x – абсолютная концентрация H2S в жидкой фазе,  ;
;
X – относительная концентрация H2S в жидкой фазе,  ;
;
х= 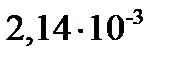



Расчёт материального баланса
Определение молярного расхода компонентов газовой смеси
Пересчитаем объемный расход при нормальных условиях (T0=273K, P0=1,013×105 Па) в объемный расход при условиях абсорбции (Т=290К, Р=0,25×106 Па).
 , (4.8)
, (4.8)
где Vсм0 – расход при нормальных условиях,  .
.
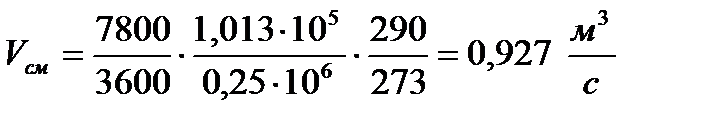 .
.
Для удобства дальнейших расчетов переведем объемный расход газовой смеси в молярный.
 , (4.9)
, (4.9)
где Vсм0 – объемный расход газовой смеси,  ;
;
Gсм – молярный расход газовой смеси,  .
.

Молярный расход инертного газа определяется по уравнению :
 , (4.10)
, (4.10)
где ун – исходная концентрация H2S в газовой смеси,  ;
;
G – молярный расход инертного газа,  .
.
Из условия задания ун=0,428 
 .
.
Концентрацию H2S на выходе из абсорбера yк,  :
:
 , (4.11)
, (4.11)
где j – степень извлечения, j=0,92 (из задания).
 .
. 
Величины yк, yн пересчитаем в относительные по формуле (3.6).
Yк= 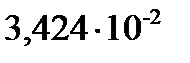
 , Yн=0.428
, Yн=0.428  .
.
Для определения молярного расхода H2S M, который поглощается, служит следующее уравнение:
 . (4.13)
. (4.13)
 .
.
4.2.2 Определение расхода поглотителя H2S из газовой смеси
Для определения минимального молярного расхода чистого поглотителя Lмин служит следующее уравнение:
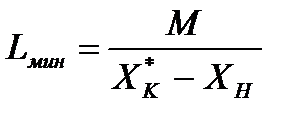 , (4.14)
, (4.14)
где X*к‑ равновесная относительная концентрация H2S в воде на выходе из аппарата,  ; Хн ‑ исходная относительная концентрация H2S в воде,
; Хн ‑ исходная относительная концентрация H2S в воде,  .
.
Равновесную относительную концентрацию H2S в воде на выходе из аппарата определим по линии равновесия, изображенной рисунке 4.1. Для противоточных абсорберов X*к=f(Yн). По графику максимально возможная концентрация H2S в воде при условиях абсорбции составляет X*к=4,4311×10  .
.

Т.к. в реальном процессе абсорбции используется не минимальный расход поглотителя, а несколько больший (для ускорения процесса), то необходимо пересчитать минимальный расход поглотителя на рабочий расход L с учетом коэффициента избытка поглотителя:
 , (4.15)
, (4.15)
где a ‑ коэффициент избытка поглотителя, принимаем равным 1,3. С увеличением расхода поглотителя (т. е. с увеличением коэффициента избытка поглотителя) снижаются допустимые скорости газа в аппарате, по которым находят его диаметр. Поэтому следует выбирать такое соотношение между размерами абсорбционного аппарата и расходом поглотителя, при котором размеры аппарата будут оптимальными.

4.2.3 Определение рабочей концентрации H2S в поглотителе на выходе из абсорбера
Для определения рабочей концентрации служит уравнение:
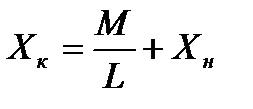 (4.16)
(4.16)


4.2.4 Построение рабочей линии абсорбции H2S и определение средней движущей силы
По полученным значениям концентраций строится график (рисунок 4.1) и определяется средняя движущая сила процесса абсорбции.
Движущая сила массопередачи в соответствии с уравнением массопередачи может быть выражена в единицах концентраций, как жидкой так газовой фаз.
Движущая сила в единицах концентраций газовой фазы определяется по формуле :
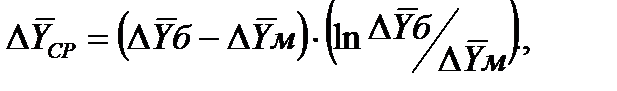 (4.17)
(4.17)
где ΔYб и ΔYм- большая и меньшая движущие силы на входе потоков в абсорбер и на выходе из него, кгH2S/кг смеси (Рисунок 4.1.).

Рисунок 4.1 – Равновесная линия процесса абсорбции
В данном примере
 (4.18)
(4.18)
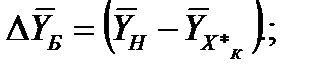 (4.19)
(4.19)
где Y*Xн и Y*Xк – концентрации H2S в исходном газе , равновесные с концентрациями в воде, соответственно на выходе из него (см Рис.3.1.).
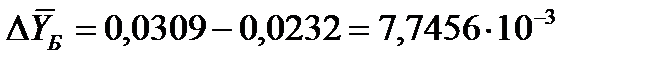 ,
, 
 ,
, 

= 4,5744*10-3,  .
.