 |
|
Рубежный контроль №1
Дисциплина: «Химия»
Специальность: «Общая медицина»
Курс 1
Студент должен владеть навыками:
- приготовления растворов заданной концентрации, определения плотности и рН растворов;
- приготовления буферных растворов с заданным значением рН, определения буферной емкости;
- проведения качественных реакций на катионы и анионы биогенных элементов;
- классификации органических соединений и проведения качественных реакций на функциональные группы.
Рубежный контроль №1
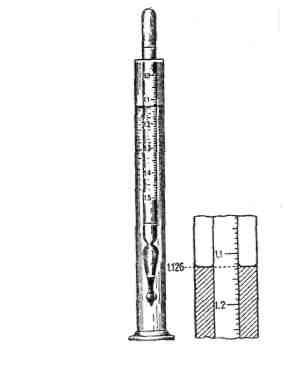
Опыт №1. Определение концентрации раствора по его плотности.
Реактивы и оборудование: исследуемый раствор (жидкость), цилиндры, набор ареометров.
В сухой стеклянный цилиндр налить исследуемый раствор на высоту ареометра (100-200мл) и опустить в него ареометр, шкала которого начинается с 1,00. Если при погружении ареометра шкала окажется полностью над жидкостью, то плотность раствора превышает величину шкалы ареометра. Замените ареометр следующим из набора (с большей плотностью) и так поступайте до тех пор, пока уровень жидкости в цилиндре окажется в пределах шкалы ареометра. Если при погружении ареометра шкала окажется полностью под жидкостью, замените ареометр следующим из набора (с плотностью меньше 1,00) и так поступайте до тех пор, пока уровень жидкости окажется в пределах шкалы ареометра. Плотность меньше 1,00 имеют многие органические жидкости и их растворы. Следите за тем, чтобы при измерении ареометр не касался стенок цилиндра. Отметьте по нижнему мениску деление шкалы ареометра, совпадающее с уровнем жидкости в цилиндре. Это и будет плотность раствора. Определение произведите 3 раза.
Используя таблицы, по плотности определите массовую долю (%) растворенного вещества в растворе. Затем проведите вычисление молярной концентрации и титра раствора. Масса растворенного вещества (mх) в 1 л раствора: mх = 10·w%·d , (г)
Молярная концентрация раствора:

 моль/л
моль/л
В этих формулах:
Мх – молярная масса вещества, г/моль,
w% - массовая доля растворенного вещества, %,
d – плотность исследуемого раствора, г/мл.
Титр раствора:
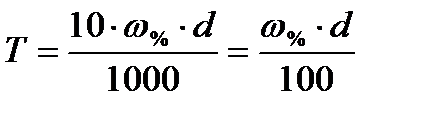 г/мл
г/мл
Опыт № 2.Приготовление раствора по навеске вещества, вычисление его эквивалентной концентрации.
Подготовить к работе мерную колбу и воронку, ополоснув их дистиллированной водой. (Если воронка сухая и чистая, то ополаскивать ее не надо).
Взять навеску вещества и через воронку перенести вещество в колбу. Струей воды из промывалки хорошо смыть вещество из воронки в колбу. Воронку убрать из колбы.
Заполнить колбу дистиллированной водой на 1/3 объема, круговыми движениями поворачивая колбу, повторить перемешивание раствора.
Добавить воды до 2/3 объема колбы, повторить перемешивание раствора
В колбу добавить воды из промывалки на 1-2 см ниже метки. Затем добавлять воду по каплям из пипетки до тех пор, пока нижний край мениска не станет на уровне метки.
Раствор в колбе закрыть пробкой и перемешать, много раз перевертывая колбу.
Вычислить эквивалентную концентрацию вещества по формуле:
 (моль/л); MЭ = f Э·МХ
(моль/л); MЭ = f Э·МХ
где mX – масса растворенного вещества, г
МХ - молярная масса растворенного вещества, г/моль
f Э - эквивалент вещества, моль
MЭ – молярная масса эквивалента вещества, г/ моль
V – объем раствора в литрах, л
Концентрацию раствора вычислить с точностью до 0,0001.