 |
|
Термодинамическая работа
План
1. Количество теплоты
2. Работа.
Количество теплоты
Количество теплоты — энергия, которую получает или теряет тело при теплопередаче. Количество теплоты является одной из основных термодинамических величин.
Количество теплоты является функцией процесса, а не функцией состояния, то есть количество теплоты, полученное системой, зависит от способа, которым она была приведена в текущее состояние.
Единица измерения: Джоуль.
Рассмотрим систему, состоящую из двух тел  и
и  . Предположим, что тело
. Предположим, что тело  заключено почти полностью в жёсткую адиабатическую оболочку, так что оно не способно совершать макроскопическую работу, а обмениваться теплом (то есть энергией) посредством микроскопических процессов может лишь с телом
заключено почти полностью в жёсткую адиабатическую оболочку, так что оно не способно совершать макроскопическую работу, а обмениваться теплом (то есть энергией) посредством микроскопических процессов может лишь с телом  . Предположим, что тело
. Предположим, что тело  также заключено в адиабатическую оболочку почти полностью, так что для него возможен теплообмен лишь с
также заключено в адиабатическую оболочку почти полностью, так что для него возможен теплообмен лишь с  , но не будем предполагать, что оболочка жёсткая. Количеством теплоты, сообщённой телу
, но не будем предполагать, что оболочка жёсткая. Количеством теплоты, сообщённой телу  в некотором процессе, будем называть величину
в некотором процессе, будем называть величину  , где
, где  — изменение внутренней энергии тела
— изменение внутренней энергии тела  . Согласно закону сохранения энергии,
. Согласно закону сохранения энергии,

где  — макроскопическая работа внешних сил над телом
— макроскопическая работа внешних сил над телом  . Если учесть, что
. Если учесть, что

где  — работа, совершённая телом
— работа, совершённая телом  , то по закону сохранения энергии можно придать форму первого начала термодинамики:
, то по закону сохранения энергии можно придать форму первого начала термодинамики:

Из первого начала термодинамики следует корректность введённого определения количества теплоты, то есть независимость соответствующей величины от выбора пробного тела  и способа теплообмена между телами. Заметим, что для определения количества теплоты необходимо пробное тело, в противном случае первое начало теряет смысл содержательного закона и превращается в определение количества теплоты (весьма бесполезное в таком виде). При определении количества теплоты независимо от
и способа теплообмена между телами. Заметим, что для определения количества теплоты необходимо пробное тело, в противном случае первое начало теряет смысл содержательного закона и превращается в определение количества теплоты (весьма бесполезное в таком виде). При определении количества теплоты независимо от  и
и  первое начало становится содержательным законом, допускающим экспериментальную проверку.
первое начало становится содержательным законом, допускающим экспериментальную проверку.
Отметим, что, как и совершённая работа, количество переданной теплоты зависит от конкретного процесса, совершённого над телом.
Неравенство Клаузиуса
Предположим, что рассматриваемое тело может обмениваться теплотой лишь с  бесконечными тепловыми резервуарами, внутренняя энергия которых столь велика, что при рассматриваемом процессе температура каждого остаётся строго постоянной. Предположим, что над телом был совершён произвольный круговойпроцесс, то есть по окончании процесса оно находится абсолютно в том же состоянии, что и в начале. Пусть при этом за весь процесс оно заимствовало из i-го резервуара, находящегося при температуре
бесконечными тепловыми резервуарами, внутренняя энергия которых столь велика, что при рассматриваемом процессе температура каждого остаётся строго постоянной. Предположим, что над телом был совершён произвольный круговойпроцесс, то есть по окончании процесса оно находится абсолютно в том же состоянии, что и в начале. Пусть при этом за весь процесс оно заимствовало из i-го резервуара, находящегося при температуре  , количество теплоты
, количество теплоты 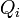 . Тогда верно следующее неравенство Клаузиуса:
. Тогда верно следующее неравенство Клаузиуса:

Здесь  обозначает круговой процесс. В общем случае теплообмена со средой переменной температуры неравенство принимает вид
обозначает круговой процесс. В общем случае теплообмена со средой переменной температуры неравенство принимает вид

Здесь  — количество теплоты, переданное участком среды с (постоянной) температурой
— количество теплоты, переданное участком среды с (постоянной) температурой 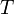 . Это неравенство применимо для любого процесса, совершаемого над телом. В частном случае квазистатического процесса оно переходит в равенство. Математически это означает, что для квазистатических процессов можно ввести функцию состояния, называемую энтропией, для которой
. Это неравенство применимо для любого процесса, совершаемого над телом. В частном случае квазистатического процесса оно переходит в равенство. Математически это означает, что для квазистатических процессов можно ввести функцию состояния, называемую энтропией, для которой


здесь 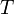 — это абсолютная температура внешнего теплового резервуара. В этом смысле
— это абсолютная температура внешнего теплового резервуара. В этом смысле  является интегрирующим множителем для количества теплоты.
является интегрирующим множителем для количества теплоты.
Для не квазистатических процессов такое определение энтропии не работает. Например, при адиабатическом расширении газа в пустоту

однако энтропия при этом возрастает, в чём легко убедиться, переведя систему в начальное состояние квазистатически и воспользовавшись неравенством Клаузиуса. Кроме того, энтропия (в указанном смысле) не определена для неравновесных состояний системы, хотя во многих случаях систему можно считать локально равновесной и обладающей некоторым распределением энтропии.
Термодинамическая работа
Механическая работа определяется как:
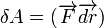 ,
,
где  — сила, а
— сила, а  — элементарное (бесконечно малое) перемещение.
— элементарное (бесконечно малое) перемещение.
Элементарная работа термодинамической системы над внешней средой может быть вычислена так:
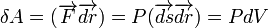 ,
,
где  — нормаль элементарной (бесконечно малой) площадки,
— нормаль элементарной (бесконечно малой) площадки,  — давление и
— давление и  — бесконечно малое приращение объёма.
— бесконечно малое приращение объёма.
Работа в термодинамическом процессе 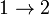 , таким образом, выражается так:
, таким образом, выражается так:
 .
.
Величина работы зависит от пути, по которому термодинамическая система переходит из состояния  в состояние
в состояние 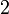 , и не является функцией состояния системы. Такие величины называют функциями процесса.
, и не является функцией состояния системы. Такие величины называют функциями процесса.
Несмотря на то, что до сих пор и в физической химии используется обозначение работы A, в соответствии с рекомендациями ИЮПАК работу в химической термодинамике следует обозначать как W[1]. Впрочем, авторы могут использовать какие угодно обозначения, если только дадут им расшифровку.