 |
|
Свойства твердых тел
Обычно вещество называют твердым, если оно сохраняет свою форму и объем. Твердые тела встречаются в природе двух видов: кристаллические (монокристаллические и поликристаллические) и аморфные. Многие твердые тела в природе имеют гладкие плоские поверхности, расположенные под определенными углами, а иногда и форму правильных многоугольников. Такие твердые тела называют монокристаллами (от греческого “моно” – один). Чаще всего монокристаллы имеют очень маленькие размеры, хотя, например, монокристаллы горного хрусталя иногда бывают величиной с человеческий рост. Изучение внутреннего строения кристаллов с помощью рентгеновских лучей позволило установить, что частицы в кристаллах (молекулы, атомы и ионы) имеют правильное расположение, т.е. образуют кристаллическую (пространственную) решетку.
Рис. 1.

Для размещения частиц в кристаллах характерно наличие симметрии по отношению к определенным плоскостям и направлениям. Число различных возможных элементов и типов симметрии также ограничено. Точки в кристаллической решетке, соответствующие наиболее устойчивому положению равновесия частиц твердого тела, называются узлами решетки. Наиболее простые способы расположения частиц, составляющих кристаллы: кубические и гексагональные пространственные решетки (рис. 1), а также решетки алмаза и графита. Кубические решетки бывают объемно-центрированные (рис. 1.а) где частицы расположены в вершинах и центрах кубов; гранецентрированные (рис. 1.б), где частицы расположены в вершинах и центрах граней кубов.
Одно из свойств твердых тел – межмолекулярное (межатомное) взаимодействие. Сила взаимодействия между двумя молекулами изменяется с расстоянием. Силы притяжения и отталкивания действуют одновременно, но на расстояниях порядка размеров нескольких молекул преобладают силы притяжения, а на очень малых расстояниях, когда начинают перекрываться электронные оболочки, преобладают силы отталкивания. Молекулярные силы взаимодействия между ними имеют электрическое происхождение. Действительно, атомы и молекулы представляют собой сложные системы электрических зарядов, находящихся в движении. Основная масса и весь положительный заряд молекул сосредоточены в атомных ядрах, имеющих линейные размеры порядка 10-14/ 10-15 м. Вокруг ядер вращаются электроны по определенным устойчивым орбитам. Вся совокупность этих электронов рассматривается как электронная оболочка, линейные размеры которой порядка 10-10 м (диаметр электронной оболочки d). Заряд атомных ядер скомпенсирован зарядом электронной оболочки, поэтому молекула (атом) в целом электрически нейтральна и в результате электрическое поле за её пределами отсутствует уже на расстоянии двух-трех диаметров ее электронной оболочки. Поэтому, когда расстояние между центрами молекул велико по сравнению с их диаметрами d, силы взаимодействия пренебрежимо малы. При сближении же молекул на расстояние порядка двух-трех диаметров постепенно начинают проявляться силы взаимодействия электрических ядер и электронных оболочек молекул. Классификация кристаллов возможна как по расположению составляющих их частиц, так и по типу сил взаимодействия между частицами. По типу сил взаимодействия кристаллы разделяют на ионные, атомные, металлические и молекулярные.
Кристалл с металлической связью. В узлах их решетки находятся положительно заряженные ионы металла, а внешние, валентные электроны, слабо связанные с атомами, хаотически движутся по сложным орбитам, охватывающим весь металл. Эти свободные электроны (“электронный газ”) “стягивают” положительные ионы в плотную кристаллическую решетку. Существование электронного газа в металлах объясняются как высокая теплопроводность, так и высокая электропроводимость всех металлов. Электронный газ удерживает положительные ионы в узлах решетки и придает большую прочность металлу (рис.2). Различные типы кристаллов и возможное расположение узлов в пространственной решетке изучает кристаллография. В физике кристаллические структуры рассматривают не с точки зрения их геометрии, а по характеру сил, действующих между частицами кристалла, т.е. по типу связей между частицами.
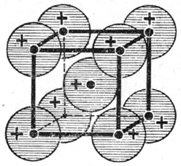
Рис. 2. Плотная упаковка положительно заряженных ионов в кристаллах Na, Cr, Fe.
В молекулярных кристаллах силы взаимодействия между молекулами обусловлены небольшим взаимным смещением электронов в электронных оболочках атомов. Это так называемые поляризационные силы. Кристаллическая структура отличается пространственной решеткой, в узлах которой находятся нейтральные молекулы вещества (рис. 3).

Рис. 3. Модели:
а – пространственной решетки кристалла СО2; б – плотной упаковки кристалла СО2.
Силы, удерживающие молекулы в узлах очень слабые. Энергия связи в таких кристаллах мала, и поэтому молекулярные кристаллы легко деформируются (разрушаются), а также имеют низкую температуру плавления. Примером веществ с молекулярной пространственной решеткой является нафталин, твердый азот, кристалл двуокиси углерода – “сухого льда”. Утверждение “все тела состоят из молекул” справедливо только для молекулярных кристаллов – у ионных, атомных и металлических кристаллов весь образец по существу представляет собой одну гигантскую молекулу.
Ионная кристаллическая структура характеризуется наличием положительных и отрицательных ионов в узлах решетки. Силы, которые удерживают ионы в узлах такой решетки, являются силы электрического притяжения и отталкивания между этими ионами. Разноименно заряженные ионы в ионной решетке расположены ближе друг к другу, чем одноименно заряженные, поэтому силы притяжения между ионами решетки преобладают над силами отталкивания. Этим и объясняется значительная прочность кристаллов с ионной решеткой. При плавлении веществ с ионной кристаллической решеткой в расплав переходят ионы, которые становятся свободными носителями зарядов. Поэтому такие расплавы хорошие проводники электрического тока. Это характерно и для растворов. Раствор поваренной соли (хлористый натрий) в воде является хорошим проводником электрического тока (рис. 4).

Рис. 4. Модель кристаллической решетки и плотной упаковки хлористого натрия.
Атомная кристаллическая структура характеризуется наличием нейтральных атомов в узлах решетки, между которыми ковалентная связь. Ковалентной называется такая связь, при которой каждые два соседних атома удерживаются силами притяжения, возникающими при взаимном обмене валентными электронами между этими атомами. При такой связи электронные облака валентных электронов атомов перекрываются. Эту область можно изобразить в виде электронного облака, которое гуще там, где электрон чаще бывает, т.е. где большая вероятность пребывания электрона. Оба валентных электрона принадлежат обоим атомам одновременно, и большую часть времени проводят между атомами, связывая их в молекулу. Эта связь сильная. Примером являются молекулы азота, водорода и т. д. Твердые вещества – это кремний, германий, алмаз и др. Схематические изображения атомной решетки типа алмаза и упаковки атомов в ней показаны на рис.5.

Рис. 5. Модель кристаллической решетки и плотной упаковки алмаза.
В этой решетке каждый атом образует ковалентные связи с четырьмя соседними атомами. Германий и кремний тоже имеют решетку типа алмаза. Ковалентная связь создает весьма прочные кристаллы. Такие вещества обладают большой механической прочностью и плавятся лишь при высоких температурах.
В физике под твердыми телами подразумевают только такие вещества, у которых имеется кристаллическое строение, т.е. у твердого тела обязательно должен быть дальний порядок в расположении его частей. В кристаллах расстояние между соседними частицами зависит от направления. Этим и объясняется различие физических свойств по разным направлениям, то есть анизотропия кристалла. Анизотропию кристаллических тел можно показать на листочках слюды, графита (рис. 6), которые легко расщепляются в одном направлении и с трудом режутся в перпендикулярном к нему.

Рис. 6. Расположение узлов в кристаллической решетке графита.
Здесь ярко выражена зависимость механической прочности кристалла от направления. В каждом слое кристалла графита атомы углерода расположены в вершинах правильных шестиугольниках, а расстояние между соседними слоями в 2,5 раза больше, чем расстояние между ближайшими атомами углерода в каждом слое. Поэтому слои в кристалле графита легко сдвигаются относительно друг друга. Соскальзыванием слоев мы пользуемся, когда пишем карандашом.
Анизотропией (неодинаковость проведения физических воздействий по разным направлениям) обладают только монокристаллы. В поликристаллических (от греческого “поли” – много) телах анизотропия отсутствует. Это объясняется беспорядочной ориентацией кристаллических зерен. Было установлено, что прочность одного и того же поликристаллического вещества зависит от величины составляющих его мелких кристалликов (зерен): чем мельче размеры кристалликов, тем больше прочность этого вещества. Твердое тело является изотропным, т.е. имеет одинаковые свойства по всем направлениям, хотя отдельный кристаллик обладает анизотропией. Аморфные тела тоже изотропны, т.к. у них нет пространственной решетки.

Рис. 7. Дислокация Рис. 8. Внедрение чужеродных атомов
Дефекты решетки в кристаллах сильно влияют на многие свойства твердых тел, например на прочность, пластичность, электропроводность и т.д.
Виды деформации
При больших деформациях нарушается пропорциональность между силами упругости и деформациями. Кроме того, во многих случаях тело может не восстанавливать свою форму после снятия нагрузки − такие деформации называются пластическими.

Рис.9. Пластическая деформация
При пластической деформации, как показали наблюдения, смещения частиц в кристалле имеют совсем другой характер, чем при упругой. При пластической деформации кристалла происходит соскальзывание слоев кристалла относительно друг друга. Это можно увидеть с помощью микроскопа: гладкая поверхность кристаллического стержня после пластической деформации становится шероховатой. Соскальзывание происходит вдоль слоев, в которых больше всего атомов. При таких смещениях частиц тело оказывается деформированным, но на смещенные частицы при этом не действуют "возвращающие" силы, так как у каждого атома в его новом положении такие же соседи и в таком же числе, как и до смещения. При расчете конструкций, машин, станков, тех или иных сооружений, при обработке различных материалов важно знать, как будет деформироваться та или иная деталь под действием нагрузки, при каких условиях ее деформация не будет влиять на работу машин в целом, при каких нагрузках наступает разрушение деталей и т.д. Деформации могут быть очень сложными. Но их можно свести к двум видам: растяжению (сжатию) и сдвигу.
Деформация растяжения (сжатия). Линейная деформация возникает при приложении силы вдоль оси стержня, закрепленного с одного конца. При линейных деформациях слои тела остаются параллельными друг другу, но изменяются расстояния между ними. Линейную деформацию характеризуют абсолютным и относительным удлинением.

Рис.10.Деформация растяжения (сжатия)
Абсолютное удлинение Δl = l – l0, где l — длина деформированного тела, l0 — длина тела в недеформированном состоянии. Относительное удлинение — отношение абсолютного удлинения к длине недеформированного тела. На практике растяжение испытывают тросы подъемных кранов, канатных дорог, буксирные тросы, струны музыкальных инструментов. Сжатию подвергаются колонны, стены и фундаменты зданий и т.д.
Деформация сдвига возникает под действием сил, приложенных к двум противоположным граням тела. Эти силы вызывают смещение слоев тела, параллельных направлению сил. Расстояние между слоями не изменяется. Любой прямоугольный параллелепипед, мысленно выделенный в теле, превращается в наклонный.


Рис.11.Деформация сдвига Рис.12.Мера деформации сдвига
Мерой деформации сдвига является угол сдвига γ — угол наклона вертикальных граней. Деформацию сдвига испытывают, например, заклепки и болты, соединяющие металлические конструкции. Сдвиг при больших углах приводит к разрушению тела — срезу. Срез происходит при работе ножниц, пилы и др. Деформации изгиба подвергается балка, закрепленная с одного конца или закрепленная с двух концов, к середине которой подвешен груз.

Рис.13. Деформация изгиба
Деформация изгиба характеризуется стрелой прогиба h — смещением середины балки (или его конца). При изгибе выпуклые части тел испытывают растяжение, а вогнутые — сжатие, средние части тела практически не деформируются — нейтральный слой. Наличие среднего слоя практически не влияет на сопротивляемость тела изгибу, поэтому такие детали выгодно делать полыми (экономия материала и значительное снижение их массы). В современной технике широко используются полые балки, трубки. У человека кости тоже трубчатые.
Деформацию кручения можно наблюдать, если на стержень, один конец которого закреплен, действует пара сил, лежащих в плоскости, перпендикулярной оси стержня.

Рис.14.Деформация кручения
При кручении отдельные слои тела остаются параллельными, но поворачиваются друг относительно друга на некоторый угол. Деформация кручения представляет собой неравномерный сдвиг. Деформации кручения возникают при завинчивании гаек, при работе валов машин. [1]