 |
|
Тема: ВОДОПІДГОТОВКА
Мета заняття:Ознайомлення з основними операціями водопідготовки
Після визначення якості води залежно від вимог виробництва проводять водопідготовку. До основних операцій водопідготовки відносять: очистку води від завислих домішок, зм'якшення води, а в окремих випадках нейтралізацію, знесолення, дезаерацію, знезаражування. Деякі операції проводять одночасно. Наприклад, воду очищають від механічних домішок, освітлюють і частково зм'якшують при відстоюванні і фільтруванні її через шар піску і гравію після додавання коагулянтів, вапна і соди.
Теоретичне обгрунтування процесу очистки води від різноманітних домішок вперше дав акад. Л. А. Кульський. Ним встановлено, що головний вплив на процеси очистки води зумовлений фазово-дисперсним станом речовин у водному середовищі. Всі домішки води поділяються на чотири групи, які утворюють з водою гомо- або гетерогенні системи.
Речовини І групи — грубодисперсні домішки, які утворюють з водою суспензії, емульсії, знаходяться в ній у завислому стані і видаляються з води під дією гравітаційних сил, сил прилипання (адгезії, когезії і аутогезії), співосадження.
Речовини II групи — домішки колоїдного ступеня дисперсності(1-100мкм): неорганічні — колоїдні алюмосилікати, колоїдна кремнекислота; органічні — білкові та целюлозні частинки, високомолекулярні речовини, віруси. Ці колоїдні домішки відносяться до електронегативних колоїдів і видаляються головним чином за допомогою коагуляції, адсорбції, окислювальних процесів.
Речовини III групи —молекулярні розчини: розчинні у воді гази і органічні речовини (неелектроліти або слабкі електроліти). Ці домішки здатні взаємодіяти між собою і з водою. Газоподібні речовини, видаляються аерацією, органічні — адсорбцією або екстракцією.
Речовини IV групи — домішки іонного ступеня дисперсності, які утворюються внаслідок дисоціації у воді солей, кислот, лугів. Видаляються перетворенням їх у нерозчинний стан (осад), а також іонообмінною сорбцією, електродіалізом, оберненим осмосом.
Освітлення і знебарвлення води. Освітлення води, або коагуляція колоїдних домішок, відбувається при додаванні таких коагулянтів, як 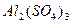 ,
, 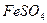 ,
,  , або флокулянтів (прискорювачів утворення великих пластівців). Як флокулянти застосовують колоїдну кремнекислоту, природні (крохмаль) і синтетичні полімери (поліакриламід, полівініловий спирт. та ін.).
, або флокулянтів (прискорювачів утворення великих пластівців). Як флокулянти застосовують колоїдну кремнекислоту, природні (крохмаль) і синтетичні полімери (поліакриламід, полівініловий спирт. та ін.).
Коагулююча дія сульфату алюмінію полягає в тому, що при взаємодії його з розчиненим гідрокарбонатом кальцію або вапном, які спеціально добавляють, утворюється гідрооксид алюмінію:

Пластівці гідроксиду алюмінію мають розвинену активну поверхню і позитивний заряд, який нейтралізує колоїдні частинки домішок. Нейтралізовані частинки домішок укрупнюються і осідають разом з гідроксидом алюмінію. Гідроксид заліза (II), що утворюється при розчиненні сульфату заліза (II), поводиться трохи інакше:
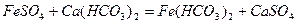
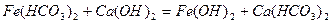
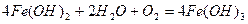
Під дією гідроксиду заліза (III) видаляються колоїдні домішки.
Зм'якшення і знесолення води. Одним з основних факторів у визначенні якості води є твердість, яка зумовлена вмістом розчинених у воді солей кальцію і магнію. Розрізняють твердість тимчасову, постійну і загальну. Тимчасова, або карбонатна, твердість зумовлена наявністю у воді розчинених гідрокарбонатів кальцію і магнію, які при кип'ятінні води розкладаються:

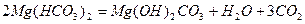
А утворені карбонат кальцію і подвійний основний карбонат магнію випадають в осад.
Постійна твердість води зумовлена всіма іншими розчинними у воді солями кальцію і магнію, які при кип'ятінні в осад не випадають. Сума тимчасової і постійної твердості становить загальну твердість води.
Кількісно твердість води виражають у міліграм-еквівалентах іонів кальцію і магнію в 1 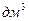 води.
води.
У деяких країнах користуються градусами твердості, які відповідають кількості міліграмів СаО в 100  води.
води.
За величиною твердості вода буває:
Дуже м'яка 0-1,5мг-екв/ 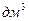
М'яка 1,5—3,0 мг-екв/ 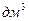
Середньої твердості 3,0—4,5 мг-екв/ 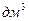
Досить тверда 4,5—6,5 мг-екв/ 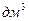
Тверда 6,5—10,0 мг-екв/ 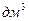
Дуже тверда більше 10,0 мг-екв/дм3
Вапняно-содовий метод зм'якшення води. Для зм'якшення води застосовують вапняно-содовий метод, який полягає в тому, що до води добавляють розраховану кількість вапна, їдкого натру або соди. Наприклад:
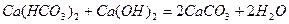
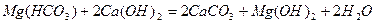
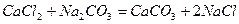
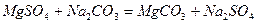
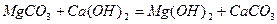
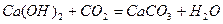
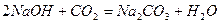
Ще кращих наслідків можна досягти, застосовуючи для зм'якшення води фосфати натрію, але вони дорогі, тому ними користуються після часткового зм'якшення води вапном і содою або у комплексі з ними.