 |
|
Тема 7. Первое начало термодинамики. Работа при изопроцессах
Первый закон (начало) термодинамики: в замкнутой макроскопической системе работа, произведенная над системой и количество теплоты, переданное системе, идут на изменение внутренней энергии системы:
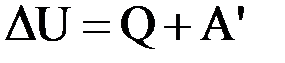 .
.
Применение первого закона термодинамики:
1)изотермический процесс(T=const)– все тепло, поступающее в систему идёт на совершение работы: Q=- A’
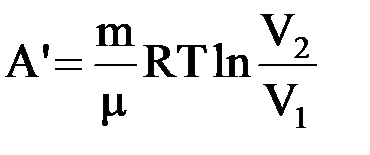 .
.
2)изохорный процесс(V=const)– изменение внутренней энергиисистемы происходит за счет передачи тепла:
 ,
, 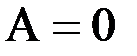 ,
, 
3)изобарный процесс(P=const)–  ,
, 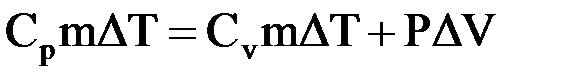 .
.
 При понижении температуры газа степени свободы молекулы «замораживаются» и ее теплоемкость уменьшается (см. рис. для кислорода).
При понижении температуры газа степени свободы молекулы «замораживаются» и ее теплоемкость уменьшается (см. рис. для кислорода).
4) адиабатный процесс – процесс происходит без теплообмена с окружающей средой:
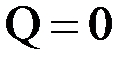 ,
, 
 ,
,
 ,
,  ,
, 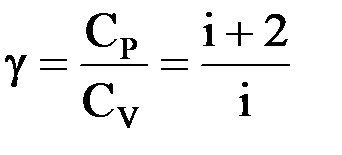
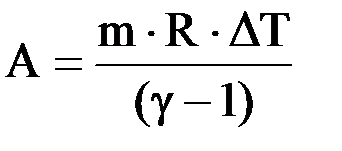 .
.
5) циклические процессы – это круговые процессы: DU = 0, А = Q.
Пример 7.1.Идеальному газу сообщается одинаковое количество теплоты при изохорном (1), изобарном (2) и изотермическом (3) процессах. Для совершаемых газом работ справедливы соотношения:
ð 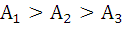 ð
ð  ð
ð 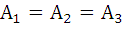 R
R 
Решение: применение первого закона термодинамики дает, что при изохорном процессе работа равна нулю, при изобарном разности полученного тепла и изменения внутренней энергии, а при изотермическом – все тепло пошло на совершение работы, следовательно:  .
.
Пример 7.2. Диаграмма циклического процесса идеального одноатомного газа представлена на рисунке. Чему равно отношение работы при нагревании газа к работе при охлаждении? 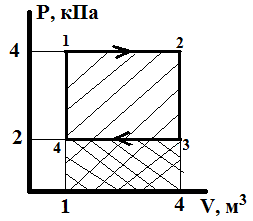
Решение: работа совершается только при изменении объема газа, т.е. на участках (1,2) и (3,4). Это изобарные процессы, при которых объем пропорционален температуре газа (  ), следовательно участок (1,2) – нагревание, а (3,4) – охлаждение.
), следовательно участок (1,2) – нагревание, а (3,4) – охлаждение.
Работа газа равна площади фигуры под графиком зависимости давления от объема. Работа при нагревании – площадь прямоугольника (141234):
Ан = 4(кПа) × 4 (м3) =4000×4=16000 Дж.
Работа при охлаждении – площадь прямоугольника (1434):
Ао= 2(кПа) × 4 (м3) =2000×4=8000 Дж.
Тогда отношение работ равно: Ан/Ао = 16000/8000 = 2. Ответ: 2.
Пример 7.3. Работа, совершаемая идеальным газом при его изобарном расширении, численно равна заштрихованной площади, показанной на рисунке …
 Решение: чтобы дать ответ необходимо определить на каком графике изображен изобарный процесс (при постоянном давлении) – на рисунке 2. (Эти же рис. можно использовать в задании о работе при изотермическом процессе – ответ рис. 5., при круговом процессе – ответ рис. 1.)
Решение: чтобы дать ответ необходимо определить на каком графике изображен изобарный процесс (при постоянном давлении) – на рисунке 2. (Эти же рис. можно использовать в задании о работе при изотермическом процессе – ответ рис. 5., при круговом процессе – ответ рис. 1.)
Пример 7.4. При изотермическом расширении 0,5 моля газа при температуре 200 К объем увеличился в е раз ( е=2,7). Чему равна работа газа (в Дж)?
Решение: работа при изотермическом процессе определяется по формуле: 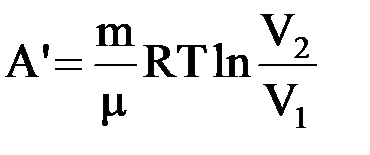
где m/m=0,5 моль; V2/V1=e; ln(е)=1; R=8,31Дж/мольК;T=200К
Ответ: 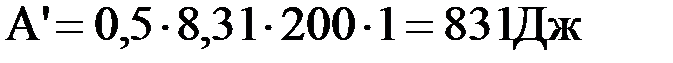
Пример 7.5. Одному молю двухатомного газа было передано 5155 Дж теплоты, при этом газ совершил работу, равную 1000 Дж. Насколько повысилась его температура? Ответ: на200 K.
Решение:по условию задачи дано Q=5155 Дж; A’=1000Дж;
i=5(число степеней свободы двухатомной молекулы); n= 1 моль.
Первое начало термодинамики:
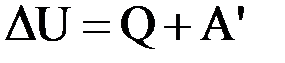 , где
, где  ,
, 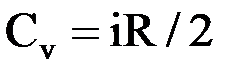
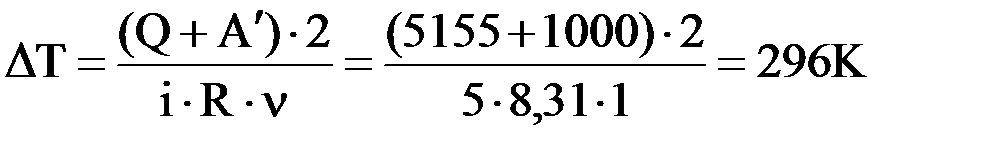
Пример 7.6. Одноатомному идеальному газу в результате изобарического процесса подведено количество теплоты DQ. На увеличение внутренней энергии газа расходуется часть теплоты DU/DQ, равная: ð0,7 R0,6 ð1,7 ð1,4
Решение: число степеней свободы молекул одноатомного газа равно трем (i=3). Запишем формулы для изобарного процесса:

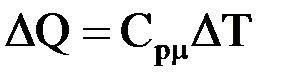
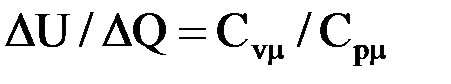



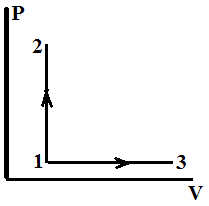 Пример 7.7. Молярные теплоемкости гелия в процессах 1-2 и 1-3 равны С1 и С2 соответственно. Тогда С1 / С2 составляет…
Пример 7.7. Молярные теплоемкости гелия в процессах 1-2 и 1-3 равны С1 и С2 соответственно. Тогда С1 / С2 составляет…
R 3/5 £ 7/5 £ 5/7 £ 5/3
Решение: процесс 1-2 изохорный, а 1-3 изобарный.


Гелий одноатомный газ – число степеней свободы молекулы равно i=3, следовательно,

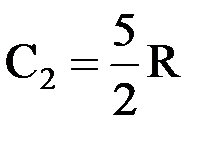
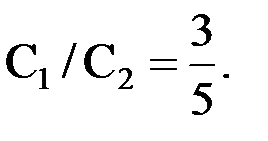
Пример 7.8. Состояние идеального газа определяется значениями параметров:T0, P0, V0, где Т – термодинамическая температура, Р – давление, V – объем газа. Определенное количество газа перевели из состояния (3Р0, V0) в состояние (Р0, 2V0). При этом его внутренняя энергия…£ увеличилась R уменьшилась £ не изменилась
Решение:мерой внутренней энергии газа (и любого вещества) служит его температура. Если температура изменяется – так же изменяется внутренняя энергия, если температура неизменна – значит и внутренняя энергия не меняется. Т.о. чтобы решить это задание нам необходимо определить как меняеися температура газа.
Состояние газа характеризует уравнение Клапейрона-Менделеева:
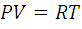 , следовательно, температура пропорциональна произведению давления и объема (
, следовательно, температура пропорциональна произведению давления и объема ( 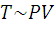 ).
).
По условиям задачи: 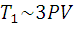 ,
, 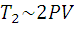 , следовательно
, следовательно 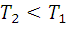 .
.
Пример 7.9. В цилиндре при сжатии постоянной массы воздуха давление возрастает в 3 раза. Если температура газа увеличилась в 2 раза, то отношение объемов до и после сжатия равно…
R 3/2 £ 6 £ 1/6 £ 2/3
Решение: по условию задачи Р2 = 3Р1, Т2 = 2Т1. Определим объемы газа из уравнения Клапейрона-Менделеева:

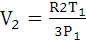
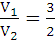 .
.
Пример 7.10. Если DU – изменение внутренней энергии идеального газа, А – работа газа, Q – количество теплоты, сообщаемое газу, то для изохорного охлаждения газа справедливы соотношения…
£ Q < 0; A < 0; DU = 0
£ Q = 0; A < 0; DU > 0
R Q < 0; A = 0; DU < 0
£ Q = 0; A > 0; DU < 0
Решение: изохорный процесс протекает при постоянном объеме, значит, работа равна нулю (А=0). При охлаждении температура и внутренняя энергия уменьшаются (DU< 0). Газ не совершает работу, охлаждается, значит, он отдает тепло (Q< 0).
(если бы происходило адиабатное сжатие газа – тепло не поступает Q = 0; сжатие A< 0; при сжатии газ нагревается DU> 0 – ответ вторая строчка). Самостоятельно рассмотрите адиабатическое расширение, изотермическое сжатие, изобарное охлаждение, изобарное нагревание.