 |
|
Определение теплоты сгорания топлива
Цель работы
Цель работы – изучить устройство и принцип работы калориметрических установок для определения теплоты сгорания твердых, жидких и газообразных топлив; исследовать характеристики топлив, состав, теплотворную способность и количественные отношения между топливом и воздухом.
Определение теплоты сгорания топлива
Под характеристиками топлива понимают химический состав, теплотворную способность и количественные соотношения между воздухом и топливными компонентами, определяющие баланс исходных и конечных продуктов процесса сжигания топлива, а также его температурный уровень.
Химический состав характеризует природу и количественное соотношение элементов топлива, что позволяет выяснять его отличительные признаки. Горючие газы представляют собой механическую смесь различных газов и их свойства определяют по сумме элементов, выраженной в % по объему:
 (1.1)
(1.1)
Каменный уголь, сланцы и мазут отличаются в сущности неопределенной химической природой связи элементов и их средние свойства находят по суммарному элементарному составу всей рабочей массы, % по массе:
 (1.2)
(1.2)
Горючими элементами топлива являются: в газах — углеводороды  ,
,  и окись углерода
и окись углерода  , в твердом и жидком топливе - углерод
, в твердом и жидком топливе - углерод 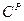 , водород
, водород  и горючая сера
и горючая сера  . В топливе содержатся также негорючие элементы, представляющие собой балласт: влага
. В топливе содержатся также негорючие элементы, представляющие собой балласт: влага  и
и  , минеральная часть (зола)
, минеральная часть (зола)  , азот
, азот  и
и  и двуокись углерода
и двуокись углерода  . Небольшое количество кислорода
. Небольшое количество кислорода  и
и  , содержащегося в топливе, участвует в горении как окислитель горючих элементов.
, содержащегося в топливе, участвует в горении как окислитель горючих элементов.
Теплоту сгорания топлива определяют экспериментально в калориметрической установке, при этом находят количество теплоты  , которое выделяется в ней на единицу массы (или объема) топлива. Существует и расчетный метод определения теплоты сгорания топлива по его элементарному составу. Технической стандартной величиной является высшая теплота сгорания
, которое выделяется в ней на единицу массы (или объема) топлива. Существует и расчетный метод определения теплоты сгорания топлива по его элементарному составу. Технической стандартной величиной является высшая теплота сгорания  , Дж/кг, равная теплоте сгорания в калориметрической установке за вычетом теплоты образования и растворения в воде получающихся при сжигании топлива окислов серы и азота. Значение
, Дж/кг, равная теплоте сгорания в калориметрической установке за вычетом теплоты образования и растворения в воде получающихся при сжигании топлива окислов серы и азота. Значение  соответствует условию, при котором все водяные пары в составе продуктов сгорания переходят в жидкое состояние при 0°С. В технических расчетах за основной показатель принимают низшую теплоту сгорания
соответствует условию, при котором все водяные пары в составе продуктов сгорания переходят в жидкое состояние при 0°С. В технических расчетах за основной показатель принимают низшую теплоту сгорания  , Дж/кг, отнесенную ко всей его рабочей массе. Она равна
, Дж/кг, отнесенную ко всей его рабочей массе. Она равна  минус теплота испарения водяного пара из физической влаги
минус теплота испарения водяного пара из физической влаги  и пара, образующегося при сжигании водорода
и пара, образующегося при сжигании водорода  :
:
 (1.3)
(1.3)
где 25 и 9 — соответственно количество скрытой теплоты парообразования, кДж на 1 % сконденсированного в калориметрической установке водяного пара и стехиометрический коэффициент пересчета  на воду.
на воду.


 Рисунок 1.1. - Калориметрическая установка для определения теплоты сгорания твердого и жидкого топлива
Рисунок 1.1. - Калориметрическая установка для определения теплоты сгорания твердого и жидкого топлива
а — калориметрическая бомба для сжигания топлива; б — общая схема установки

Рисунок 1.2. - Калориметрическая установка для определения теплоты сгорания газообразного топлива
Основным узлом установки для определения теплоты сгорания твердого и жидкого топлива является калориметрическая бомба (рис. 1.1, а), которая состоит из стакана 1, изготовленного из кислотоупорной стали, с ножками 13 и навинчивающейся сверху крышкой 8. Для герметичности между стаканом и крышкой прокладывают свинцовое кольцо 7. В крышке имеется три отверстия: 4 — для впуска в стакан кислорода через трубку 3, 6 — для выпуска из него продуктов сгорания и 5 — для ввода в стакан стержня 9, являющегося проводником электрического тока. К кислородной трубке 3 прикреплено кольцо 1I, на которое устанавливают платиновую чашку 12 с пробой топлива. На трубке 3 и стержне 9 имеются крючки 2 дли закрепления зажигательной проволоки 10, концы которой вводят в чашку 12. Перед опытом заряженный стакан помещают в калориметр, при этом крышка должна быть завинчена, в бомбу заложена проба топлива и накачен кислород давлением 2,5 МПа, вентили отверстий для впуска кислорода и вывода продуктов сгорания перекрыты.
Калориметр (рис. 1.1, б) представляет собой латунный никелированный сосуд 8, который во избежание потерь тепла в окружающую среду помещают во второй (внешний)  сосуд 3 с двойными стенками, между которыми залита вода. В калориметр 8 должно быть залито точно отвешенное количество воды (около 3 кг) для поглощения тепла от стенок бомбы. Калориметр снабжен мешалкой 2 с электродвигателем 4. Внешний сосуд закрыт эбонитовой крышкой 5, через нее вставлен термометр 7 для измерения температуры воды в сосуде 8, а также подведены провода 6 для зажигания пробы топлива в бомбе электрической искрой. При проведении опыта пускают в ход мешалку, воспламеняют пробу топлива и следят за температурой воды в калориметре, регулируя изменение ее, значения во времени до момента полной стабилизации.
сосуд 3 с двойными стенками, между которыми залита вода. В калориметр 8 должно быть залито точно отвешенное количество воды (около 3 кг) для поглощения тепла от стенок бомбы. Калориметр снабжен мешалкой 2 с электродвигателем 4. Внешний сосуд закрыт эбонитовой крышкой 5, через нее вставлен термометр 7 для измерения температуры воды в сосуде 8, а также подведены провода 6 для зажигания пробы топлива в бомбе электрической искрой. При проведении опыта пускают в ход мешалку, воспламеняют пробу топлива и следят за температурой воды в калориметре, регулируя изменение ее, значения во времени до момента полной стабилизации.
Калориметрическая установка для определения теплоты сгорания газообразного топлива (рис. 1.2) состоит из четырех основных частей: калориметра 10, счетчика расхода газа 1, регулятора давления газа 20 и весов для учета расхода охлаждающей воды 18. Исследуемый газ по трубке поступает в счетчик, снабженный манометром 5 и термометром 3, далее по трубке 22 направляется в регулятор давления 20, за которым в газовой линии поддерживается постоянное давление посредством дросселирования на основе показаний дифманометра 21. Газ зажигается бунзеновской горелкой 17, инжектирующей окружающий воздух через регулировочную шайбу 16. Вода, получаемая в результате конденсации содержащихся в продуктах сгорания водяных паров, собирается в мерный цилиндр 19. Температуру сухих продуктов сгорания, выбрасываемых из калориметра, контролируют термометром 9. Вода поступает в калориметр из бачка 7. Постоянный расход ее поддерживается регулировочным краном 6. Избыток воды сливается по трубке 4, минуя калориметр. Использованная для охлаждения калориметра вода выходит из него в коллектор II, за которым установлен кран-переключатель 12, благодаря чему вода может направляться по трубке 13 в установленное на весах ведро 14 либо по трубке 15 сливается в воронку, минуя весы. Разность температур воды на входе в калориметр и выходе из него определяют при помощи двух термометров 8. При исследовании на описанной установке теплоты сгорания легких жидких видов топлива (горючего для двигателей внутреннего сгорания) газовую горелку 17 заменяют форсункой, а вместо газового счетчика 1 и регулятора давления 20 устанавливают весовой дозатор, обеспечивающий постоянную подачу топлива к форсунке.
Калориметрическая установка действует по схеме непрерывного тока топлива, теплота сгорания которого отводится тоже непрерывным током охлаждающей воды. По обеим описанным установкам (см. рис. 1.1 и 1.2) результаты опытов позволяют подсчитать теплоту сгорания топлива по методам, изложенным в инструкциях, которыми должны быть снабжены эти установки.
Теплоту сгорания топлива рассчитывают по его элементарному составу, исходя из тепловых эффектов окислительных реакций, протекающих при горении каждого элемента:
для твердого и жидкого топлива  , Дж/кг (формула Д. И. Менделеева),
, Дж/кг (формула Д. И. Менделеева),
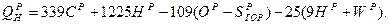 (1.4)
(1.4)
для газообразного топлива QPH, Дж/м3,
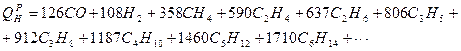 (1.5)
(1.5)
Соотношения между воздухом и топливными компонентами подсчитывают по расходу воздуха и выходу продуктов сгорания топлива. Окружающий воздух содержит кислород и азот по объему:  и
и  ; по массе:
; по массе:  и
и  . При температурах 0 - 20°С относительную влажность воздуха можно принимать j»60%, абсолютную d»12 г/м3 или 1% объема влажного воздуха. Необходимый для сгорания топлива расход воздуха можно подсчитать в массовых или объемных единицах — оба метода, естественно, дают одинаковые результаты. При этом безразлично, находятся ли топ
. При температурах 0 - 20°С относительную влажность воздуха можно принимать j»60%, абсолютную d»12 г/м3 или 1% объема влажного воздуха. Необходимый для сгорания топлива расход воздуха можно подсчитать в массовых или объемных единицах — оба метода, естественно, дают одинаковые результаты. При этом безразлично, находятся ли топ  ливные элементы в каких-либо химических связях между собой или формулы связи их неизвестны.
ливные элементы в каких-либо химических связях между собой или формулы связи их неизвестны.
Теоретически необходимый для полного сгорания топлива удельный расход сухого воздуха определяют по формулам:
для твердого и жидкого топлива (м3 на 1 кг топлива)
 ; (1.6)
; (1.6)
для газообразного топлива (м3 на 1 м3 топлива)
 . (1.7)
. (1.7)
При отсутствии точных данных о характере соединений углеводородов  их принимают состоящими целиком из этилена
их принимают состоящими целиком из этилена  .
.
Для единообразной оценки теплового качества натурального топлива различных видов применяют эталон, называемый условным топливом, теплота сгорания которого равна 29310 кДж/кг. Теоретический выход продуктов сгорания, который получился бы при полном сжигании топлива с теоретическим расходом воздуха, можно подсчитать по формулам для каждого получающегося компонента (табл. 1.1).
Таблица 1.1. Теоретический выход продуктов сгорания
| Продукты сгорания | Выход продуктов сгорания при сжигании топлива | |
| твердого и жидкого, м3 на 1 кг топлива | Газообразного, м3 на 1 м3 топлива | |
| Азот |  (1.8) (1.8)
|  (1.9) (1.9)
|
| Сухие трехатомные газы |  (1.10) (1.10)
|  (1.11)
(1.11)
|
| Водяной пар |  (1.12)
(1.12)
|  (1.13)
(1.13)
|
В формуле (1.13) влажность газообразного топлива  в зависимости от его температуры
в зависимости от его температуры  можно принимать равной:
можно принимать равной:
 , г/м3 , г/м3
| 4,98 | 10,06 | 19,4 | 64,6 | 202,5 | 738,7 |
 , °C , °C
|
Таким образом, общий теоретический выход продуктов сгорания топлива равен сумме:
 (1.14)
(1.14)
В практических условиях топливо сжигается с некоторым избытком воздуха по сравнению с теоретическим, причем коэффициент избытка воздуха a обычно колеблется в пределах 1,1— 1,5, в связи с чем практические количественные соотношения расхода влажного воздуха и выхода продуктов сгорания составляют:
удельный расход воздуха
 ; (1.15)
; (1.15)
удельный выход продуктов сгорания
 . (1.16)
. (1.16)
Температуру горения топлива разделяют на калориметрическую и практическую (расчетную). Первую из них  подсчитывают по теплоте сгорания, отнесенной к рабочей массе топлива, исходя из адиабатических условий горения, когда потери тепла камерой сгорания и эндотермические эффекты диссоциации продуктов сгорания принимают равными нулю. Подсчитывая температуру
подсчитывают по теплоте сгорания, отнесенной к рабочей массе топлива, исходя из адиабатических условий горения, когда потери тепла камерой сгорания и эндотермические эффекты диссоциации продуктов сгорания принимают равными нулю. Подсчитывая температуру  в отличие от
в отличие от  , учитывают диссоциацию продуктов сгорания при теоретическом расходе топлива, а физические тепловые потери не учитывают. При подсчете
, учитывают диссоциацию продуктов сгорания при теоретическом расходе топлива, а физические тепловые потери не учитывают. При подсчете  следует учитывать все факторы реального процесса: избыток воздуха, степень диссоциации продуктов сгорания, эндотермические эффекты минеральной части топлива, а также отвод тепла из камеры сгорания, включающий тепловые потери во внешнюю среду через стенки и прямое излучение тепла через открытые отверстия камеры, а также химический и механический недожог топлива. Все перечисленные методы опираются на балансовые соотношения, вытекающие из закона сохранения энергии Р. Майера.
следует учитывать все факторы реального процесса: избыток воздуха, степень диссоциации продуктов сгорания, эндотермические эффекты минеральной части топлива, а также отвод тепла из камеры сгорания, включающий тепловые потери во внешнюю среду через стенки и прямое излучение тепла через открытые отверстия камеры, а также химический и механический недожог топлива. Все перечисленные методы опираются на балансовые соотношения, вытекающие из закона сохранения энергии Р. Майера.
 Если принять на единицу сжигаемого топлива:
Если принять на единицу сжигаемого топлива:  — начальное (до горения) теплосодержание реагирующих веществ (элементов топлива с воздухом),
— начальное (до горения) теплосодержание реагирующих веществ (элементов топлива с воздухом),  — теплоту диссоциации трехатомных газов и
— теплоту диссоциации трехатомных газов и  — потери теплоты в зоне горения, то указанные температуры горения топлива (°С) могут быть представлены отношениями:
— потери теплоты в зоне горения, то указанные температуры горения топлива (°С) могут быть представлены отношениями:
 ; (1.17)
; (1.17)
 ; (1.18)
; (1.18)
 (1.19)
(1.19)
где  и
и  — средняя теплоемкость смеси продуктов сгорания при соответствующих искомых температурах.
— средняя теплоемкость смеси продуктов сгорания при соответствующих искомых температурах.
Для упрощения формулы (1.19) применяют пирометрический коэффициент e, значения которого находят опытным путем. Он представляет собой по физическому смыслу тепловой к.п.д. топки и учитывает долю всех тепловых потерь, при сжигании топлива  , возрастающих с ухудшением организации топочного процесса. Значения этого параметра колеблются в пределах 0,6—0,9. Таким образом, расчетная формула (1.19) получает вид
, возрастающих с ухудшением организации топочного процесса. Значения этого параметра колеблются в пределах 0,6—0,9. Таким образом, расчетная формула (1.19) получает вид
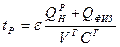 . (1.20)
. (1.20)
Средние значения теплоемкости продуктов сгорания можно подсчитать аддитивным способом по формуле
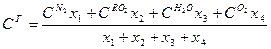 (1.21)
(1.21)
где 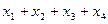 — объемные доли соответствующих индивидуальных газовых компонентов в составе продуктов сгорания. При решении задач по формулам (1.17) — (1.19) теплоемкость газовых компонентов, входящих в формулу (1.21), берут по справочным данным при искомой температуре, которая заранее неизвестна. Кроме того, приходится пользоваться методом интерполяции.
— объемные доли соответствующих индивидуальных газовых компонентов в составе продуктов сгорания. При решении задач по формулам (1.17) — (1.19) теплоемкость газовых компонентов, входящих в формулу (1.21), берут по справочным данным при искомой температуре, которая заранее неизвестна. Кроме того, приходится пользоваться методом интерполяции.
Диссоциация трехатомных газов, находящихся в продуктах сгорания, протекает с поглощением тепла по реакциям:

Константы равновесия этих реакций определяют отношения парциальных давлений исходного количества  и
и 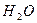 и продуктов диссоциации
и продуктов диссоциации  ,
,  и
и  :
:
 ; (1.22)
; (1.22)
 . (1.23)
. (1.23)
В качестве меры диссоциации принимают отношение количества распавшегося вещества к количеству исходного. Эту меру называют степенью диссоциации, которая количественно связана с константой равновесия общей зависимостью:
 , (1.24)
, (1.24)
где  — степень диссоциации
— степень диссоциации  и
и 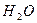 ;
;  и
и  — число молей избыточного кислорода на моль диссоциирующего газа и число молей газа, не принимающих участия в реакции;
— число молей избыточного кислорода на моль диссоциирующего газа и число молей газа, не принимающих участия в реакции;  — общее давление газовой смеси.
— общее давление газовой смеси.
В практических условиях значение  близко к атмосферному давлению, а влиянием содержания в продуктах сгорания гидроокислов и атомарных газов можно пренебречь. При этих допущениях уравнение (1.24) преобразуется к упрощенному виду
близко к атмосферному давлению, а влиянием содержания в продуктах сгорания гидроокислов и атомарных газов можно пренебречь. При этих допущениях уравнение (1.24) преобразуется к упрощенному виду
 (1.25)
(1.25)
Константы равновесия реакций диссоциации [уравнения (1.22) и (1.23)] имеют количественную связь с абсолютной температурой:
 (1.26)
(1.26)
 (1.27)
(1.27)
Рассматривая совместно уравнения, характеризующие диссоциацию трехатомных газов, можно установить функциональную зависимость степени диссоциации от температуры. Изменение степени диссоциации двуокиси углерода и водяного пара  и
и  в долях единицы в зависимости от изменения их температуры показано на кривых рис. 1.3.
в долях единицы в зависимости от изменения их температуры показано на кривых рис. 1.3.
В результате суммарная теплота диссоциации трехатомных газов может быть подсчитана по формуле (кДж на 1 кг твердого и жидкого топлива, кДж на 1 м3 газообразного топлива)
 (1.28)
(1.28)
где  и
и 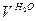 — выход
— выход  и
и 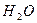 , м3 на 1 кг твердого и жидкого топлива или кг на 1 м3 газообразного топлива;
, м3 на 1 кг твердого и жидкого топлива или кг на 1 м3 газообразного топлива;  =12600 кДж и
=12600 кДж и  =10 800 кДж — теплота диссоциации 1 м3,
=10 800 кДж — теплота диссоциации 1 м3,  и
и  , равная тепловым эффектам их окисления.
, равная тепловым эффектам их окисления.
Таблица 1.2.Предельная концентрация (% по объему)горючих газов для воспламенения газовоздушной смеси
| Газ | Предел | |
| Нижний | Верхний | |
| Метан CH4 | ||
| Окись углерода CO | 12.5 | |
| Водород H2 |
 Сжигание газообразного топлива отличается тем, что воспламенение его может произойти только при определенном соотношении «газ — воздух». За пределами его газовоздушная смесь не может воспламениться вследствие недостаточного выделения тепла для нагрева смеси до нужной температуры. В табл. 1.2 приведены данные о нижних и верхних пределах воспламенения газовоздушных смесей.
Сжигание газообразного топлива отличается тем, что воспламенение его может произойти только при определенном соотношении «газ — воздух». За пределами его газовоздушная смесь не может воспламениться вследствие недостаточного выделения тепла для нагрева смеси до нужной температуры. В табл. 1.2 приведены данные о нижних и верхних пределах воспламенения газовоздушных смесей.


Рис. 1.3. Степень диссоциации трехатомных газов
а — двуокись углерода; б — водяной пар; 1 — парциальное давление 0,01 МПа; 2 — то же, 0,02 МПа; 3 — 0,03 МПа; 4—0,04 МПа; 5 — 0,05 МПа; 6 — 0,06 МПа