 |
|
НАСИЧЕНІ АЛЬДЕГІДИ ТА КЕТОНИ
До насичених альдегідів та кетонів відносять оксосполуки, радикали котрих є радикалами насичених вуглеводнів (алкіли).
Номенклатура. Альдегіди називають за номенклатурою ІЮПАК (м) як відповідні вуглеводні, до яких додають суфікс –аль (нумерацию головного ланцюга починають з атома вуглецю функціональної групи). За раціональною номенклатурою (р) – виходячи від оцтового альдегіда (Н3С-С(О)Н) Для них также росповсюджена тривіальна номенклатура (т) (див. табл. ХХХ).
Кетони також називають як відповідний вуглеводень, додаючи суфікс –он і вказуючи номер атома вуглецю карбонільної групи (м) (повинен бути найменьшим), та по назві радикалів, сполучених з карбонільною группою (р) (див. табл. ХХХ).
Ізомерія.Оксосполукам характерна структурна ізомерія (А), а для кетонів і положення функціональної групи (В) (див. с. ХХХ ).

бутаналь 2-метилпропаналь пентанон-2 пентанон-3
Фізичні властивості.Мурашиний альдегід – газ, нижчі альдегіди та кетони – леткі рідини. Добре розчинні в органічних розчинниках.
Таблица ХХХ
Номенклатура деяких оксосполук
| Формула | Номенклатура | Формула | Номенклатура |
| Альдегіди | Кетони | ||

| м: метаналь | 
| м: пропанон |
| р: - | р: диметилкетон | ||
| т: мурашиний | т: ацетон | ||

| м: етаналь | 
| м: бутанон |
| р: оцтовий | р: метилетилкетон | ||
| т: оцтовий | т: - | ||

| м: пропаналь | 
| м: пентанон-2 |
| р: метилоцтовий | р: етилпропилкетон | ||
| т: пропіоновий | т: - | ||
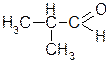
| м: 2-метилпропаналь | 
| м: 2,5-диметилгексан-он-3 |
| р: диметилоцтовий | р: ізопропілізобутил-кетон | ||
| т: ізомасляний | т: - |
Хімічні властивості.Хімічні властивості оксосполук визначає наявність оксогрупи (альдегіди та кетони досить реакційноздатні сполуки).
Зв’язок С=О в оксогрупі, на відміну від етиленового С=С, досить поляризований, електронна густина зміщена в бік кисню і атом вуглецю набуває часткового позитивного заряду (див. мал.).

Завдяки цьому оксосполукам характерні реакціі нуклеофільного приєднання.
Як електроакцептор оксогрупа збільшує рухливість гідрогену при α-вуглецевому атомі і оксосполуки проявляють СН-кислотність. Вони також вступають у реакції відновлення-окислення, конденсації та полімерізації.
Реакції нуклеофільного приєднання.
Альдегіди та кетони приєднують різні сполуки, а саме воду, синильну кислоту, гідросульфіт натрію, спирти та інше.
- приєднання води. Альдегіди приєднують воду (І, див. мал.), утворюючи гідрати (ІІ). Гідрати сполуки нестійкі, існують тільки в розчинах. Кетони воду не приєднують.
- приєднання синільної кислоти. Оксосполуки приєднують синільну кислоту (ІІІ) і утворюють оксинітрили (ІV), які є проміжними сполуками при синтезі окси- та аміноспиртів.
- приєднання гідросульфіту натрію. При взаємодії із гідросульфітом натрію (V) утворюються кристалічні сполуки (VI) – бісульфітні похідні. Реакція використовується для виділення та очистки альдегідів та кетонів. Із кетонів у цю реакцію вступають лише ті, які містять хоча б один метильний радикал.

Приєднання альдегідами аміаку (I) та первічних амінів (III) супроводжується відщепленням молекули води і веде до утворення альдімінів (II) і імінів (IV).

Кетони теж взаємодіють із аміаком, але утворюють більш складні сполуки.
Реакції заміщення.
Оксосполуки взаємодіють із галогенуючими реагентами. В залежності від умов проведення реакції та природи реагента утворюються різні сполуки. При взаємодії із галогенідами фосфору кисень оксогрупи заміщується на два галогени (І), а при використанні молекулярного хлору або брому виявляється СН-кислотність і заміщення гідрогену на галоген відбувається при α-вуглецевому атому (ІІ)

Реакції відновлення та окислення.
- реакції відновлення широко застосовують для добування спиртів (альдегіди відновлюються до первинних спиртів, кетони - до вторинних):

альдегід первинний спирт кетон вторинний спирт
- реакції окислення для альдегідів і кетонів відбуваються по різному: альдегіди окислюються досить легко (киснем повітря) до відповідних кислот, кетони – більш стійкі сполуки:

альдегід кислота кетон
Способи добування.
- окислення спиртів (див.с. ХХХ).
- окислення алкенів (див. с. ХХХ).
- відновлення карбонових кислот (див. с. ХХХ – кислоти).
- гідратацією ацетиленових вуглеводнів (див. с. ХХХ).
- гідроліз дигалогеналканів (гемінальних):

1,1-дибромпропан нестійкий проміжний двоатомний спирт пропаналь
- піроліз кальцієвих солей карбонових кислот:

ацетат кальцію ацетон