 |
|
НАСИЧЕНІ МОНОКАРБОНОВІ КИСЛОТИ
Загальна формула насичених монокарбонових кислот – СnH2n+1-COOH або R-COOH.
Номенклатура.За номенклатурою ІЮПАК (м) кислоти називають як відповідні вуглеводні, до яких додають закінчення –ова і слово кислота (нумерацию головного ланцюга починають з атома вуглецю функціональної групи). За раціональною номенклатурою (р) – виходячи від оцтової кислоти (Н3С-СООН) Для них также росповсюджена тривіальна номенклатура (т) (див. табл. ХХХ).
Якщо відняти від карбонової кислоти гідроксил - ОН, то одержують залишок карбонової кислоти - ацильну групу (ацил, див. мал.). Назви ацильних груп утворюють від назв ІЮПАК відповідних вуглеводнів, з додаванням закінчення -оїл. Широко також вживаються тривіальні назви ацилів:

ацил форміл ацетил пропіоніл ізобутиріл
метаноїл етаноїл пропаноїл ізобутаноїл
Ізомерія.Для насичених монокарбонових кислот ізомерія зумовлена різною будовою вуглецевого радикала.
Таблица ХХХ
Номенклатура деяких насичених карбонових кислот
| Формула | Номенклатура | Формула | Номенклатура |
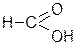
| м: метанова | 
| м: пентанова |
| р: - | р: пропілоцтова | ||
| т: мурашина | т: валеріанова | ||
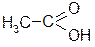
| м: етанова | 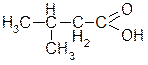
| м: 3-метилбутанова |
| р: оцтова | р: ізопропілоцтова | ||
| т: оцтова | т: ізовалеріанова | ||
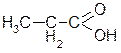
| м: пропанова | 
| м: гексадеканова |
| р: метилоцтова | р: - | ||
| т: пропіонова | т: пальмітинова | ||
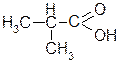
| м: 2-метилпропанова | 
| м: октадеканова |
| р: диметилоцтова | р: і- | ||
| т: ізомасляна | т: стеаринова |
Фізичні властивості.Карбонові кислоти з С1-С3 - безбарвні рідини з гострим запахом, з С4-С9 - маслянисті рідини з неприємним запахом, починаючи від С10- тверді речовини без кольору і запаху. Низькомолекулярні кислоти добре розчинні у воді, зі збільшенням молекулярної маси розчинність кислот зменшується. Температура кипіння карбонових кислот вища, ніж відповідних спиртів. Це зумовлено їхньою здатністю до асоціації з утворенням лінійних або циклічних димерів за рахунок водневого зв'язку:

циклічний димер лінійний димер
Хімічні властивості.Реакційна здатність карбонових кислот зумовлена наявністю карбоксильної групи і будовою вуглеводневого залишку.
На атомі оксигену гідроксильної групи відбувається зміщення електронної хмари і послаблення σ-зв'язку О-Н, у результаті чого атом гідрогену стає рухливим, здатним дисоціювати, також атоми гідрогену сполучені з атомом карбону, що перебуває в α-положенні відносно карбоксильної групи набувають рухливості (СН-кислотність). Отже основні хімічні перетворення карбонових кислот це - вияв кислотних властивостей (утворення солей); заміна гідроксилу у карбоксильній групі на різні угруповання з утворенням функціональних похідних карбонових кислот; СН-кислотні властивості.
Кислотні властивості.
У водних розчинах карбонові кислоти дисоціюють на:
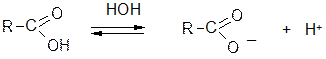
кислота аніон кислоти протон
Одноосновні карбонові кислоти, за винятком мурашиної, слабкі кислоти. Ступінь дисоціації залежить від структури та замісників вуглеводневого радикала, сполученого з карбоксильною групою:
- зі збільшенням кількості вуглецевих атомів радикала сила кислоти послаблюється (див. табл. ХХХ);
- наявність електронодонорних замісників зумовлює ослаблення кислотних властивостей, електроакцептори – посилюють кислотність.
Таблиця ХХХ
Константи дисоціації деяких кислот у воді при 25 оС.
| Назва | Формула | рКа |
| Мурашина | Н-СООН | 3,75 |
| Оцтова | СН3-СООН | 4,76 |
| Пропіонова | СН3-СН2-СООН | 4,87 |
| Масляна | СН3-СН2-СН2-СООН | 4,82 |
| Хлороцтова | ClCH2-COOH | 2,85 |
| Трихлроцтова | Cl3C-COOH | 0,66 |
Карбонові кислоти з металами, оксидами і гідроксидами лужних та лужноземельних металів, карбонатами, основами утворюють солі:
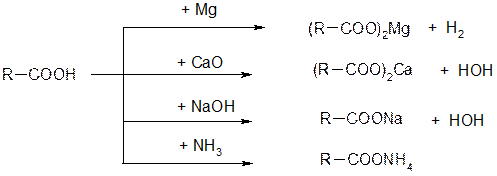
Утворення функціональних похідних карбонових кислот.
Взаємодією кислоти та спирту утворюється естер ( І, реакція етеріфікації). При дії на карбонові кислоти галогенідів фосфору або тіонілхлориду утворюються галогенангідриди карбонових кислот (ІІ) – реакційноздатні речовини, широко застосовувані в органічному синтезі. Ангідриди кислот утворюються внаслідок межмолекулярної дегідротації карбонових кислот при нагріванні в присутності водовіднімаючих засобів (ІІІ). Карбонові кислоти взаємодіють із аміаком (первинними та вторинними амінами). Спочатку утворюються амонієві солі (IV), які при нагріванні в сухому вигляді (піроліз) відщеплюють воду і перетворюються на аміди (V).

СН-кислотність.
В α-положенні відносно карбоксильної групи атоми гідрогену набувають рухливості:

пропанова кислота 2-бромпропанова кислота
Способи добування.Карбонові кислоти знаходяться в природі як у вільному стані, так і у вигляді компонентів деяких природних сполук - жирів, восків і іншіх. Проте здебільшого карбонові кислоти добувають синтетично.
- реакції окислення. Кінцевим продуктом окиснення багатьох органічних сполук (алканів, алкенів, ароматичних вуглеводнів, спиртів, оксосполук) є карбонові кислоти.
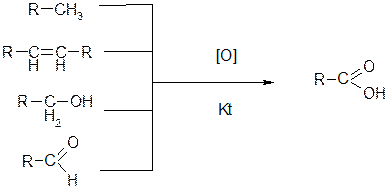
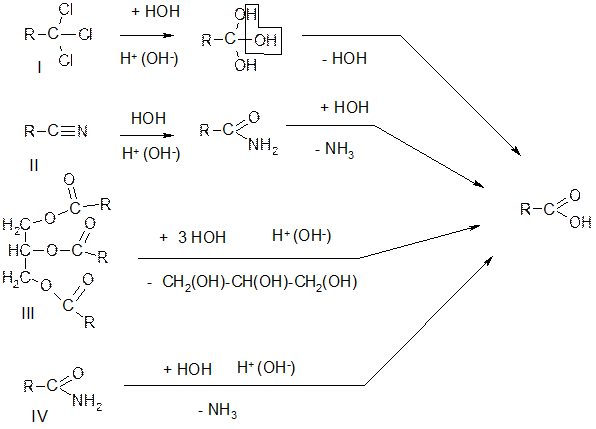
- реакції гідролізу. Карбонові кислоти добувають гідролізом сполук, що містять трихлорометильну групу (І) або ціангрупу (ІІ), а також гідролізом естерів (ІІІ) та амідів (IV).
Також кислоти добувають оксосинтезом та через металоорганічні сполуки.