 |
|
Приклади розв'язування задач
Задача 1
У балоні місткістю 240 л знаходиться повітря при абсолютному тиску 1 МПа ітемпературі 50° С. Визначити тиск, кількість теплоти та зміну ентропії при підвищеннітемператури повітря до 150° С.
Дано: V = 240 л = 0,24м3; P1=1MПа=106 Па; t1=50°С; Т1= 50+273 = 323 К; t2=150°С; T2=150+273=423 K.
Знайти: Р2, Q, ∆S.
Розв'язання:
Процес відбувається при сталому об'емі:
 .
.
3 рівняння стану

знайдемо масу повіря
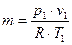 ,
,
де питома газова стала повітря
 ,
,
 ДЖ/кг К,
ДЖ/кг К,
 кг.
кг.
Для ізохорного процессу:
 Па=1,3 МПа.
Па=1,3 МПа.
Кількість теплоти:
 ,
,
де питома масова теплоємність:
 .
.
Повітря є суміш двохатомних газів, тому для нього: і=5,
 Дж/кг К
Дж/кг К
 кДж.
кДж.
Зміна ентропії:
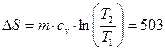 Дж/К,
Дж/К,
Задача 2
Від повітря при сталому тиску 0,2 МПа відводиться теплота. Початковий об'єм повітря 120 л. Початкова температура 200 °С, кінцева 0 °С. Знайти клькість відведеної теплоти, роботу стиснення та зміну внутршньої енергії повітря. Рішення перевірити за допомогою першого закону термодинаміки. Знайти також змінення ентропії повітря.
Дано: V, = 120 л = 0,12м3 ; Р1=Р2=0,2МПа=2*105Па; t1= 200°С; Т1= 473 К; t2= 0°С; Т2=273К.
Знайти: Q, L, ∆U, ∆S.
Розв'язання
Процес ізобарний, р=const, з чого випливає
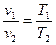 .
.
Звідси
 м3.
м3.
3 рівняння стану  знайдемо масу повітря
знайдемо масу повітря
 кг.
кг.
Кількість теплоти
 ,
,
 [Дж/кг К],
[Дж/кг К],
 кДж
кДж
Работа
 кДж, або
кДж, або
 кДж.
кДж.
Зміна внутршньої енергії:
 кДж.
кДж.
Перший закон термодинаміки:
 : -10,1-25,4=-35,5 кДж.
: -10,1-25,4=-35,5 кДж.
Зміна ентропії:
 Дж/К.
Дж/К.
Задача 3
У процессі ізотермічного стиснення кисню, що має початковий об’єм 0,5 м3, температуру 227° С, тиск 0,6 МПа, від нього відводиться теплота 440 кДж. Визначити кінцеві значення тиску та об’єму газу.
Дано: Газ – кисень О2; µ=32* 10-3 кг/моль; V1=0,5 м3; P1=0,6 МПа=6* 105 Па; t1=227° С, Т1=500 К; Q =-440 кДж.
Знайти: Р2,V2.
Розв'язання
Кількість теплоти в ізотермічному процесі
 ,
,
звідси
 ;
;
 ;
;
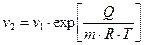 .
.
Масу газу знайдемо з рівняння стану:
 ,
,
де питома газова стала:
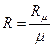 ,
,
 Дж/кг К,
Дж/кг К,
 кг;
кг;
 м3.
м3.
Для ізотермічного процесу:
 Па
Па  МПа.
МПа.
Задача 4
1 кг азоту адіабатно стискається від початкового стану t1=20°С, р1=1000 гПа до тиску р2=5000 гПа. Визначити об’єм та температуру в кінці стиснення, а також роботу процесу. Прийняти k=1,4.
Дано: газ-азот N2; µ=28* 10-3 кг/моль; m=1 кг; k=1,4; P1=1000 гПа=105 Па; P2=5000 гПа=5* 105 Па; t1=20°С, T1=293 K.
Знайти: T2, v2, l.
Розв'язання
Рівняння адіабатного процесу
 ,
,
тобто
 ,
,
або
 .
.
Звідси
 .
.
З рівняння стану

знаходимо
 ,
,
де
 Дж/(кг К),
Дж/(кг К),
 м3/кг;
м3/кг;
 м3/кг;
м3/кг;
 ,
,
або
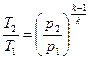 .
.
Звідси
 К.
К.
Робота прцесу
 кДж/кг.
кДж/кг.
Задача 5
Кисень розширюється політропно (n=1,2). Початковий стан газу – тиск 3 МПа, температура 600° С. кінцевий тиск 0,75 МПа. Визначити питомий об’єм та температуру газу наприкінці процесу, а також роботу, теплоту, зміну внутрішньої енергії та ентропії.
Дано: газ – кисень О2; µ=32* 10-3 кг/моль; n=1,4; Р1=3 МПа= 3* 106 Па; Р2=0,75 МПа =0,75* 106Па; t1=600° С, T1=873 K.
Знайти: T2, v2, l, q, ∆u, ∆s.
Розв'язання
З рівняння політропного процесу

впливає:

або
 ,
,
звідси
 ;
;
v1 знайдемо з рівняння стану:
 ,
,
де
 Дж/(кг К).
Дж/(кг К).
 м3/кг;
м3/кг;
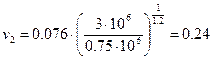 м3/кг;
м3/кг;
 К.
К.
Робота:
 кДж/кг.
кДж/кг.
Теплота:
 .
.
 Дж/кг К;
Дж/кг К;
 ;
;
 кДж/кг.
кДж/кг.
Зміна внутрішньої енергії:
 кДж/кг.
кДж/кг.
Зміна ентропії:
 кДж/(кг К).
кДж/(кг К).