 |
|
Этап 1. Определение теплоёмкости калориметрической системы.
А) Расчетный метод
По формуле (3) рассчитывают постоянную калориметра.
Б) Экспериментальный метод
1. Обработку результатов начинают с построения графика зависимости  , полученной на этапе 1, и нахождения
, полученной на этапе 1, и нахождения  (таблица 1).
(таблица 1).
Типичный вид кривой изменения температуры со временем для эндотермического процесса растворения приведен на рис.3.

| Из графика следует, что весь эксперимент можно разбит на три периода: подготовительный; основной период растворения соли; окончательный. В первом периоде жидкость слегка нагревается за счет трения о мешалку и стенки стакана. Во втором периоде при растворении соли происходит резкое охлаждение жидкости. В третьем периоде, после окончания растворения, жидкость опять слегка начинает нагреваться. Для определения величины DТ при растворении соли поступают следующим образом. Точки В и С, соответствующие началу и концу растворения соли, проектируют на ось ординат, находят середину отрезка nm (проекция кривой растворения на ось ординат) и проводят линию kl. |
| Рис. 3. График для определения изменения температуры |
Экстраполируют линейные участки АВ и CD изменения температуры в первом и третьем периодах до абсциссы точки 1. За DТ принимается величина отрезка EF.2. После этого находят постоянную калориметра K.
2. На основании приведенных в таблице 3 справочных данных строят график зависимости интегральной теплоты растворения взятой для эксперимента соли от моляльной концентрации раствора. Рассчитывают моляльную концентрацию получившегося раствора, принимая плотность воды раной 1 г/см3. По графику определяют величину 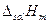 при той моляльной концентрации, которая имела место в опыте.
при той моляльной концентрации, которая имела место в опыте.
Таблица 3
Интегральные теплоты растворения хлорида калия и хлорида аммония в воде
Моляльная концентрация раствора, моль/кг 
| 
| Моляльная концентрация раствора, моль/кг 
| 
| ||
| KCl | NH4Cl | KCl | NH4Cl | ||
| 0.01 | 17.23 | 14.85 | 0.4 | 17.55 | 15.27 |
| 0.02 | 17.39 | 14.94 | 0.5 | 17.50 | 15.27 |
| 0.05 | 17.44 | 15.02 | 1.0 | 17.43 | 15.31 |
| 0.1 | 17.51 | 15.10 | 2.0 | 17.28 | 15.27 |
| 0.2 | 17.55 | 15.19 | 3.0 | 16.72 | 15.23 |
| 0.3 | 17.57 | 15.23 | 4.0 | 16.17 | 15.19 |
3. Постоянную калориметра рассчитывают по формуле (5). Эту величину используют в дальнейших расчетах.
4*. Рассчитав постоянную калориметра, определяют теплоемкость материала стакана (полиэтилена), используя формулу (3).