 |
|
Промежуточное состояние
Рис. 1.4. Цикл процесса для определения теплоты образования
кристаллогидрата: 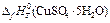 – мольная теплота образования кристаллогидрата;
– мольная теплота образования кристаллогидрата; 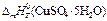 – мольная теплота растворения кристаллогидрата;
– мольная теплота растворения кристаллогидрата; 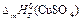 – мольная теплота растворения
– мольная теплота растворения
безводной соли
Порядок выполнения работы
1. Взвесить две одинаковые навески кристаллогидрата CuSO4×5H2O (2¸10 г). Выдержать одну навеску в сушильном шкафу при температуре 200¸250 °С до постоянной массы (голубая окраска кристаллогидрата перейдет в белую окраску безводной соли CuSO4). Безводную соль охладить и хранить в герметичной пробирке.
2. Определить температурный ход калориметрического опыта и величину DТ1 при растворении кристаллогидрата. Для этого налить в калориметрический сосуд 900 см3 дистиллированной воды и внести в главном периоде калориметрического опыта точную навеску кристаллогидрата. По окончании опыта освободить калориметрический сосуд.
3. Определить температурный ход калориметрического опыта и DТ2 при растворении безводной соли. Для этого внести в главном периоде калориметрического опыта точную навеску безводной соли.
4. Определить температурный ход калориметрического опыта и изменение температуры DТ3 при пропускании через систему определенного количества теплоты.
Примечание.Пункты 2-4 выполняются по методике, описанной в работе 1. Полученные опытные данные представить в виде таблиц и графиков, из которых определить DТ в каждом опыте.
Обработка опытных данных
1. Вычислить теплоемкость калориметрической системы:
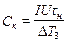 , (1.29)
, (1.29)
где I – сила тока, А; U – напряжение, В; tн – время пропускания тока (продолжительность нагревания), с.
2. Вычислить интегральную мольную теплоту растворения кристаллогидрата
 ,
,
где m1 и M1 – соответственно масса и молярная масса кристаллогидрата.
3. Рассчитать интегральную мольную теплоту растворения безводной соли:
 ,
,
где m2 и M2 – соответственно масса и молярная масса безводной соли.
4. По формуле (1.28) рассчитать теплоту образования кристаллогидрата и сравнить полученное значение со справочным.
Примечание. В качестве объектов исследования можно использовать хлорид алюминия гидрат AlCl3×6H2O, сульфат алюминия гидрат Al2(SO4)3×18H2O, хлорид бария гидрат BaCl2×2H2O, хлорид кальция гидрат CaCl2×6H2O, сульфат железа (II) гидрат FeSO4×7H2O, сульфат железа (III) гидрат Fe2(SO4)3×9H2O.
Контрольные вопросы и задания
1. Что такое теплота образования кристаллогидрата?
2. Опишите методику калориметрического определения теплоты образования кристаллогидрата.
3. Обоснуйте из термохимического цикла формулу для вычисления теплоты образования кристаллогидрата.
Лабораторная работа № 4