 |
|
Определение теплоты нейтрализации
Цель работы: определение теплоты нейтрализации сильной кислоты сильным основанием.
Реактивы: раствор щелочи (KOH или NaOH) концентрацией 0,1 моль/дм3, раствор кислоты (HCl, HNO3) концентрацией
2 моль/дм3.
Теоретические сведения
Теплотой нейтрализации называется количество теплоты, выделяющееся при взаимодействии 1 моль кислоты с 1 моль основания. Этот тепловой эффект при взаимодействии сильных кислот и сильных оснований отвечает реакции образования
молекул воды из ионов H+ и OH–:
 ,
, 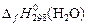 ,
,
где 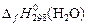 = -57,1 кДж/моль [6].
= -57,1 кДж/моль [6].
При вливании раствора сильной кислоты в раствор щелочи кроме процесса нейтрализации протекают процессы разбавления кислоты щелочью с тепловым эффектом DН1 и разбавления щелочи кислотой с тепловым эффектом DН2. Суммарный тепловой эффект процесса DНизм при этом равен:
DНизм = 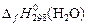 + DН1 + DН2.
+ DН1 + DН2.
Порядок выполнения работы
1. Определить температурный ход калориметрического опыта и величину DТ1 при смешивании щелочи и кислоты. Для этого налить в калориметрический сосуд 400 см3 щелочи, к которой в главном периоде калориметрического опыта добавить пипеткой 10 см3 кислоты. По окончании опыта освободить калориметрический сосуд.
2. Определить температурный ход калориметрического опыта и DТ2 при разбавлении кислоты щелочью. Для этого налить в калориметрический сосуд 400 см3 дистиллированной воды, к которой в главном периоде добавить пипеткой 10 см3 кислоты.
3. Определить температурный ход калориметрического опыта и DТ3 при пропускании через систему определенного количества теплоты.
Примечание.Пункты 1-2 выполняются по методике, описанной в работе 1. Полученные опытные данные представить в виде таблиц и графиков, из которых определить DТ в каждом опыте.
Обработка опытных данных
1. Вычислить теплоемкость калориметрической системы по уравнению (1.29).
2. Вычислить суммарный тепловой эффект процесса по формуле
 ,
,
где m1 и M1 – соответственно масса и молярная масса сильной кислоты.
3. Рассчитать теплоту разбавления кислоты щелочью
 .
.
4. Теплоту разбавления щелочи водным раствором кислоты DН2 можно считать равной нулю, так как объем щелочи мало изменяется при вливании в него кислоты.
5. Теплоту нейтрализации вычислить по уравнению
DНнейтр = 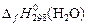 = DНизм – DН1.
= DНизм – DН1.
Полученный результат сравнить со справочным значением.
Контрольные вопросы и задания
1. Какие процессы сопровождают нейтрализацию сильной кислоты сильным основанием? Что такое теплота нейтрализации?
2. Какие процессы сопровождают нейтрализацию сильной кислоты слабым основанием (слабой кислоты сильным основанием)?
3. Как вычислить теплоту диссоциации слабой кислоты из значений теплот нейтрализации слабой кислоты сильным основанием?
4. Опишите методику калориметрического определения теплоты нейтрализации.
Лабораторная работа № 5