|
|
Константа рівноваги
Студентів з фізичної та колоїдної хімії
Спеціальність: 5.05130107
Хімічна рівновага
Питання
1.Рівновага в гетерогенних системах.
2. Визначення констант рівноваги в гетерогенних системах.
Література
Гамеева О.С. Физическая и коллоидная химия. – М.: Высшая школа, 1977, с. 224-226.
Ахметов Б.В. Физическая и коллоидная химия. – Л.:Химия, 1986, с.148-150.
Гамеева О.С. Сборник задач по физической и коллоидной химии. – М.: Высшая школа, 1980, с. 115-118.
Уважно прочитайте увесь матеріал. Виділіть головне.
Розберіться з тим, як треба визначати константи хімічної рівноваги, якщо речовини знаходяться в різних агрегатних станах.
Законспектуйте матеріал.
Студенти повинні
знати:
- сутність та основні характеристики рівноваги;
- формулу для розрахунку констант рівноваги для оборотних гетерогенних реакцій;
вміти:
- розраховувати константу рівноваги в гетерогенних системах;
Питання для самоконтролю
1. Чим відрізняються гетерогенні системи від гомогенних?
2. Як можна визначити константу рівноваги гетерогенних реакцій?
3. При досягненні рівноваги реакції 3Fe + 4Н2О(n) ↔ Fe3О4 + 4Н2
при 2000С парціальний тиск водню дорівнює 127168 Па. Початковий тиск водяної
пари 133322Па. Обчислити константу рівноваги реакції при даній температурі.
(Відповідь:1,825 ·105)
Форма контролю: письмовий
Рівновага в гетерогенних системах
Константа рівноваги
Оборотними гетерогенними процесами є важливі в практичному відношенні реакції:

 С(тв) + СО2(г) 2СО(г)
С(тв) + СО2(г) 2СО(г)

 МgСО3(тв) МgО(тв) + СО2(г)
МgСО3(тв) МgО(тв) + СО2(г)

 2FeО(тв) Fe(тв) + О2(г)
2FeО(тв) Fe(тв) + О2(г)

 Для гетерогенної реакції СаСО3(тв. ) СаО(тв)+ СО2
Для гетерогенної реакції СаСО3(тв. ) СаО(тв)+ СО2
вважають тиск насиченої пари твердих речовин  постійними величинами
постійними величинами 
 .
.

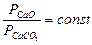
 ;
; 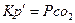 (з урахуванням тільки газоподібної речовини)
(з урахуванням тільки газоподібної речовини)
При обчислюванні константрівноваги гетерогенних реакцій необхідно враховувати тільки парціальні тиски газоподібних речовин, в ступені, що дорівнює стехіометричному коефіцієнту перед даною речовиною в рівнянні хімічної реакції. Наприклад, для реакцій:

 FeО(тв) + СО Fе(тв) + СО2
FeО(тв) + СО Fе(тв) + СО2 

 3Fe + 4Н2О(п) Fe3О4(тв) + 4Н2
3Fe + 4Н2О(п) Fe3О4(тв) + 4Н2 

 2FeО(тв) 2Fe(тв) + О2
2FeО(тв) 2Fe(тв) + О2