 |
|
БІОГЕННІ s-, p-ЕЛЕМЕНТИ
БАЗА ЗАВДАНЬ НА МОДУЛЬ №1
з медичної хімії «Комплексоутворення в біологічних системах»
Для студентів спеціальностей «Лікувальна справа» та «Педіатрія»
І рівень
БІОГЕННІ s-, p-ЕЛЕМЕНТИ
1.1.1. Біогенними називаються елементи:
а) O, C, H, N, P, S. б) I, Zn, Cu, F, Fe;
в) Co, Ni, K, Na, Mg; г) Ca, P, Mg, Fe, Mn.
1.1.2. Елементи-органогени записані у ряді:
а) N,P,K,Mg,Cl, б) C,H,O,N,P,S,
в) C,H,O,Ca,F,Br, г) N,P,S,Ba,O,F.
1.1.3. Елементи-органогени VI групи записані у парі:
а) полоній, сульфур, б) оксиген, селен,
в) оксиген, сульфур, г) селен, телур.
1.1.4. Елементи-органогени V групи записані у парі:
а) бісмут, арсен, б) арсен, фосфор,
в) нітроген, стибій, г) нітроген, фосфор.
1.1.5. До s-елементів відносяться:
а) Na. Mg, Fe, S; б) Na, K, Mg, Ca;
в) O, C, H, N; г) Cu, Co, Fe, Zn.
1.1.6. До p-елементів відносяться:
а) Na. Mg, Fe, S; б) Na, K, Mg, Ca;
в) O, C, N. F; г) Cu, Co, Fe, Zn.
1.1.4. Макроелементи містяться в організмі людини в кількості:
а) >0,01%; б) <0,01%;
в) >0,001; г) <0,001%.
1.1.5. Мікроелементи містяться в організмі людини в кількості:
а) >0,01%; б) <0,01%;
в) >0,1; г) <0,1%.
1.1.7. До макроелементів (більше 0,01%) можна віднести –
а) F, Mg, Fe, Cd; б) Na, K, Сl, Ca;
в) Ca, Cu, Au, N; г) Mn, Co, Fe, Zn.
1.1.8 До макроелементів відносяться:
а) N, Р, K, O, S; б) Na, Cl, Co, Cu;
в) Mg, Na, Al, Si; г) Si, O, F, Fe.
1.1.9. До мікроелементів (10-3 – 10-6%) відносять:
а) Na, K, Сl, Ca, C; б) Mg, Zn, Сu, Fe, J;
в) Ca, Cu, Au, N, F; г) Mn, Cd, Ag, Cl, О.
1.1.10. До мікроелементіввідносяться:
а) Cu, Co, Ni, Mo; б) C, H, Mg, S;
в) Ag, Cu, O, F; г) Cl, Br, J, O.
1.1.11. До незаміннихелементів відносять:
а) Na, K, Сl, Ca, Cd; б) Mg, Zn, Сu, Fe, Hg;
в) Ca, Cu, Au, N, F; г) C, H, O, N, Ca.
1.1.12. До біокаталітичних елементів відносяться:
а) Na. Mg, Fe, S, Р; б) Na, K, Mg, Ca, Ва;
в) Cu, Zn, Mn, Co, Fe; г) O, C, N. F, Н.
1.1.13. Елементи С і О відносяться до:
а) органогенів; б) макроелементів;
в) мікроелементів; г) ультрамікроелементів.
1.1.14. Елементи Si і Se відносяться до:
а) органогенів; б) макроелементів;
в) мікроелементів; г) ультрамікроелементів.
1.1.15. Елементи Ca і P відносяться до:
а) органогенів; б) макроелементів;
в) мікроелементів; г) ультрамікроелементів.
1.1.16. Елементи Hg і Au відносяться до:
а) органогенів; б) макроелементів;
в) мікроелементів; г) ультрамікроелементів.
1.1.17. Елементи Na і K відносяться до:
а) органогенів; б) макроелементів;
в) мікроелементів; г) ультрамікроелементів.
1.1.18. ЙонNa+ має наступну електронну будову:
а) 1s22s22p63s2; б) 1s22s22p63s1;
в) 1s22s22p6; г) 1s22s22p5.
1.1.19. ЙонСа2+ має наступну електронну будову:
а) 1s22s22p63s2; б) 1s22s22p63s1;
в) 1s22s22p6; г) 1s22s22p5.
1.1.20. ЙонS6+ має наступну електронну будову:
а) s22s22p4 б) 1s22s22p63s23p4;
в) 1s22s22p6; г) 1s22s22p63s23p6.
1.1.21. ЙонS2- має наступну електронну будову:
а) 1s22s22p4 б) 1s22s22p63s23p4;
в) 1s22s22p6; г) 1s22s22p63s23p6.
1.1.22. Скільки неспарених електронів має атом Фосфоруу незбудженому стані?
а) 2; б) 3; в) 4; г) 5.
1.1.23. Скільки неспарених електронів має атом Сіліцію у незбудженому стані?
а) 2; б) 3; в) 4; г) 5.
1.1.24. Скільки неспарених електронів має атом Сульфуруу незбудженому стані?
а) 2; б) 3; в) 4; г) 5.
1.1.25.Скільки неспарених електронів має атом Хлору у незбудженому стані?
а) 2; б) 3; в) 4; г) 5.
1.1.26.Які хімічні властивості проявляють вищі оксид і гідроксид елемента з порядковим номером 12?
а) основні, б) кислотні,
в) амфотерні, г) несолетворні.
1.1.27. Які хімічні властивості проявляють оксид і гідроксид елемента з порядковим номером 11?
а) основні, б) кислотні,
в) амфотерні, г) несолетворні.
1.1.28. Які хімічні властивості проявляють оксид і гідроксид елемента з порядковим номером 13?
а) основні, б) кислотні,
в) амфотерні, г) несолетворні.
1.1.29. Які хімічні властивості проявляють оксид і гідроксид елемента з порядковим номером 16?
а) основні, б) кислотні,
в) амфотерні, г) несолетворні.
1.1.30. Які хімічні властивості проявляє N2O?
а) основні, б) кислотні,
в) амфотерні, г) несолетворні.
1.1.31. Які хімічні властивості проявляє NO?
а) основні, б) кислотні,
в) амфотерні, г) несолетворні.
1.1.32. Які хімічні властивості проявляє N2O3?
а) основні, б) кислотні,
в) амфотерні, г) несолетворні.
1.1.33. Які хімічні властивості проявляє NO2?
а) основні, б) кислотні,
в) амфотерні, г) несолетворні.
1.1.34. Які хімічні властивості проявляє N2O5?
а) основні, б) кислотні,
в) амфотерні, г) несолетворні.
1.1.35. Що спільного в будові атомів елементів з порядковими номерами 13 і 31?
а) заряд ядра, б) кількість електронів,
в) кількість енергетичних рівнів,
г) кількість електронів на зовнішньому рівні.
1.1.36. Що спільного в будові атомів елементів з порядковими номерами 6 і 9?
а) заряд ядра, б) кількість електронів,
в) кількість енергетичних рівнів,
г) кількість електронів на зовнішньому рівні.
1.1.37. Що спільного в будові атомів елементів з порядковими номерами 3 і 8?
а) заряд ядра, б) кількість електронів,
в) кількість енергетичних рівнів,
г) кількість електронів на зовнішньому рівні.
1.1.38. Що спільного в будові атомів елементів з порядковими номерами 7 і 15?
а) заряд ядра, б) кількість електронів,
в) кількість енергетичних рівнів,
г) кількість електронів на зовнішньому рівні.
1.1.39. Вкажіть набір порядкових номерів елементів, вищому оксиду яких відповідає кислота типу RO3:
а) 14 і 16; б) 13 і 14; в) 12 і 35; г) 16 і 34.
1.1.40. Вкажіть набір порядкових номерів елементів, вищому оксиду яких відповідає кислота типу RO2:
а) 14 і 16; б) 13 і 14; в) 14 і 32; г) 32 і 33.
1.1.41. Вкажіть набір порядкових номерів елементів, вищому оксиду яких відповідає кислота типу НRO4:
а) 17 і 18; б) 17 і 53; в) 14 і 17; г) 12 і 53.
1.1.42. Вкажіть набір порядкових номерів елементів, вищому оксиду яких відповідає кислота типу відповідає кислота типу Н2RO3:
а) 6 і 14; б) 14 і 16; в) 14 і 28; г) 12 і 34.
1.1.43 Сполуки Sr2+ забарвлюють полум’я в:
а) фіолетовий; б) кармінно-червоний;
в) жовтий колір; г) цегляно-червоний.
1.1.44.Сполуки К+ забарвлюють полум’я в:
а) фіолетовий; б) кармінно-червоний;
в) жовтий колір; г) цегляно-червоний.
1.1.45. Сполуки Сa2+ забарвлюють полум’я в:
а) фіолетовий; б) кармінно-червоний;
в) жовтий колір; г) цегляно-червоний.
1.1.46. Сполуки Вa2+ забарвлюють полум’я в:
а) фіолетовий; б) жовто-зелений;
в) жовтий колір; г) цегляно-червоний.
1.1.47. Сполуки Na+ забарвлюють полум’я в:
а) фіолетовий; б) жовто-зелений;
в) жовтий колір; г) цегляно-червоний.
1.1.48. Серед вказаних формул знайдіть формулу сполуки з ковалентним полярним зв’язком:
а) Cl2, б) NH3, в) N2, г) КClO3.
1.1.49.Серед вказаних формул знайдіть формулу сполуки з ковалентним неполярним зв’язком:
а) I2, б) PH3, в) SO2, г) KCl.
1.1.50. Серед вказаних формул знайдіть формулу сполуки з йонним зв’язком:
а) О2, б) NH3, в) N2О5, г) КCl.
1.1.51. Який р-елемент бере участь у синтезі статевих гормонів (тестостерона) і регулює функцію статевих залоз:
а) Br; б) Cl; в) I; г) Se.
1.1.52.НадлишокF- в організмі викликає захворювання:
а) флюороз; б) карієс зубів;
в) тиреотоксикоз; г) анемію.
1.1.53.Сульфат барію – практично-нерозчинна сіль застосовується в медицині:
а) для промивки гнійних ран;
б) для рентгенодіагностики хвороб ШКТ;
в) як антисептик; г) як обезболюючий засіб.
1.1.54. При дії BaCl2 на який аніон утворюється осад, нерозчинний в оцтовій кислоті?
а) SO42-; б) SO32-; в) PO43-; г) CO32-.
1.1.55. Природний дефіцит йоду в літосфері деяких біогеохімічний провінцій (зокрема в Карпатському регіоні) викликає захворювання:
а) флюороз; б) силікоз;
в) ендемічний зоб; г) анемію.
1.1.56. Бере участь у синтезі гормону інсуліну елемент:
а) Zn; б) Fe; в) Ag; г) Mn.
1.1.57. До складу гормону щитовидної залози тироксину входить елемент:
а) Se; б) Br; в) Cl; г) I.
1.1.58. Який галоген використовують у медичній практиці у вільному стані:
а) фтор, б) хлор, в) бром, г) йод.
1.1.59. Оксиди-елементів V А групи, які використовують у лікарській практиці, записані у парі:
а) N2O, As2O3, б) As2O3. P2O5,
в) NO, P2O5, г) NO2, N2O5.
1.1.60. Яку з галогеногідрогенних кислот містить шлунковий сік:
а) фторидну, б) хлоридну,
в) бромідну, г) йодидну.
1.1.61. При дефіцитi якого елементу в організмі виникає карієс зубів та який метод профілактики використовують:
а) хлору, хлорування води,
б) фтору, додавання фторидів до зубної пасти,
в) йоду, додавання йодидів до харчової солі,
г) бром, додавання бромідів до питної води.
1.1.62. При дефіциті якого елементу в організмі виникає ендемічний зоб та який метод профілактики використовують:
а) хлору, хлорування води,
б) фтору, додавання фторидів до зубної пасти,
в) йоду, додавання йодидів до харчової солі,
г) бром, додавання бромідів до питної води.
1.1.63. Як рентгенконтрасні засоби використовують сполуки елементів, записаних у парі:
а) стронцію, калію, б) плюмбуму, фтору,
в) барію, йоду, г) натрію, арсену.
1.1.64. Для приготування фізіологічного розчину використовують сполуку:
а) натрій хлорид, б) калій хлорид,
в) магній сульфат, г) натрій гіпохлорит.
1.1.65. Кістки та зуби містять такі сполуки фосфору:
а) Са3(РО4)2, б) Са3(Н2РО4)2,
в) Са5(РО4)3ОН, Са5(РО4)3F, г) Ca(HPO4)
1.1.66. Позаклітинними катіонами, в основному, є йони, записані у ряду:
а) Li+, Na+, Ca2+, б) K+, Na+, Ca2+ ,
в) Na+, Mg2+, K+, г) Li+, K+, Ca2+.
1.1.67. Внутрішньоклітинними катіонами, в основному, є іони, записані у парі:
а) K+, Mg+, б) K+, Na+,
в) Na+, Mg+, г) K+,Ca2+.
1.1.68. У молодого чоловіка, який часто вживає алкоголь, на фоні лікування сечогінними засобами виникла сильна м'язова і серцева слабість, блювота, діарея. Причиною такого стану є посилене виділення з сечею йонів:
а) K+, б) Na+, в) Cl¯, г) Ca2+.
1.1.69. Хворому поставлено діагноз –анемія. Недостача якого мінерального елементу призвів до даної патології?
а) Fe, б) Na, в) P, г) Mg.
1.1.70. До якого з йонів центральна нервова система є найбільш чутливою:
а) I-, б) Br-, в) F-, г) Ca2+.
1.1.71. Нітроген утворює кілька оксидів, один з них продукується судинами з метою їх розширення, інший – застосовують для наркозу. У якій парі записані ці оксиди:
а) N2O3, NO, б) NO2, NO,
в) N2O, NO, г) N2O5, NO2.
1.1.72. Професійною хворобою шахтарів є антрикоз. Дана хвороба викликана накопиченням у легенях елементу:
а) Si, б) Al, в) C, г) F.
1.1.73. Спиртовий розчин якого галогену використовують у медичній практиці:
а) брому, б) йоду, в) хлору, г) фтору.
1.1.74. Нашатирний спирт медичний – це є:
а) водний розчин аміаку,
б) спиртовий розчин аміаку,
в) водний розчин натрій хлориду,
г) спиртовий розчин йоду.
1.1.74 Назвати сполуки у вигляді яких літій застосовується в медицині:
а ) літію бромат; б) літію карбонат*;
в) літію барит; г) літію ацетат.
1.1.75. s-Елементами називають елементи:
а) в яких заповнюється зовнішній s-підрівень;
б) головних підгруп; в) малих періодів;
г) в яких заповнюється зовнішній p-підрівень.
1.1.76. p-Елементами називають елементи:
а) побічних підгруп; б) великих періодів;
в) в яких заповнюється зовнішній p-підрівень;
г) малих періодів.
1.1.77. d-Елементами називають елементи:
а) в яких заповнюється передостанній d-підрівень;
б) головних підгруп; в) малих періодів;
г) в яких заповнюється передостанній f-підрівень;
1.1.78. Головна функція цього р-елементу пов'язана з ростом і підтримкою цілісності кісткової тканини і зубів. В організмі дорослої людини його вміст до 86%:
а) Фосфор б) Сульфур
в) Кальцій г) Нітроген
1.1.79. Цей макроелемент входить до складу мембран клітин та нуклеїнових кислот, які беруть участь у процесах росту, ділення клітин, зберігання та використання генетичної інформації:
а) Фосфор б) Сульфур
в) Кальцій г) Нітроген
1.1.80. р-елемент VIIгрупи зменшує вірогідність розвитку карієсу, проте дуже великі дози можуть змінити колір зубів:
а) Фтор б) Хлор
в) Йод г) Астат
1.1.81 В організмі дорослої людини цей макроелемент складає від 1 до 1,5 кг
а) кальцію; б) Цинку
в) Аргентуму г) Меркурію
1.1.82. бере участь у процесі згортання крові:
а) кальцій б) Ферум
в) Хлор г) Бром
1.1.83. Цей мікроелемент метал входить до складу основного мінерального компонента кісткової тканини - оксиапатиту, мікрокристали якого утворюють жорстку структуру кісткової тканини:
а) кальцій б) Фосфор
в) Хлор г) Магній
1.1.83. Який s-елемент зменшує прояви алергічних реакцій при алергічних захворюваннях (сироваткова хвороба, кропив'янка, набряк Квінке, поліноз, бронхіальна астма)?
а) кальцій б) Фосфор
в) Хлор г) Магній
1.1.84. При дефіциті цього макроелементу відбувається порушення росту у дітей, викривлення хребта, кісток нижніх кінцівок, остеопороз, підвищена захворюваність карієсом, поява каменів у нирках:
а) Са б) К в) Р г) Н
1.1.85. Погане згортання крові, множинні синці на тілі внаслідок кровотеч з капілярів тканин, підвищена кровоточивість ясен відбуваються при недостачі такого s-елементу:
а) Са б) K г) Li д) Sr
1.1.86. Цей s-елемент разом з натрієм регулює водний баланс в організмі і нормалізує ритм серця:
а) Калій; б) Барій;
в) Натрій; г) Кальцій
1.1.87. Входить до складу внутрішньоклітинних рідин (50% всіх солей в організмі). Сприяє виведенню з організму зайвої води, допомагає ліквідувати набряки, затримку виділення сечі, необхідний для лікування водянки (асциту).
а) Калій; б) Барій;
в) Натрій; г) Кальцій.
1.1.88. Цей макроелемент нормалізує травлення стимулюючи апетит - оскільки активує фермент амілазу, яка бере участь в утворенні соляної кислоти - основного компонента шлункового соку:
а) Хлор; б) Фосфор;
в) Натрій; г) Кальцій.
1.1.89. Підтримує буферну систему крові, оскільки є головним катіоном позаклітинної рідини, регулює pH крові (концентрацію водневих іонів крові).
а) Натрій; б) Ванадій;
В) Калій; г) Хлор
1.1.90. s-елемент є найважливішим мінералом для серця, бере участь в обміні фосфору. Його дефіцит звичайне явище для людей, що піддаються хронічним стресам.
а) Магній; б) Натрій;
в) Ванадій; г) Хлор.
1.1.91. З наведених нижче сполук найбільш отруйною є:
а) CO; б) CO2;
в) CO(NH2)2; г) SiO2
1.1.92. Одна з класифікацій хімічних елементів грунтується на будові їх електронних оболонок. Згідно неї всі елементи можна поділити на s-, p-, d- і f-елементи. Які з наведених елементів належать до р-елементів?
а) S, P, Cl ; б) K, Ca, Sc
в) Be, Mg, Al; г) Mn, Br, Mo
1.1.93. Одна з класифікацій хімічних елементів грунтується на будові їх електронних оболонок. Згідно неї всі елементи можна поділити на s-, p-, d- і f-елементи. Які з наведених елементів належать до s-елементів?
а) K, Ca, Sc; б) S, P, Cl
в) Be, Mg, Al ; г) Mn, Br, Mo
1.1.94. Ряд неорганічних і органічних лікарських засобів містять атоми елементів з’єднані ковалентним полярним типом хімічного зв’язку. У яких з наведених сполук присутній тільки цей тип зв’язку?
а) H2SO4 ; б) NaCl
в) NH4Сl г) O2
1.1.95. Тіосульфат натрію використовують в медицині як протитоксичний, протизапальний та десенсибілізуючий засіб. Яка з наведених формул сполук є формулою тіосульфату натрію?
а) Na2S2O3; б) Na2S2O5 ;
в) Na2SO3; г) Na2S2O4
1.1.96. Хлорид кальцію застосовують при різних патологічних станах як засіб, що зменшує проникність судин, як кровоспинний засіб. Яка із наведених сполук служить для ідентифікації CaCl2?
а) AgNO3; б) KNO3;
в) HNO3; г) NaCl
1.1.97. Який із перерахованих елементів може проявляти тільки додатній ступінь окиснення ?
а) Магній; б) Бісмут;
в) Сульфур; г) Нітроген.
1.1.98. До розчинів даних солей долили кислоту. В якому випадку спостерігається виділення газу?
а) Na2CO3; б) K2SO4;
в) CuSO4; г) Na2SiO3.
1.1.99. Натрій йодид застосовують у медицині як:
а) Джерело мікроелементу йоду
б) Плазмозамінник
в) Заспокійливий засіб
г) Антацидний засіб
1.1.100. Натрій гідрогенкарбонат застосовують в медичній практиці для лікування захворювань, що супроводжуються ацидозом. До якого типу солей відноситься ця сполука:
а) кисла сіль ;
б) змішана сіль ;
в) середня сіль;
г) основна сіль.
1.1.101. Нітроген утворює сполуки з різними ступенями окислення, деякі з них відіграють важливу роль в організмі людини (регуляція серцево-судинної діяльності, кров’яного тиску). Для якої з даних сполук ступінь окиснення N є найменшим?
а) N2 ; б) NО;
в) N2О; г) NO2
1.1.102. Хлорактивні сполуки широко застосовуються як дезінфікуючі засоби. Яка з наведених формул відповідає гіпохлоритній кислоті?
а) HClO; б) HClO4;
в) HClO2 ; г) HClO3.
1.1.103. Який елемент у вигляді простої речовини є рідиною:
а) Бром; б) Фосфор;
в) Сірка; г) Водень
1.1.104. Солі карбонатної кислоти знаходять дуже поширене застосування. В медицині застосовують при захворюванні шлунку та кишечника, а також при печії, подагрі тощо одну з солей, яка в побуті зветься питною содою. Яка це сіль?
а) NaHCO3; б) Na2CO3;
в) K2CO3; г) Ca(HCO3)2.
1.1.105. В обміні речовин організму людини активно беруть участь біогенні макроелементи. Вміст якого макроелемента у позаклітиній рідині значно вищій, ніж в плазмі клітини?
а) Натрію; б) Калію;
в) Магнію; г) Брому.
1.1.106. Геміоксид нітрогену ( N2O ) використовується для інгаляційного наркозу і має назву:
а) звеселяючий газ;
б) Нашатирний спирт;
в) Протаргол;
г) Олеум .
1.1.107. Оксид нітрогену (I), відомий під назвою „звеселяючий газ”, у суміші з киснем використовують у медицині для наркозу. Вкажіть формулу цього оксиду.
а) N2O; б) NO;
в) NO2 ; г) N2O3.
1. 2. БІОГЕННІ d-ЕЛЕМЕНТИ
1.2.1.Ступінь окиснення d-елемента у сполуці K2Cr2O7:
а) +1; б) +2; в) +3; г) +4;
д) +5; з) +6; ж) +7.
1.2.2. Ступінь окиснення d-елемента у сполуці Na2CrO4:
а) +1; б) +2; в) +3; г) +4;
д) +5; з) +6; ж) +7.
1.2.3. Ступінь окиснення d-елемента у сполуціCr2(SO4)3:
а) +1; б) +2; в) +3; г) +4;
д) +5; з) +6; ж) +7.
1.2.4. Ступінь окиснення d-елемента у сполуці KMnO4:
а) +1; б) +2; в) +3; г) +4;
д) +5; з) +6; ж) +7.
1.2.5. Ступінь окиснення d-елемента у сполуці K2[Zn(OH)4]:
а) +1; б) +2; в) +3; г) +4;
д) +5; з) +6; ж) +7.
1.2.6. Ступінь окиснення d-елемента у сполуці AgNO3:
а) +1; б) +2; в) +3; г) +4;
д) +5; з) +6; ж) +7.
1.2.7. Якому d-елементу відповідає електронна конфігурація 3s23p63d24s2
а) Zn; б) Fe; в) Ag; г) Ті.
1.2.8. Якому d-елементу відповідає електронна конфігурація 3s23p63d54s1
а) Zn; б) Fe; в) Ag; г) Cr.
1.2.9. Якому d-елементу відповідає електронна конфігурація 3s23p63d64s2
а) Zn; б) Fe; в) Ag; г) Cu
1.2.10. Якому d-елементу відповідає електронна конфігурація 3s23p63d74s2
а) Zn; б) Fe; в) Ag; г) Co.
1.2.11. Якому d-елементу відповідає електронна конфігурація 3s23p63d104s2
а) Zn; б) Fe; в) Ag; г) Cu.
1.2.12. Якому d-елементу відповідає електронна конфігурація 4s24p64d105s1
а) Zn; б) Fe; в) Ag; г) Cu.
1.2.13. Які властивості проявляють оксид і гідрат оксиду Ті у ступені окиснення +2:
а) кислотні; б) основні;
в) амфотерні; г) несолетворні.
1.2.14. Які властивості проявляють оксид і гідрат оксиду Fe у ступені окиснення +2:
а) кислотні; б) основні;
в) амфотерні; г) несолетворні.
1.2.15. Які властивості проявляють оксид і гідрат оксиду Fe у ступені окиснення +3:
а) кислотні; б) основні;
в) амфотерні; г) несолетворні.
1.2.16. Які властивості проявляють оксид і гідрат оксиду Cr у ступені окиснення +3:
а) кислотні; б) основні;
в) амфотерні; г) несолетворні.
1.2.17. Які властивості проявляють оксид і гідрат оксиду V у ступені окиснення +5:
а) кислотні; б) основні;
в) амфотерні; г) несолетворні.
1.2.18. Які властивості проявляють оксид і гідрат оксиду Mn у ступені окиснення +7:
а) кислотні; б) основні;
в) амфотерні; г) несолетворні.
1.2.19. Який із наведених нижче йонів виявляє тільки властивості окисника:
а) Mn+7; б) Mn+2 в) Mn+3; г) Mn+4.
1.2.20. Який із наведених нижче йонів виявляє тільки властивості окисника:
а) Cr+6; б) Cr +2 в) Cr +3; г) Cr0.
1.2.21. Який із наведених нижче йонів виявляє тільки властивості окисника:
а) V+5; б) V +2 в) V+4; г) V+3.
1.2.22. Який із наведених нижче йонів виявляє тільки властивості відновника:
а) S-2; б) S 0 в) S +4; г) S+6.
1.2.23. Який із наведених нижче йонів виявляє тільки властивості відновника:
а) N-3; б) N 0 в) N +5; г) N+3.
1.2.24. Який із наведених нижче йонів виявляє властивості як окисника так і відновника:
а) Mn+4; б) Mn+7 в) Mn0; ) Mn+2.
1.2.25. Який із наведених нижче йонів виявляє властивості як окисника так і відновника:
а) Cr+3; б) Cr 0 в) Cr +6; г) Cr+2.
1.2.26. Скільки електронів приймає d елемент при відновленні в даній окисно-відновній реакції:
KMnO4 + Na2SO3 + H2SO4 → MnSO4 +
а) 1; б) 2; в) 3; г) 5
1.2.27. Скільки електронів приймає d елемент при відновленні в даній окисно-відновній реакції:
KMnO4 + Na2SO3 + KOH → K2MnO4 +
а) 1; б) 2; в) 3; г) 5
1.2.28. Скільки електронів приймає d елемент при відновленні в даній окисно-відновній реакції:
KMnO4 + Na2SO3 + H2O → MnO2 +
а) 1; б) 2; в) 3; г) 5
1.2.29. Скільки електронів приймає d елемент при відновленні в даній окисно-відновній реакції:
FeSO4 + KMnO4 + + H2SO4 → Fe2(SO4)3+
а) 1; б) 2; в) 3; г) 5
1.2.30. Скільки електронів приймає d елемент при відновленні в даній окисно-відновній реакції:
KMnO4 + HCl → MnCl2+
а) 1; б) 2; в) 3; г) 5
1.2.31. Скільки електронів приймає d елемент при відновленні в даній окисно-відновній реакції:
K2Cr2O7 + K2SO3 + HCl → CrCl3 +
а) 1; б) 2; в) 3; г) 5
1.2.32. Який d-елемент входить в склад вітаміну В12?
а) Fe; б) Co; в) Mn; г) V.
1.2.33. Який з d-елементів входить до складу гемоглобіну і деяких ферментів, а також до складу м’язового білка міоглобіну:
а) Fe; б) Co; в) Mn; г) V.
1.2.34. Який d-елемент може інактивувати певні ділянки молекул ферментів, виступаючи ферментативною отрутою:
а) Fe; б) Co; в) Ag; г) Ti.
1.2.35. Який d-елемент проявляє ліпотропний ефект, знижуючи відкладення жиру в організмі:
а) Fe; б) Co; в) Mn; г) V
1.2.36. Який d-елемент впливає на діяльність залоз внутрішньої секреції, ріст і розвиток організму. Добова потреба збільшується в період росту, статевого дозрівання і під час вагітності:
а) Fe; б) Co; в) Zn; г) V.
1.2.37. Сполуки якого d-елемента є особливо токсичнимидля організму людини:
а) Cu б) Cd в) Ti г) Fe
1.2.38. Сполуки якого d-елемента є особливо токсичними для організму людини:
а) Cu; б) Tl; в) Ti; г) Fe.
1.2.39. Основна біологічна роль мікроелемента Mn ґрунтується на властивостях:
а) окисно-відновних; б) кислотно-відновних;
в) комплексотвірних; г) буферних.
1.2.40. Основна біологічна роль мікроелемента Cr ґрунтується на властивостях:
а) окисно-відновних;
б) кислотно-відновних;
в) комплексотвірних; г) буферних.
1.2.41. При виготовленні ліків, що містять КІ, необхідно враховуючи його окисно-відновні властивості. З якою із перелічених сполук КІ несумісний:
а) KCl; б) KI; в) H2O2; г) FeSO4.
1.2.42. Застосування гідроген пероксиду в медицині грунтується на окисних властивостях H2O2, які проявляються в реакції з:
а) KI; б) KMnO4; в) K2Cr2O7; г) H2O.
1.2.43. Які хімічні властивості зумовлюють використання в медицині як антисептика KMnO4:
а) здатність до повної дисоціації на іони; б) окисні властивості; в) відновні властивості;
г) відсутність гідролізу.
1.2.44. Якою зміною ступеня окиснення феруму супроводжується перенос електрона цитохромомС в організмі людини:
а) Fe0 → Fe+2; б) Fe+2 → Fe+3; в) Fe0 → Fe+3; г) Fe+2 → Fe+6.
1.2.45.Одним з шляхів видалення гідрогенпероксиду з організму є реакція
2Н2О2 = 2Н2О + О2.
До якого типу реакцій вона належить:
а) міжмолекулярного окиснення-відновлення;
б) внутрішньомолекулярного окиснення-відновлення;
в) диспропорціонування; г) нейтралізації.
1.2.46. Нітрит-йон проявляє токсичну дію, яку можна представити схемою:
HbFe+2 + NO-2 + 2H+ → HbFe+3 + NO + 2H2O
в якій NO-2 виконує роль:
а) окисника; б) відновника;
в) середовища; г) інгібітора.
1.2.47. Ферметативний процес окиснення аміаку в організмі відбувається за рівнянням:
2NН3 + 3О2 → 2Н+ + 2Н2О + 2NО
Скільки електронів віддає відновник в цій реакції:
а) 4; б) 6; в) 3; г) 8.
1.2.48. Нітрит-іон продуктується в організмі людини в кількості 400 мл за добу. Реагуючи з катіоном Fe+2 гемоглобіну він перетворюється в оксид нітрогену (ІІ), який розширює стінки судин. Скільки електронів приєднує нітрат-іон:
а) 1; б) 3; в) 4; г) 2.
1.2.49. Найважливішою функцією цього d-елементу вважють здатність прискорювати розпад пуринів і виводити з організму сечову кислоту, що при сприяє профілактиці розвитку подагри:
а) Молібден; б) Ферум;
в) Аурум; г) Тітан.
1.2.50. d-елемент необхідний для активності ряду ферментів, які беруть участь у тканинному диханні та синтезі аскорбінової кислоти, що сприяє нормальному росту і розвитку організму в цілому:
а) Молібден; б) Ферум;
в) Аурум; г) Тітан.
1.2.51. Дія мікроелементу молібдену на людський організм:
а) покращує ріст ;
б) Входить до складу інсуліну;
в) Зменшує набряки;
г) Входить до складу шлункового соку.
1.2.52. Який мікроелемент входить до складу ферменту, який відповідає за засвоєння та утилізацію заліза, у зв'язку з чим запобігає анемії?
а) молібден; б) Кадмій
в) Скандій; г) Літій.
1.2.53. Цей мікроелемент бере участь у регуляції жирового і вуглеводного обміну, утворенні кісткової і сполучної тканини, в обміні тироксину (гормону щитовидної залози):
а) Марганець; б) Меркурій
в) Ферум; г) Аурум
1.2.54. Необхідний для росту, відтворення, загоєння ран, максимально ефективної роботи мозку і правильного метаболізму цукру, інсуліну і холестерину. бере участь у регуляції обміну вітамінів С, Е, холіну і вітамінів групи В.
а) Марганець; б) Меркурій;
в) Ферум; г) Аурум
1.2.55. Нормалізує вуглеводний обмін, активно впливає на метаболізм інсуліну, що важливо для профілактики розвитку цукрового діабету.
а) марганець ; б) Меркурій;
вВ) Ферум; г) Аурум
1.2.56. Нормалізує роботу щитовидної залози - бере участь в обміні тироксину (гормону щитовидної залози) і, є ефективний для профілактики захворювань щитовидної залози, цукрового діабету, порушень жирового обміну, остеопорозу, хвороб суглобів.
а) марганець ; б) Меркурій;
в) Ферум; г) Аурум
1.2.57. Разом з інсуліном бере участь у метаболізмі цукру.
а) Хром; б) Кобальт;
в) Ферум; г) Сульфур.
1.2.58. Мікроелемент хром необхідний:
а) хворим на цукровий діабет (насамперед II типу);
б) Для лікування алкоголізму;
в) Для лікування «курячої сліпоти»;
г) Хворим з виразкою шлунку.
1.2.59. Мікроелемент, що сприяє зростанню і регенерації тканин і бере участь у синтезі нуклеїнових кислот - входить в структуру ДНК і РНК:
а) Хром; б) Кобальт;
в) Ферум; г) Сульфур.
1.2.60. Регулює роботу щитовидної залози , при нестачі йоду і певних умовах, здатний заміщати йод в тиреоїднихгормонах.
а) Хром; б) Кобальт;
в) Ферум; г) Сульфур.
1.2.61. Регулює ліпідний обмін - знижує рівень "поганого" холестерину в крові, запобігає розвитку атеросклерозу і серцево-судинних захворювань.
а) Хром; б) Кобальт;
в) Ферум; г) Сульфур.
1.2.62. Сприяє нормалізації ваги - нормалізуючи вуглеводний обмін, сприяє переробці жиру і запобігає його відкладення в м'язовій масі:
а) Хром; б) Кобальт;
в) Ферум; г) Сульфур
1.2.63. Достатній вміст в мозку підтримує його судини в хорошому стані і перешкоджає розвитку склерозу, запобігає ризику серцево-судинних захворювань, гіпертонії;
а) Ванадій; б) Натрій;
в) Калій; г) Хлор
1.2.64. Мікроелемент Ванадій використовують для:
а) нормалізації вуглеводного обміну (зокрема при лікуванні цукрового діабету)
б) Лікування безпліддя
в) Лікування неврозів
г) лікування виразки шлунку.
1.2.65. Препарати цього мікроелементу мають протипухлинну дію - стимулють правильний поділ клітин організму:
а) Ванадій; б) Натрій
в) Калій; г) Хлор
1.2.66. Цей мікроелемент бере участь у регуляції водно-сольового балансу (підтримка балансу натрію і калію в організмі), що дозволяє підтримувати нормальний артеріальний тиск, знижувати набряки, регулювати роботу м'язової та нервової тканин:
а) Ванадій; б) Натрій
в) Калій; г) Хлор.
1.2.67. Мікроелемент бере участь у регуляції процесів кровотворення і впливає на рівень гемоглобіну в крові - засвоюється організмом за допомогою молекул-переносників, подібних до тих, які транспортують залізо:
а) Ванадій; б) Натрій;
в) Калій; г) Хлор.
1.2.68. Цей мікроелемент бере участь у формуванні кісткового скелета - сприяє накопиченню солей кальцію в кістках, бере участь у формуванні зубів, підвищує їх стійкість до карієсу.
а) Ванадій; б) Натрій
в) Калій; г) Хлор
1.2.69. Залізо є одним з незамінних мікроелементів. Яку важливу дію в органзмі він виконує?
а) бере участь у тканинному диханні ;
б) Є ферментативною отрутою
в) Впливає на водний баланс організму
г) Нормалізує ліпідний обмін.
1.2.70. Основна дія Цинку в організмі людини:
а) імуностимулююча
б) транспорт Кисню
в) Синтез тироксину
г) Зниження збудливості і депресивних станів.
1.2.71. Цей мікроелемент при взаємодії з марганцем підвищує вироблення статевих гормонів, збільшує активність сперматозоїдів, сприяє правильному функціонуванню та розвитку чоловічих статевих залоз:
а) Цинк; б) Кадмій;
в) Молібден; г) Аурум
1.2.72. є важливою речовиною для підтримки та поліпшення зору, особливо багато цинку міститься в сітківці ока, тому він важливий для профілактики короткозорості, підвищує здатність адаптації до темряви (при лікуванні «курячої сліпоти»):
а). Цинк; б) Кадмій;
в) Молібден; г) Аурум
1.2.73. Він регулює рівновагу цукру в крові, тому що є одним з компонентів інсуліну.
а) Цинк; б) Кадмій;
в) Молібден; г) Аурум
1.2.74. Різка затримку росту (карликовість) виникає при недостачі мікроелементту:
а) Цинк; б) Кадмій;
в) Молібден; г) Аурум
1.2.75. Різні розлади статевої функції, що призводять до бездітності (головним чином, через атрофію статевих залоз у чоловіків, недорозвиненості статевих органів); простатит і аденома передміхурової залози; передчасні пологи і народження ослаблених, маленьких дітей виникає при недостачі мікроелементту:
а) Цинк; б) Кадмій;
в) Молібден; г) Аурум.
1.2.76. Ураження головного мозку: психічні розлади (апатія, депресія, сплутаність свідомості, посилення симптомів шизофренії, епілепсії), неврологічні порушення (втрата смакових відчуттів, порушення слуху та зору) виникає при недостачі мікроелементту:
а) Цинк; б) Кадмій
в) Молібден; г) Аурум
1.2.77. Сульфат міді (II) використовують як антисептичний та в’яжучий засіб в офтальмології, гінекології, урології, а також як протиотруту при отруєнні білим фосфором. При взаємодії з надлишком водного розчину аміаку CuSO4 утворює сполуку, яка містить іон:
а) [Cu(NH3)4]2+ ; б) CuOH+
в) [Cu(NH3)2] + ; г) [Cu(OH)NH3] +
1.2.78. Нітрат срібла застосовують в офтальмології як бактерицидний, протизапальний засіб. Вказати реагент, який може служити для ідентифікації Ag+:
а) NaCl ; б) KNO3
в) Ва(NO3)2 г) (NH4)2СO3
1.2.79. Сульфат заліза (II) входить як складова частина до засобів, які застосовують при лікуванні залізодефіцитних анемій. З якою з наведених сполук реагує FeSO4:
а) KMnO4; б) HCl
в) CO2; г) FeCl2
1.2.80. Що являє собою перетворення Cr+3 > CrO42-
а) окислення в лужному середовищі
б) окислення в кислому середовищі
в) відновлення в кислому середовищі
г) відновлення в нейтральному середовищі
1.2.81. Що являє собою перетворення MnO4- > MnO2
а) відновлення в нейтральному середовищі
б) окислення в кислому середовищі
в) відновлення в кислому середовищі
г) окислення в лужному середовищі
1.2.82. Зміна кислотно-лужних властивостей в сполуках MnO > MnO2 > Mn2O7 відповідає закономірності
а) кислотні властивості підсилюються
б) основні властивості підсилюються
в) кислотно-лужні властивості не змінюються
г) кислотні властивості зменшуються
1.2.83. Ферум (ІІІ) гідроксид проявляє амфотерні властивості тому що:
а) реагує з кислотами і основами
б) реагує тільки з кислотами
в) реагує тільки з основами
г) диспропорціонує
1.2.84. Серед елементів ІІВ групи амфотерні властивості проявляють:
а) тільки цинк; б) цинк і кадмій;
в) кадмій і ртуть г) тільки ртуть
1.2.85. Калій перманганат в реакції з гідроген пероксидом у кислому середовищі проявляє властивості:
а) окисника;
б) відновника;
в) диспропорціонує;
г) окисника та відновника;
1.2.86. Купруму сульфат застосовують як:
а) Антисептичний засіб
б) Антацидний засіб
в) Проносний засіб
г)Заспокійливий засіб
1.2.87. Сполуки Au використовують для лікування:
а) туберкульозу; б) Гастриту
в) Безпліддя; г) Анемії
1.2.88. Меркурію хлорид (сулема) використовується як:
а) Антисептичний засіб
б) Антацидний засіб
в) Проносний засіб
г) Заспокійливий засіб
1.2.89. При відновленні калій перманганату у нейтральному середовищі утворюється сполука мангану:
а) MnO2 ; б) К2MnO4;
в) MnO; г) MnSO4
1.2.90. Ферум у сполуках може знаходитись у різних ступенях окиснення. Який найвищий ступінь окиснення феруму у сполуках:
а) +6; б) +8; в) +3; г) +4
1.2.91. Механізм токсичної дії сполук Плюмбуму полягає у:
а) зв’язуванні SH - груп ферментних систем;
б) утворенні метгемоглобіну у крові;
в) зменшенні величини рН крові;
г) збільшенні величини осмотичного тиску крові.
1.2.92. Марганець відноситься до біометалів, концентрується в печінці, відповідає за функцію утворення піровиноградної кислоти. Яка сполука марганцю є найсильнішим окисником?
а) КMnO4 ; б) MnO2;
в) MnO; г) Mn2O3.
1.2.93. Хром відноситься до мікроелементів, бере участь в процесах обміну глюкози. Вкажіть, якій закономірності відповідає зміна кислотно-основних властивостей в ряді сполук CrO - Cr2O3 - CrO3?
а) Кислотні властивості підсилюються
б) Основні властивості підсилюються
в) Кислотно-основні властивості не змінюються
г) Кислотні властивості зменшуються
1.2.94. За один день організм людини потребує 5-10мг хрому, він приймає участь в стабілізації структури нуклеїнових кислот, входить до складу ферменту трипсину. Вказати йон, яка є якісним реагентом на хромати:
а) Ag+; б) К+; в) Na+; г) Ca2+.
1.2.95. Цинк належить до групи незамінних мікроелементів. Знаходиться в печінці, молочних залозах, сітчастій оболонці ока. Вибрати сполуку цинку, яку використовують в дерматології, в основі «цинкової мазі» для загоєння ран:
а) ZnO; б) Zn(OH)2 ;
в) Zn(NO3)2; г) ZnCl2.
1.2.96. Цинк належіть до мікроелементів, а розчин цинк сульфату ZnSO 4 використовують у медицині як очні краплі. Вкажіть до якого типу солей відноситься ця сполука:
а) Середні; б) Кислі;
в) Основні; г) Комплексні.
1.2.97. Вкажіть, в якому ступені окиснення Манган та Хлор виявляє найбільшу схожість у властивостях :
а) +7; б) +3;
в) 0; г) +4
1.2.98. Аргентум нітрат застосовують в офтальмології як бактерицидний, протизапальний засіб. З яким із йонів AgNO3 утворює білий сирнистий осад?
а) Cl-; б) NO3-; в) SO42-; г)NO2-
1.2.99. Ферум в організмі людини входить до складу гемоглобіну та ряду ферментів. Недостача заліза в організмі викликає:
а) анемію; б) Остеопороз;
в) Карієс; г) Флюороз.
КОМПЛЕКСНІ СПОЛУКИ
1.3.1. Для комплексної сполуки [Ag(NH3)2]OH йон Ag+ є:
а) комплексоутворювачем;
б) лігандом;
в) зовнішньою сферою;
г) внутрішньою сферою.
1.3.2. Для комплексної сполуки [Ag(NH3)2]OH група частинка NH3+ є:
а) комплексоутворювачем;
б) лігандом;
в) зовнішньою сферою;
г) внутрішньою сферою.
1.3.3. Для комплексної сполуки [Ag(NH3)2]OH група OH- є:
а) комплексоутворювачем;
б) лігандом;
в) зовнішньою сферою;
г) внутрішньою сферою.
1.3.4. Для комплексної сполуки [Ag(NH3)2]OH йон [Ag(NH3)2]+ є:
а) комплексоутворювачем;
б) лігандом;
в) зовнішньою сферою;
г) внутрішньою сферою.
1.3.5. Для комплексної сполуки Fe4[Fe(CN)6]3 йон Fe+3 є:
а) комплексоутворювачем;
б) лігандом;
в) зовнішньою сферою;
г) внутрішньою сферою.
1.3.6. Для комплексної сполуки Fe4[Fe(CN)6]3 йон Fe+2 є:
а) комплексоутворювачем;
б) лігандом;
в) зовнішньою сферою;
г) внутрішньою сферою.
1.3.7. Для комплексної сполуки Fe4[Fe(CN)6]3 група CN- є:
а) комплексоутворювачем;
б) лігандом;
в) зовнішньою сферою;
г) внутрішньою сферою.
1.3.8. Для комплексної сполуки Fe4[Fe(CN)6]3 йон [Fe(CN)64-] є:
а) комплексоутворювачем;
б) лігандом;
в) зовнішньою сферою;
г) внутрішньою сферою.
1.3.9. Для комплексної сполуки [Cu(NH3)4](OH)2 йон Cu2+ є:
а) комплексоутворювачем;
б) лігандом;
в) зовнішньою сферою;
г) внутрішньою сферою.
1.3.10. Для комплексної сполуки [Cu(NH3)4](OH)2 молекула NH3 є:
а) комплексоутворювачем;
б) лігандом;
в) зовнішньою сферою;
г) внутрішньою сферою.
1.3.11. Комплексоутворювач повинен бути:
а) акцептором електронів, мати вільні електронні орбіталі;
б) нейтральною частинкою;
в) оксигеновмісним,
г) донором електронних пар.
1.3.12. Лігандповинен бути:
а) акцептором електронів, мати вільні електронні орбіталі;
б) нейтральною частинкою;
в) оксигеновмісним,
г) донором електронних пар.
1.3.13. Характерним типом зв’язку між комплексоутворювачем і лігандами є зв’язок:
а) ковалентний; б) йонний;
в) донорно-акцепторний г) водневий.
1.3.14. В якій із комплексних сполук комплексоутворювачем є Fe2+:
а) K4[Fe(CN)6]; б) K3[Fe(CN)6];
в) Fe(OH)2Cl г) Fe2(SO4)3
1.3.15. В якій із комплексних сполук
комплексоутворювачем є Fe3+:
а) K4[Fe(CN)6]; б) K3[Fe(CN)6];
в) Fe(OH)2Cl г) Fe2(SO4)3
1.3.16. Який з перелічених катіонів можуть бути комплексоутворювачем?
а) K+; б) Na+ в) Co2+ г) NH4+
1.3.17. Яка з частинок може стати комплексоутворювачем?
а) OH-; б) Cu2+; в) СN-; г) Н2О;
1.3.18. Яка з частинок може стати комплексоутворювачем?
а) Fe2+; б) Cl-; в) OH-; г) Br-;
1.3.19. Яка з частинок може стати комплексоутворювачем?
а) Co3+; б) OH-; в) СN-; г) SCN;
1.3.20. Яка з частинок може стати комплексоутворювачем?
а) Al3+; б) H2O; в) SО42-; г) OH-;
1.3.21.. Яка з частинок може стати лігандом?
а) Cu2+; б) Cu+; в) Ag+; г) OH-;
1.3.22. Яка з частинок може стати лігандом:
а) Fe2+; б) Cl-; в) Fe3+; г) Zn2+;
1.3.23.Яка з частинок може стати лігандом:
а) NН3; б) Mg2+; в) Cu2+; г) Cr3+;
1.3.24. Яка з частинок може стати лігандом:
а) H2O; б) Zn2+; в) Al3+; г) Sn2+;
1.3.25. В якій із наведених сполук H2O є лігандом:
а)CuSO4*5H2O; б) K[Al(OH)4(H2O)2];
в) [Zn(NH3)2](OH)4 г)FeSO4•7H2O;
1.3.26. В якій із наведених сполук ціанід-йон є лігандом:
а) Zn(СN)2; б) K2[PtCl4];
в)K2[Au(CN)4]; г) Fe(CN)3
1.3.27. В якій із наведених сполук хлорид-йон є тільки лігандом:
а) ZnCl2; б) K2[PtCl4];
в) [Ag(NH3)2]Cl; г) [PtCl2]Cl2;
1.3.28. Яка із перелічених частинок може грати роль ацидного ліганда:
а) Cl-; б) NH3; в) СО; г) NH4+;
1.3.29. Яка із перелічених частинок може грати роль нейтрального ліганда:
а) Cl-; б) NH3; в) СN; г) OH-;
1.3.30. Яка із перелічених частинок може грати роль акваліганда:
а) Cl-; б) NH3; в) СО; г) Н2О;
1.3.31. При дії надлишку розчину гідроксиду амонію на катіон Cu2+ утворюються:
а) гідроксиди цих металів;
б) основні солі цих металів;
в) аквакомплекси;
г) аміакaтні комплекси цих сполук.
1.3.32. При дії надлишку розчину гідроксиду амонію на катіон Cо2+ утворюються:
а) гідроксиди цих металів;
б) основні солі цих металів;
в) аквакомплекси;
г) аміакaтні комплекси цих сполук.
1.3.33. При дії надлишку розчину гідроксиду амонію на катіон Zn2+ утворюються:
а) гідроксиди цих металів;
б) основні солі цих металів;
в) аквакомплекси;
г) аміакaтні комплекси цих сполук.
1.3.34. Ціанкобаламін (вітамін В12) є комплексною сполукою кобальту. До якого типу комплексних сполук він належить?
а) катіонних комплексів; б) аквакомплексів;
в) ціанідних комплексів;
г) хелатних комплексів.
1.3.35. Хлорофіл є комплексною сполукою магнію. До якого типу комплексних сполук він належить?
а) катіонних комплексів; б) аквакомплексів;
в) ціанідних комплексів;
г) хелатних комплексів.
1.3.36. Гемоглобін є комплексною сполукою заліза. До якого типу комплексних сполук він належить?
а) катіонних комплексів; б) аквакомплексів;
в) ціанідних комплексів;
г) хелатних комплексів.
1.3.37. Амінокислоти можуть утворювати комплекси з йонами кобальту. До якого типу комплексних сполук він належить?
а) катіонних комплексів; б) аквакомплексів;
в) ціанідних комплексів;
г) хелатних комплексів.
1.3.38. Комплексна сполука, що сприяє участі рослин у фотосинтезі називається:
а) гемоглобін; б) ціанкобаламін;
в) трилон Б; г)хлорофіл.
1.3.39. Які із наведених речовин грають роль комплексону в хелатотерапії?
а)трилон Б; б) амінооцтова кислота ;
в)сода г)аміак.
1.3.40 Для наведеної комплексної сполуки K2[HgI4] вказати комплексоутворювач:
а) Hg2+ ; б) K+;
в) I– ; г) HgI42–
1.3.41. Вкажіть тип реакції, що застосовують для якісного визначення катіону Fe3+:
а) комплексоутворення;
б) осаждення
в) гідролізу
г) окиснення-відновлення
1.3.42. Реалізація якого типу хімічного зв’язку обов’язкова в комплексних сполуках?
а) Донорно-акцепторного ;
б) Йонного ;
в) Ковалентного;
г) Водневого .
1.3.43. Яка координаційна формула сполуки з сумарним складом PtCl4•6NH3, якщо координаційне число Pt (IV) дорівнює 6?
а) [Pt(NH3)6]Cl4 ;
б) [Pt(NH3)6]Cl2
в) [Pt(NH3)4]Cl4
г) [Pt(NH3)6]Cl3
1.3.44. Яка з наведених комплексних сполук є катіонним комплексом:
а) [Cr(H2O)4Cl2]Cl ; б) H2[PtCl6]
в) Na3[Co(NO2)6] ; г) K3[Fe(CN)6]
1.3.45. Ртуть здатна утворювати сполуки, в яких проявляє ступінь окислення +1 або +2. В якій з наведених формул сполук, ртуть проявляє ступінь окислення +2
а) K2[HgI4]; б) Hg2Cl2
в) Hg2O; г) Hg2(NO3)2•2H2O
1.3.46. Визначити комплексну сполуку, заряд центрального атома-комплексоутворювача якої дорівнює +3
а) K3[Fe[CN]6]; б) [Pt[NH3]2Cl2]
в) K2[Mn[CN]4] ; г) K2[PtCl4]
1.3.47. Який вид ізомерії має місце для комплексної сполуки [Pt[NH3]2Cl2]
а) геометрична; б) оптична
в) гідратна; г) іонізаційна
1.3.48. Присутність якого з іонів d-елементів у розчинах можна встановити за допомогою K4[Fe[CN]6]
а) Fe3+; б) Fe2+;
в) Zn2+; г) Cr3+
1.3.49. Вказати комплексну сполуку, в якій комплексоутворювачем є Pt(IV):
а) [Pt(NH3)4Cl2] Cl2 ;
б) K2[PtCl4];
в) Ba [Pt(CN)4];
г) [Pt(NH3)4](NO3)2;
[Pt(NH3)2Cl2];
1.3.50. Купрум (ІІ) гідроксид утворює з лугами комплексні сполуки, в яких купрум проявляє координаційне число:
а) 4; б) 5; в) 6; г) 3
1.3.51. Жовта кров’яна сіль K 4[Fe(CN) 6] є реактивом на:
а) іони Fe3+ ; б) іони Fe2+ ;
в) іони Ca2+; г) іони FeO42-.
1.3.52. Гем (складова частина гемоглобіну) є комплексною сполукою Феруму. До якого типу комплексних сполук він належить?
а) Хелатних комплексів
б) Ацідокомплексів
в) Аквакомплексів
г) Катіонних комплексів
1.3.52. Дихлордіамінплатину використовують у медицині як протипухлинний засіб. Серед наведених сполук вкажіть цей лікарський препарат:
а) [Pt(NH3)2Cl2]
б [Pt(NH3)4]Cl2
в) [Pt(NH3)3Cl]Cl
г) [Pt(NH3)4](NO3)2
1.3.53. Комплексна сполука [Pt(NH3)2Cl2] утворює цис- і транс-форми. Назвіть вид ізомерїї:
а) геометрична; б) іонізаціонна;
в) гідратна; г) координаційна
1.3.54. Деякі лікарські засоби відносять до комплексних сполук. Укажіть який з лігандів є бідентатним.
а) Оксалат-іон; б) Гідроксид-іон;
в) Аміак; г) Хлорид-іон.
1.3.55. Який ступінь окиснення має центральний іон у сполуці Н2[PtCl6]?
а) +4; б) 0; в) +2; г) +3.
РОЗЧИНИ
1.4.1. Розчин, в якому речовина при певній температурі більше не розчиняється, називають:
а) насичений; б) ненасичений;
в) розведений; г) пересичений.
1.4.2. В шлунковому соці людини розчиненою речовиною є:
а) соляна кислота; б) натрій гідроксид;
в) вода; г) сірчана кислота.
1.4.3. Щоб збільшити розчинність газу, треба:
а) понизить температуру;
б) підвищити температуру;
в) підвищити тиск; г) понизить тиск.
1.4.4. При збільшенні температури,розчинність речовини:
а) зменшується; б) збільшується;
в) не змінюється;
г) спочатку збільшується, а потім зменшується.
1.4.5. Тиск впливає на розчинність речовини:
а) рідкої; б) твердої;
в) газоподібної; г) нерозчинної.
1.4.6. Вибрати фактор, який збільшує розчинність твердих речовин:
а) пониження температури;
б) підвищення температури;
в) підвищення тиску; г) пониження тиску.
1.4.7. Хлорид натрію розчиняється у воді і не розчиняється в бензолі. Це пояснюється:
а) різною природою хімічного зв’язку у молекулах води і бензолу;
б) різною густиною води і бензолу;
в) різними ступенями окиснення атомів гідрогену у воді і у бензолі;
г) різними молярними масами у води і бензолу.
1.4.8. Вибрати формулу для знаходження масової концентраціїрозчину:
а) Cm = 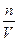 ; б)
; б) 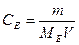 ;
;
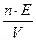 г) ω =
г) ω =