 |
|
Так получают очень чистые Ме
▲ Задача
Рассмотрите процесс рафинирования Ni, содержащего примеси Zn и Cu в растворе H2SO4. Какие процессы будут протекать на катоде и аноде? Какое время нужно для проведения рафинирования при токе 500 А для выделения 5 кг никеля при выходе по току 98%?
Решение.
Ионный состав раствора:
H2SO4 → H+ + SO42-
H2O ↔ H+ + OH- рН=2
Запишем потенциалы возможных электродных процессов
ЕрО2/ОН- =1,23-0,059рН = +1,112В;
ЕрН+/Н2 = -0,059рН = -0,118В
Е0Ni2+/Ni = - 0,250В
Е0Zn2+/Zn = -0,76В;
Е0Сu2+/Cu = + 0,337В
Т.к. Е0Zn2+/Zn < Е0Ni2+/Ni < Е0Cu2+/Cu < EpO2/OH- то первым на аноде окисляется Zn, затем очищаемый Ме – Ni, примеси Cu не растворяются, а выпадают в осадок (шлам).
Т.к. Е0Ni2+/Ni > Е0Zn2+/Znи потенциал ионов Ni2+ ↑, чем ионов Zn2+, то на катоде осаждается чистый никель.
В начале процесса в растворе отсутствуют ионы Ni2+ и на катоде выделяется Н2.
Þ [+A]: Zn0 → Zn2+ + 2е
Ni0 → Ni2+ + 2е
[- K]: 2Н+ + 2е → Н2↑
Ni2+ + 2е → Ni0
Время для рафинирования по закону Фарадея (Мэ,Ni=29,5 г/моль):
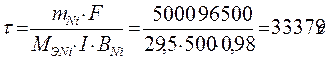 или τ =9,27 ч
или τ =9,27 ч

РЕШЕНИЕ ЗАДАЧ
▲ Задача
Определите объем Cl2, выделившийся при электролизе водного раствора NaCl на платиновых электродах, если объем выделившегося при этом Н2 - 44,8 мл. Выход по току хлора – 80%.
Решение. Ионный состав раствора:
NaCl → Na+ + 2l-
H2O ↔ H+ + OH-
рН=7 гидролизa соли
Потенциалы возможных процессов:
ЕрН+/Н2 = -0,059рН = -0,41В
ЕрО2/ОН- =1,23-0,059рН = +0,81В;
Е0Сl2/Cl- = + 1,36В
Е0Сl2/Cl- - ЕрО2/ОН- < 1 Þвозможны оба процесса
Электродные процессы:
[- K]: 2Н+ + 2е → Н2↑
[+A]: 4ОН- → О2 ↑ + 2Н2О + 4е
2Cl- → Cl2 + 2e
По закону Фарадея:


Количество электричества, прошедшее через электроды:
qk = qa =I·τ
 Þ
Þ 
Þ 
▲ Задача
Определить выход по току Fe, Co, Cd при электролизе раствора смеси их сернокислых солей (сульфатов), если массы выделившихся на катоде Ме соответственно mFe= 5,58 г; mCo=5,9 г; mCd=11,2 г.
Пример 1.3.Рассчитайте величину максимальной электроэнергии, которая может быть выработана серебряно – цинковым ГЭ при уменьшении массы анода на 1 г в результате протекания электрохимической реакции при условиях заданных в примере 1.2.
Решение. Анодом ГЭ является цинковый электрод. Количество электричества Q, прошедшего через электродную поверхность, рассчитывается из объединенного закона Фарадея:


Максимально вырабатываемая электроэнергия  или Wэл = 1,23 Вт ч.
или Wэл = 1,23 Вт ч.
Пример 1.5. Рассчитайте ЭДС концентрационного ГЭ:
H2,Pt | НCl || СН3СООН| H2,Pt , работающего при одинаковых давлениях 
и одинаковых концентрациях водных растворов кислот c0 = 0,1 моль/л.
Решение.Для кислой среды уравнения электродных реакций в концентрационном элементе:
А -: H2 → 2H+ + 2 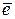
К+: 2H+ + 2 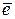 → H2
→ H2
Величина равновесного потенциала этих электродов определяется по уравнению
 , при
, при  .
.
Рассчитаем активность ионов водорода  :
:
а) в растворе уксусной кислоты: СН3СООН 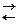 СН3СООН– + H+,
СН3СООН– + H+,
т.к. уксусная кислота является слабым электролитом, то коэффициент активности  и
и  ≈
≈  ; константа диссоциации Кд = 1,75 10-5
; константа диссоциации Кд = 1,75 10-5
 = αс0 , где степень диссоциации
= αс0 , где степень диссоциации  и тогда
и тогда


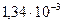 , следовательно
, следовательно  В.
В.
б) в растворе соляной кислоты: HCl → H+ + Cl–,
так как НСl является сильным электролитом, то сначала рассчитываем ионную силу раствора :
 ,
,
затем по таблице находим коэффициент активности  и тогда:
и тогда:
 и
и  В.
В.
Т.к.  , рассчитанный для соляной кислоты больше, чем для уксусной, то катодом будет электрод погруженный в раствор соляной кислоты, анодом - электрод погруженный в раствор уксусной кислоты.
, рассчитанный для соляной кислоты больше, чем для уксусной, то катодом будет электрод погруженный в раствор соляной кислоты, анодом - электрод погруженный в раствор уксусной кислоты.
 В.
В.