|
|
VII. Кинетически расчет
Кинетическими уравнениями обычно называют уравнения, выражающие зависимость скорости реакции от различных макроскопических параметров системы. Кинетические уравнения реакций, протекающих в изобарно-изотермических условиях, содержат лишь концентрации компонентов системы и некоторые константы – константы скорости и порядки реакции относительно отдельных компонентов системы.
Для элементарных реакций порядок обычно совпадает с молекулярностью. Молекулярность реакции равна числу молекул соответствующего исходного компонента, участвующему в элементарном акте химического взаимодействия.
Упорядоченная совокупность элементарных актов химической и физической природы некоторой химической реакции составляет механизм химической реакции, или кинетическую модель процесса. Исследование механизма химических реакций в существенной мере основано на детальном исследовании кинетики реакций.
Задание: Определить порядок реакции аналитическим и графическим методами, величину энергии активации графически-аналитическим методом и составить полное кинетическое уравнение.
Дано:

Таблица 15. Исходные данные

| 0,52 | 1,10 | 1,73 | 2,44 | 3,24 | 4,16 | 5,23 | 6,52 | 8,16 | |
| СА,0 | 0,1 | 0,091 | 0,083 | 0,075 | 0,067 | 0,059 | 0,051 | 0,043 | 0,035 | 0,027 |
Таблица 16. Исходные данные
| Температура, К | ||||
| Константа, с-1 | 3,17.10-2 | 6,73.10-2 | 0,132 | 0,243 |
Определении порядка реакции и энергии активации
7.1.1. Порядок реакции, определяемый аналитическим методом.





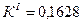






















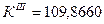

По полученным данным делаем вывод, что реакция первого порядка
7.1.2. Порядок реакции, определяемый графическим методом. Построим графическую зависимость С=f (  ):
):

Рис. 5. Зависимость концентрации от времени.
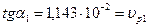


Построим график зависимости ln(  )=f(lnC)
)=f(lnC)
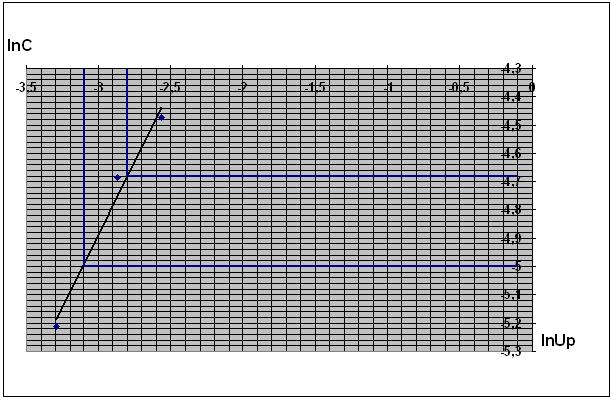
Рис. 6. Зависимость логарифма концентрации от логарифма скорости реакции.