 |
|
Порядок проведения эксперимента
Краткая теория
Рассмотрим обратимую реакцию
аА + bB « cC + Dd, (8)
где a, b, c, d – стехиометрические коэффициенты.
В определенных условиях скорость прямой реакции значительно превышает скорость обратной, и в целом процесс самопроизвольно протекает в прямом направлении. С изменением условий может превалировать скорость обратной реакции. В этом случае процесс изменит свое направление. Однако в каждых данных условиях направление процесса будет вполне определенным.
К условиям, которые могут влиять на направление химического процесса, относятся начальные концентрации реагирующих веществ, Т, Р.
При постоянных Т и Р скорости прямой и обратной реакции в результате изменения концентраций реагирующих веществ во времени постоянно выравниваются. Химическая реакция протекает в одном направлении до тех пор, пока не будет достигнуто химическое равновесие между реагирующими веществами. Химическое равновесие является динамическим процессом, при котором скорости прямой и обратной реакции равны друг другу. Состояние химического равновесия определяется двумя признаками:
1) если система находится в состоянии равновесия, то состав ее с течением времени при постоянных внешних условиях не меняется;
2) если система, находящаяся в равновесии, будет выведена из этого состояния вследствие внешних воздействий, то с прекращением их действий она возвратится в прежнее состояние.
При практическом определении равновесия химических реакций, протекающих сравнительно быстро, часто руководствуются только одним первым признаком.
Согласно основного постулата химической кинетики, скорость реакции прямо пропорциональна произведению концентраций реагирующих веществ в степенях, равных соответствующим стехиометрическим коэффициентам.
Для реакции (8)
Wпр = Кпр  , (9)
, (9)
Wобр = Кобр 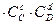 , (10)
, (10)
где Wпр – скорость прямой реакции; Wобр – скорость обратной реакции; Кпр и
К обр – константы скоростей прямой и обратной реакций; СА, СВ, СС, СD – концентрации реагентов.
При равновесии Wпр = Wобр или
Кпр  = Кобр
= Кобр 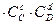 , (11)
, (11)
отсюда
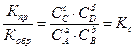 . (12)
. (12)
Основным количественным законом химического равновесия является закон действующих масс (12).
При химическом равновесии отношение произведений равновесных молярных концентраций продуктов реакции к произведению равновесных молярных концентраций исходных веществ есть постоянная величина для данной реакции при постоянной Т. Эта постоянная величина (Кс) называется константой равновесия.
Для расчета констант равновесия реакций, идущих в газовой среде, применяют равновесные парциальные давления реагентов. Для реакции (8) константа равновесия имеет вид:
Кр= 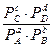 . (13)
. (13)
Константу равновесия можно выразить через равновесные мольные доли реагирующих веществ:
КN= 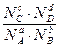 . (14)
. (14)
Согласно уравнению (14), КN является безразмерной величиной. Кс и Кр в соответствии с уравнениями (12) и (13) имеют размерность:
[Kc] = [моль/дм3]Dn и [Kp] = [Па]Dn,
где Dn = (с + d) – (а + b) – разность алгебраических сумм стехиометрических коэффициентов продуктов реакции и исходных веществ.
Константы равновесия Кр, Кс, КN взаимосвязаны следующими уравнениями:
Кр = Кс·(R·T)Dn, (15)
Кр = КN·(P)Dn, (16)
где R-универсальная газовая постоянная, [R = 8,314 Дж/(моль/К)]; Т - абсолютная температура, К; Р - давление в системе, Па.
При Dn = 0 все константы равновесия равны между собой.
Зависимость константы равновесия от температуры описывается уравнением Вант-Гоффа
dlnK/dT = q/(RT2), (17)
где q - тепловой эффект реакции.
Согласно уравнению (17) влияние температуры на константу равновесия обусловливается знаком теплового эффекта. Если q > 0 (реакция эндотермическая), то dlnK/dT > 0, с повышением температуры константа равновесия будет расти, и химическое равновесие будет смещаться в сторону образования продуктов реакции. При q < 0 (реакция экзотермическая) dlnK/dT < 0, константа равновесия будет уменьшаться с ростом температуры, и химическое равновесие будет смещаться в сторону образования исходных веществ.
По уравнению Вант – Гоффа по значениям констант равновесия при двух различных температурах можно вычислить тепловой эффект химической реакции. Если принять, что тепловой эффект химической реакции не зависит от Т, то после определенного интегрирования уравнения (17) от Т1 до Т2 и от К1 до К2, получим
ln 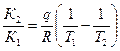 , (18)
, (18)
отсюда
q = 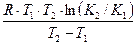 . (19)
. (19)
Цель работы: определение констант равновесия (при двух значениях температуры 200С и 400С) и вычисление теплового эффекта обратимой химической реакции:
2FeCl3 + 2KJ « 2FeCl2 + 2KCl + J2. (70)
В ионной форме уравнение имеет вид:
2Fe+3 + 2J- = 2Fe+2 + 2J20. (71)
О достижении равновесия судят по неизменности во времени концентрации йода в системе, которую определяют титрованием проб реакционной смеси раствором тиосульфата натрия в присутствии крахмала.
Порядок проведения эксперимента
В две сухие колбы наливают 50 мл 0,03М раствора FeCl3 и доливают до 100 мл 0,03М раствор KJ. Затем одну колбу оставляют при комнатной температуре (200С), а вторую помещают в термостат, в котором поддерживают температуру 400С.
Для титрования проб реакционной смеси в восемь конических колб на 100 мл наливают 50 мл дистиллированной воды и охлаждают. Через 20 минут после термостатирования из каждой колбы с реакционной смесью отбирают пипеткой 15 мл раствора и сливают в колбу с водой. Сразу после отбора пробы выделившейся йод титруют 0,015М раствором тиосульфата натрия до бледно-желтой окраски. Затем добавляют раствор крахмала и дотитровывают раствором тиосульфата натрия до исчезновения синего окрашивания раствора.
В последующем пробы отбирают с интервалом 30 минут из колбы термостатируемой при 200С, и с интервалом 20 минут из колбы термостатируемой при 400С.
Экспериментальные данные заносят в таблицу 4.