 |
|
КОНТРОЛЬНЫЕ Задания для самостоятельноЙ РАБОТЫ
Задача 6
Осмотическое давление раствора, содержащего в  раствора
раствора  вещества при
вещества при  , составляет
, составляет 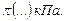 Установите формулу этого вещества, если его состав (...) %.
Установите формулу этого вещества, если его состав (...) %.
| Вариант | Состав вещества, % | 
| 
| 
| 
|

| 4,96 | 251,0 | |||

| 7,3 | 83,0 | |||

| 0,77 | 202,6 | |||

| 2,3 | 297,8 | |||

| 1,55 | 81,0 | |||

| 0,36 | 74,6 | |||

| 16,2 | 303,9 | |||

| 18,4 | 482,2 | |||

| 8,0 | 311,0 | |||

| 3,0 | 481,2 | |||

| 11,6 | 415,3 | |||

| 2,9 | 602,7 | |||

| 11,6 | 587,5 | |||

| 6,2 | 810,4 | |||

| 10,6 | 830,7 | |||

| 9,0 | 415,3 | |||

| 7,85,2 | 699,0 | |||

| 3,1 | 207,7 | |||

| 3,0 | 830,7 | |||

| 4,4 | 567,3 | |||

| 4,68 | 830,7 | |||

| 5,8 | 415,3 | |||

| 4,4 | 413,3 | |||

| 36,0 | 453,8 | |||

| 91,0 | 1134,6 |
2.2. Давление насыщенного пара растворителя над
раствором. Первый закон Рауля
Если в каком-либо открытом сосуде находится чистый растворитель, то в результате процесса испарения над его поверхностью образуется пар и устанавливается равновесие  которое характеризуется давлением насыщенного пара растворителя над чистым растворителем
которое характеризуется давлением насыщенного пара растворителя над чистым растворителем  В чистом растворителе мольная доля растворителя
В чистом растворителе мольная доля растворителя  равна (
равна (  - количество растворителя):
- количество растворителя):
 .
.
Если в данный растворитель ввести нелетучее растворенное вещество, переход которого в парообразную фазу невозможен, то равновесие в системе  нарушится вследствие уменьшения концентрации (мольной доли) растворителя:
нарушится вследствие уменьшения концентрации (мольной доли) растворителя:
 .
.
Тогда, в соответствии с принципом Ле Шателье, начнется процесс конденсации пара, перехода молекул растворителя из парообразной фазы в жидкую, способствующий повышению  , в результате чего давление насыщенного пара растворителя над раствором
, в результате чего давление насыщенного пара растворителя над раствором  станет меньше, чем над чистым растворителем
станет меньше, чем над чистым растворителем 

Cумма мольных долей растворителя  и растворенного вещества
и растворенного вещества  равна:
равна:
 .
.
Тогда  и
и 
Выразив мольную долю вещества  , получим
, получим

Отношение  называется относительным понижением давления насыщенного пара растворителя над раствором.
называется относительным понижением давления насыщенного пара растворителя над раствором.
Первый закон Рауля: относительное понижение давления насыщенного пара растворителя над раствором  , вызываемое присутствием растворенного вещества
, вызываемое присутствием растворенного вещества 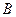 , пропорционально мольной доле растворенного вещества
, пропорционально мольной доле растворенного вещества  .
.
Поскольку в разбавленных растворах количество растворенного вещества  значительно меньше количества растворителя
значительно меньше количества растворителя 
 , то при вычислениях допустимо использовать формулу:
, то при вычислениях допустимо использовать формулу:

Пример 13. Вычислите, каким будет при 25 °С давление пара над раствором, содержащим 2 г антрахинона 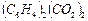 в 500 г анилина
в 500 г анилина  , если давление пара анилина при той же температуре равно 6,79 кПа?
, если давление пара анилина при той же температуре равно 6,79 кПа?
Решение:

Рассчитаем количество вещества (антрахинона)  и количество растворителя (анилина)
и количество растворителя (анилина)  :
:
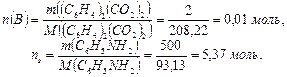
Подставим эти значения в формулу для расчета  , получим:
, получим:

Давление пара над раствором будет

Пример 14. Определите массовую долю нафталина  в бензоле
в бензоле  , если величина понижения давления пара составляет 1,5 % от давления пара чистого растворителя?
, если величина понижения давления пара составляет 1,5 % от давления пара чистого растворителя?
Решение: Воспользуемся формулой

Из условия задачи известно, что  количество вещества
количество вещества  и количество растворителя
и количество растворителя  выразим формулами:
выразим формулами:

Подставим эти выражения в исходную формулу

Отсюда: 
 Подставим эти значения и выразим
Подставим эти значения и выразим  :
:

Воспользуемся этим выражением для расчета массовой доли нафталина.
