 |
|
По ионно-молекулярным
В ионно-молекулярном уравнении ионы - это остатки сильных электролитов. Чтобы составить молекулярное уравнение по ионно-молекулярному, нужно подобрать формулу сильного электролита соответствующего каждому иону.
К данным в ионно-молекулярном уравнении ионам добавляют ионы противоположного знака, чтобы получить формулы сильных кислот, сильных оснований или хорошо растворимых солей. Например, к заданным ионам можно добавить следующие ионы:
| Ион | Добавить |
| H+ | Кислотный остаток сильной кислоты: Cl-; NO3-; SO42-; Br-; I- |
| OH- | Катионы щелочных металлов: K+;Na+ и др. или Ba2+; Sr2+; Ca2+ |
| Ba2+ | 2Cl-;2NO3-;2OH- |
| SO42- | 2H+;2K+;2Na+;2NH4+ и др. |
Пример 27. Составьте молекулярные уравнения реакций, которым соответствует следующее ионно-молекулярное уравнение:

В левой части данного ионно-молекулярного уравнения указаны ионы, которые образуются при диссоциации сильных электролитов. Поэтому при составлении молекулярного уравнения следует подобрать соответствующие сильные электролиты (см. выше):

Такие же ионы необходимо добавить в правую часть уравнения и соединить их между собой. Тогда получим:

Приведённое ионно-молекулярное уравнение выражает сущность реакции. Оно относится к целой группе реакций.
Пример 28. Составьте молекулярное и ионно-молекулярное уравнения, которые доказывают амфотерный характер гидроксида алюминия.
Решение:Для доказательства амфотерного характера гидроксида алюминия необходимо привести уравнения реакций, в которых этот гидроксид проявляет основные и кислотные свойства.
Основные свойства  проявляет при взаимодействии с растворами кислот, например, с серной кислотой:
проявляет при взаимодействии с растворами кислот, например, с серной кислотой:
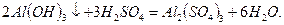
При составлении полного ионно-молекулярного уравнения в виде ионов записываем сильную кислоту  и растворимую соль
и растворимую соль  :
:

Исключив из обеих частей уравнения одинаковые ионы, получаем сокращённое ионно-молекулярное:

Кислотные свойствагидроксид алюминия проявляет при взаимодействии с водными концентрированными растворами щелочей, например, с  :
:

Полное ионно-молекулярное уравнение имеет вид:
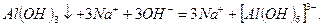
Сокращённое ионно-молекулярное уравнение получаем после сокращения одинаковых ионов:
