 |
|
Образование слабого электролита
Малодиссоциирующие и малорастворимые вещества в ионно-молекулярных уравнениях записываются в молекулярном виде. Реакции, в которых слабые электролиты или малорастворимые вещества входят в состав только продуктов реакции, протекают, как правило, необратимо, т.е. до конца.
Слабые электролиты — химические соединения, молекулы которых даже в сильно разбавленных растворах не полностью диссоциированны на ионы, которые находятся в динамическом равновесии с недиссоциированными молекулами. К слабым электролитам относится большинство органических кислот и многие органические основания в водных и неводных растворах.
Слабыми электролитами являются:
почти все органические кислоты и вода;
некоторые неорганические кислоты: HF, HClO, HClO2, HNO2, HCN, H2S, HBrO, H3PO4, H2CO3, H2SiO3, H2SO3 и др.;
некоторые нерастворимые гидроксиды металлов: Fe(OH)3, Zn(OH)2 и др.; а также гидрат аммиака NH4OH.
Реакции с образованием слабого электролита:
а) Воды: 2NaOH + H2SO4 = H2O + Na2SO4 - молекулярное уравнение реакции,
2Na+ + 2OH- + 2H+ +SO 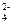 = 2H2O + 2Na+ + SO
= 2H2O + 2Na+ + SO 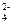
-ионно-молекулярное уравнение реакции,
OH- + H+ = H2O - краткая форма уравнения реакции.
Реакция нейтрализации сильной кислоты сильным основанием сводится к взаимодействию ионов водорода с гидроксид-ионами.
б) Слабой кислоты:
2NaNO2 + H2SO4 = 2HNO2 + Na2SO4
- молекулярное уравнение реакции,
2Na+ + 2NO2- + 2H+ + SO 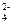 = 2HNO2 + 2Na+ + SO
= 2HNO2 + 2Na+ + SO 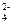
-ионно-молекулярное уравнение реакции,
H+ + NO2- = HNO2 - краткая форма уравнения реакции.
Сильные кислоты вытесняют слабые кислоты из их солей.
в) Слабого основания:
NH4Cl + NaOH = NH4OH + NaCl
- молекулярное уравнение реакции,
NH4+ + Cl- + Na+ + OH- = NH4OH + Na+ + Cl-
-ионно-молекулярное уравнение реакции,
NH4+ + OH- = NH4OH - краткая форма уравнения реакции.
Сильные основания вытесняют слабые основания из их солей.
Примеры реакций, протекающих практически необратимо с образованием слабых электролитов:
а) HCl + NaOH = NaCl + H2O - молекулярное уравнение,
H+ + Cl- + Na+ + OH- = Na+ + Cl- + H2O - полное ионно-молекулярное уравнение,
H+ + OH- = H2O - сокращенное ионно-молекулярное уравнение,
б) NaF + HCl = NaCl + HF,
F- + H+ = HF - сокращенное ионно-молекулярное уравнение,
в) NH4Cl + NaOH = NH4OH + NaCl,
NH4+ + OH- = NH4OH - сокращенное ионно-молекулярное уравнение,
Таким образом, сильные кислоты (основания) вытесняют слабые кислоты (основания) из растворов их солей.
Примеры обратимых реакций, равновесие которых смещено вправо:
HF + NaOH « NaF + H2O,
HF + OH- « F- + H2O - сокращенное ионно-молекулярное уравнение.
Вода более слабый электролит, чем HF: Kд(H2O) = 1,8·10-16 ; Kд(HF) = 6,6·10-4 , поэтому равновесие обратимого процесса смещено в сторону образования H2O.
NH3·H2O + HCl « NH4Cl + H2O,
NH3·H2O + H+ « NH4+ + H2O - сокращенное ионно-молекулярное уравнение
Kд(NH3·H2O) = 1,78·10-5 ; Kд(H2O) = 1,8·10-16
HF + NH3·H2O « NH4F + H2O,
HF + NH4OH « NH4+ + F- + H2O - сокращенное ионно-молекулярное уравнение
Реакции нейтрализации слабых кислот (оснований) сильными основаниями (кислотами) или слабых кислот слабыми основаниями не доходят до конца (т.е. точка эквивалентности находится, соответственно, в основной или кислой области значений рН).
AgCl¯ + NaI « NaCl + AgI¯ ,
AgCl¯ + I- « Cl- + AgI¯ - сокращенное ионно-молекулярное уравнение
ПР(AgCl) = 1,78· 10-10;
ПР(AgI) = 8,3· 10-17
ПР(AgI) меньше ПР(AgCl), равновесие обратимого процесса смещено в сторону образования AgI.
MnS¯ + 2HCl « H2S + MnCl2 ,
MnS¯ + 2H+ « H2S + Mn2+ - сокращенное ионно-молекулярное уравнение
Be(OH)2¯ + 2KOH « K2[Be(OH)4],
Be(OH)2¯ + 2OH- « [Be(OH)4]2- - сокращенное ионно-молекулярное уравнение
Выделение газа
Образование газообразного вещества
Na2S + 2HCl = H2S↑ + 2NaCl
- молекулярное уравнение реакции,
2Na+ + S2- + 2H+ + 2Cl- = H2S↑ + 2Na+ + 2Cl-
-ионно-молекулярное уравнение реакции,
2H+ + S2- = H2S↑ - краткая форма уравнения реакции.