 |
|
Неэлектролиты и электролиты
Свойства растворов относятся к коллигативным свойствам, т.е. к таким свойствам, которые зависят от концентрации частиц в растворе. Изучение свойств растворов различных веществ показало, что для большинства растворов наблюдаются отклонения от закона Р. Рауля.
Например, при растворении 0,1 моля хлорида натрия в 1000 г воды понижение температуры замерзания раствора составило не 0,186о, а 0,318о, т.е. примерно в 2 раза больше теории.
Ван-Гофф ввел в уравнение Р.Рауля поправочный коэффициент, который назвал изотоническим коэффициентом – отношение наблюдаемого значения к расчетному значению.
Полученные экспериментальные данные привели к выводу, что при растворении вещества происходит распад (диссоциация) молекул (кристаллов) растворенного вещества в растворе на более мелкие частицы (ионы).
Растворы, в которых не происходит диссоциация растворенного вещества на ионы, называются растворами неэлектролитов. Система характеризуется отсутствием ионов в растворе и не обладает ионной проводимостью.
Растворы, в которых растворенное вещество распадается на ионы, называются растворами электролитов. Растворы электролитов являются ионными проводниками.
Описание процесса диссоциации изложено в теории электролитической диссоциации созданной С. Аррениусом.
Основные положения этой теории:
1.При растворении электролитов происходит диссоциация (распад) их молекул на заряженные частицы – ионы.
2.При диссоциации устанавливается термодинамическое равновесие между образовавшимися ионами и молекулами.
3.Величина заряда иона совпадает с валентностью атома элемента или кислотного остатка, а число положительных зарядов равно числу отрицательных зарядов.
4.В целом раствор нейтрален. Растворы электролитов проводят электрический ток. Они являются проводниками « второго рода».
Согласно современной теории растворов диссоциация происходит в результате взаимодействия структурных частиц растворённого вещества (молекул, ионов) с молекулами растворителя. Хорошо диссоциируют вещества с ионной и ковалентной полярной связью. Неполярные и малополярные вещества не диссоциируют или диссоциируют очень мало. На диссоциацию электролитов в значительной степени влияет полярность растворителя. Чем выше полярность растворителя, тем выше степень диссоциации электролита.
Диссоциация кислот:
НСl = H+ + Cl-
H2SO4 = 2H+ + SO42-
CH3COOH ↔ H+ + CH3COO-
С точки зрения электролитической диссоциации, кислотами называются электролиты, образующие при диссоциации в водных растворах ионы водорода (Н+).
Диссоциация оснований:
NaOH = Na+ + OH-
Ba(OH)2 = Ba2+ + 2OH-
NH4OH ↔ NH+4 + OH-
Основаниями называются электролиты, которые при диссоциации в водном растворе образуют гидроксид-ионы (ОН-).
Диссоциация солей:
NaCl = Na+ + Cl-
NiSO4 = Ni2+ + SO42-
AlPO4 ↔ Al3+ + PO43-
Солями называются электролиты, которые при диссоциации в водном растворе образуют ионы металлических элементов /катионы/ (за исключением NH4+) и ионы кислотного остатка /анионы/.
Сильные и слабые электролиты
Изучение коллигативных свойств растворов электролитов показало, что в растворах присутствуют наряду с ионами и молекулы, так как диссоциация происходит не полностью, т.е.
КА ↔ К+ + А-
Долю молекул, распавшихся на ионы, характеризуют степенью диссоциации (a). Степень диссоциации – отношение числа распавшихся на ионы молекул (n) к общему числу растворённых молекул N:
a = n / N.
Например: a = 20 %. Это значит, что из 100 молекул электролита 20 молекул распалось на ионы. КА Û К+ + А- и в растворе присутствует 40 ионов, а также 80 нераспавшихся молекул. Всего в растворе будет присутствовать 120 частиц. Изотонический коэффициент равен 1,2
Все электролиты по степени диссоциации делятся на две группы: сильные и слабые.
Электролиты, для которых при эквивалентной концентрации растворов Cн = 0,01-0,1мол/л, степень диссоциации (a) больше 50% относят к сильным. Принято, что сильные электролиты при растворении в воде полностью диссоциируют на ионы (в растворе присутствуют только в виде ионов).
Электролиты, для которых при эквивалентной концентрации растворов Cн = 0,01-0,1мол/л, степень диссоциации (a) меньше, 50 % относят к слабым. Принято, что слабые электролиты при растворении в воде лишь частично диссоциируют на ионы (в растворе присутствуют в основном в молекулярном виде).
К сильным электролитам относятся:
соли, растворимые в воде;
основания элементов I и II групп главных подгрупп Периодической системы элементов Д.И.Менделеева;
кислоты Н2SO4, HNO3, HCl, HBr, HJ, HMnO4, HClO4, HCl03 и др.
К слабым электролитам относятся:
соли, не растворимые в воде;
основания не растворимые в воде, за исключением NH4OH, а также элементов I и II групп главных подгрупп.
кислоты органические (СН3 СООН), H2S, H2SO3, H2CO3, H2SiO3, H3BO3, H3PO4.
К СЛАБЫМ ЭЛЕКТРОЛИТАМ ОТНОСИТСЯ ВОДА ! ! !
Слабые электролиты имеют различную степень диссоциации, которая зависит от концентрации электролита и температуры раствора.
Чтобы исключить влияние концентрации электролита для характеристики диссоциации, используют константу диссоциации.
Так как диссоциация является обратимым процессом КА <=>К+ + А- то по закону действующих масс:


В состоянии равновесия
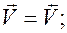



отсюда  .
.
Константа равновесия в этом случае характеризует диссоциацию электролита и называется константой диссоциации / KД /. KД зависит от температуры и не зависит от концентрации раствора. По величине KД можно судить о силе электролита.
Например: Для одной и той же температуры KД (NH4OH) = 1,79∙10-5;
KД (СН3СООН) = 1,75∙10-5;
KД (HСN) = 4,79∙10-10.
Самым слабым электролитом является HСN, имеющая наименьшее значение константы диссоциации.