 |
|
закон разведения Оствальда
 Если a << 1, то
Если a << 1, то
упрощенная формула
закона Оствальда -
a - уменьшается с увеличением концентрации.
Многоосновные слабые кислоты и основания диссоциируют ступенчато:
1 ст.: H2SО3 Û Н+ + HSО3 - КД1 = 1,7×10-2.
2 ст.: HSО3 - Û H+ + SО32 - КД2= 6,3×10-8.
раствор имеет сложный ионно-молекулярный состав.
 |
Сильные электролиты диссоциированы полностью:
CaCl2 ® Ca2+ + 2Cl-
Al2(SO4)3 ® 2Al3+ + 3SО42-
Сионов большая Þ свойства зависят от взаимодействия ионов друг с другом и с молекулами Н2О.

 П.Дебай и Э.Хюккель –1923г - ион окружен противоположно заряженными ионами – ионная атмосфера
П.Дебай и Э.Хюккель –1923г - ион окружен противоположно заряженными ионами – ионная атмосфера

 Чем Сэлектролита Þ среднее расстояние между ионами Þ образование ионных пар.
Чем Сэлектролита Þ среднее расстояние между ионами Þ образование ионных пар.
 |

Ионная сила раствора I -количественная характеристика межионного взаимодействия:

ci– концентрация i -иона
zi- заряд i -иона
g ¹ 1 Þ активность а =g×с.
Для электролита АnВm
 Средний коэффициент активности электролита g± - среднее геометрическое коэффициентов активности образующих его ионов:
Средний коэффициент активности электролита g± - среднее геометрическое коэффициентов активности образующих его ионов:
для раствора Аl2(SО4)3 
gi - зависят от: 1) природы растворителя и
растворенного вещества;
2) концентрации раствора;
3) температуры.
| Концентрация моль/1000г H2O | g электролитов | ||||||
| NaCl | KCl | NaOH | KOH | HCl | H2SO4 | CaCl2 | |
| 0,001 0,01 0,1 0,5 1,0 2,0 5,0 | 0,965 0,874 0,778 0,681 0,657 0,668 0,874 | 0,966 0,901 0,769 0,651 0,607 0,576 - | 0,966 0,900 0,776 0,693 0,679 0,700 1,060 | 0,966 0,900 0,766 0,712 0,735 0,683 1,670 | 0,966 0,904 0,796 0,758 0,809 1,010 2,380 | 0,830 0,544 0,265 0,156 0,132 0,128 0,208 | 0,840 0,580 0,518 0,448 0,500 0,792 0,890 |
· в области высококонцентрированных растворов Þ единицы, десятки и даже сотни.
· в области разбавленных растворов Þ к 1
· в области разбавленных растворов (ниже 0,1 моль/л) g зависят от концентрации и заряда ионов и мало зависят от природы растворенных веществ.
 |
| Ионы | Коэффициент активности для ионной силы | |||||
| 0,001 | 0,01 | 0,02 | 0,05 | 0,07 | 0,1 | |
| водорода Однозарядные Двухзарядные Трёхзарядные | 0,98 0,98 0,77 0,73 | 0,92 0,92 0,58 0,47 | 0.90 0,89 0,50 0,37 | 0,88 0,85 0,50 0,37 | 0,86 0,83 0,36 0,25 | 0,84 0,80 0,30 0,21 |
Задача
Определить активность ионов в 0,01 М растворе СаСl2.
СаCl2 ® Ca 2+ + 2Cl-
С моль/л: 0,01 0,012×0,01 моль/л
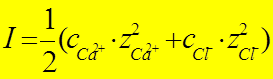 =1/2(0,01×4+0,02×1)= 0,03
=1/2(0,01×4+0,02×1)= 0,03
а = 
Коэффициент активности g находят:
1)по таблице: I = 0,03 Þ 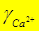 » 0,47;
» 0,47;  » 0,87.
» 0,87.
а  =
= 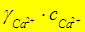 = 0,47×0,01 = 4,7×10-3 (моль/л)
= 0,47×0,01 = 4,7×10-3 (моль/л)
 =
=  = 0,87×0,02 = 1,74×10-2 (моль/л).
= 0,87×0,02 = 1,74×10-2 (моль/л).
2) по формулам:
 если I £ 0,01
если I £ 0,01

если 0,1 > I > 0,01
 |

если I» 1

Вода - очень слабый электролит:
Н2О + Н2О Û Н3О+ + ОН-
 самоионизация
самоионизация
 молизация
молизация
Н2О Û Н+ + ОН-; DH0 298дисс = 55,9 кДж
DS0298 дисс = -80,48 Дж/К
 =1,8×10-16 при 25оС
=1,8×10-16 при 25оС
аН2О = const

ионное произведение Н2О:
DG0дисс=DН0дисс - ТDS0дисс =-RTlnKW
lnKW =-55900/8,31×298 - 80,48/8,31×298

KW = 10-14
K398W = 74×10-14

моль/л
ионы Н+ - носители кислотных свойств
ионы ОН- - носители основных свойств.
Прологарифмируем ионное произведение Н2О
lgKW= lgaH+ + lgaOH- = -14
пусть -lgaH+ = рН – водородный показатель
-lgaOH- = рОН - показатель ионов ОН-
 логарифмическая форма ионного произведения Н2О:
логарифмическая форма ионного произведения Н2О:
при 295 К
| среда | СН+,моль/л | СОН-,моль/л | рН |
| Нейтральная | 10-7 | 10-7 | |
| Кислая | >10-7 | <10-7 | <7 |
| щелочная | <10-7 | >10-7 | >7 |

 |
а) для кислот: аН+ » сН+ рН » - lg сН+
 Þ
Þ  Þ
Þ  Þ рН = -lg сН+
Þ рН = -lg сН+
б) для оснований: аОН- » сОН- рОН » - lg сОН-
 Þ рН = 14 + lgсOH-
Þ рН = 14 + lgсOH-
 |
а) для кислот:
Iр-ра = 0,5×å (сi ××z2i) ÞgН+ (по таблице или формуле) Þ аН+ = gН+ ×сН+ Þ рН = -lg аН+
б) для оснований:
Iр-ра = 0,5×å (сi ××z2i) ÞgOН-(по таблице или формуле) Þ аОН- = gОН-×сОН- Þ рН = 14 + lg аОН-
Задача.
Рассчитать рН 0,05 М раствора НСN.
НСN Û Н+ + СN- - слабая кислота со = 0,05 моль/л
КД= 7,9×10-10 (из таблицы)
a =  =
=  = 1,26×10-4.
= 1,26×10-4.
сH+ = aсо = 1,26×10-4×0,05 = 6,3×10-6
рН = ‑lg сH+ = - lg 6,3×10-6 = 5,18.
Задача
Рассчитать рН 0,05 М раствора NаОН.
Решение
NаОН ® Nа+ + ОН- - сильное основание
с: 0,05 0,05 0,05 моль/л
I = 1/2(0,05×12 + 0,05×12) = 0,05.
gОН- = 0,85 (по таблице)
аОН- = gОН-×сOH- = 0,85×0,05 = 0,043
рН = 14 + lg аОН- = 14 - 1,37 = 12,63.
| Индикатор | Область рH | Окраска | |
| В кислом растворе | В щелоч растворе | ||
| Пикриновая кислота Метиловый оранжевый Лакмус Феноловый красный Фенолфталеин Ализариновый желтый | 0,0-2,0 3,1-4,4 6,0-8,0 6,8-8,4 8,2-10,0 10,1-12,1 | Бесцветная Красная >> Желтая Бесцветная Желтая | Желтая >> Синяя Красная Малиновая Оранжевая |

Гидролиз – результат поляризационного взаимодействия ионов соли с их гидратной оболочкой.
Соли - сильные электролиты:
КА ® Кm+ + An-
Гидролиз:

 Кm+ + НOH Û КОН(m-1)+ + H+
Кm+ + НOH Û КОН(m-1)+ + H+
 или
или

 An- + НОH Û HA(n-1)- + OH-
An- + НОH Û HA(n-1)- + OH-
малодиссоциированные изменение рН раствора
частицы
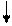
 Чем заряд и радиус иона Þ сильнее взаимодействие с Н2О Þ сильнее гидролиз.
Чем заряд и радиус иона Þ сильнее взаимодействие с Н2О Þ сильнее гидролиз.
DНг > 0 - эндотермический процесс.
Количественная характеристика гидролиза:
 |
 |
(для разбавленных растворов а = с)
Гидролиз – обратимый равновесный процесс

КГ - константа гидролиза
Сi –равновесные концентрации
КГ зависит от: природы реагентов и Т.
 |
 Т.к. DНГ > 0 Þ с температуры КГ Þ
Т.к. DНГ > 0 Þ с температуры КГ Þ
выход продуктов гидролиза растет.
Применим закон разведения Оствальда:



 | |||||
 | |||||
 | |||||







 | |||
 | |||
Соли, образованные сильной кислотой и сильным основанием (Na2SO4) – гидролизу не подвергаются.
 Na2SO4 ® Na+ + SO42-
Na2SO4 ® Na+ + SO42-
NaOH H2SO4
Сильное основание сильная кислота
раствор нейтральный: рН » 7.
 |

 Диссоциация соли: СН3СООNa ® CH3COO- + Na+
Диссоциация соли: СН3СООNa ® CH3COO- + Na+
CH3COOH NaOH
Слабая кислота сильное основание
Гидролиз – по слабому электролиту:
CH3COO- + НОН Û CH3COOH + ОН-
 выражение константы гидролиза
выражение константы гидролиза
Гидролиз многозарядных ионов протекает ступенчато (FeCl3):
Fe3+ + НОН Û FeОН2+ + Н+ - 1-я ступень;
FeОН2+ + НОН Û Fe(ОН)2+ + Н+ - 2-я ступень;
Fe(ОН)2+ + НОН Û Fe(ОН)3 + Н+ - 3-я ступень



 Кг1> Кг2 > Кг3
Кг1> Кг2 > Кг3

AgNO3 ® Ag+ + NO3-
 |  | ||
AgОН HNO3
слабое основание сильная кислота
 Ag+ + НОН Û AgОН + Н+.
Ag+ + НОН Û AgОН + Н+.
кислая среда рН< 7
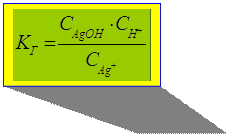
-константа гидролиза

 KW
KW


КД(AgOH) : AgOH Û Ag+ + OH-
 |
- константа гидролиза по
катиону
Если КГ (1-ой ступени) Þ КД (последней ступени)
Если КГ (последней ступени) Þ КД (1-ой ступени)
Расчет рН гидролиза по катиону:



 Na2S ® Na+ + S2-
Na2S ® Na+ + S2-
NaOH H2S
сильное основание слабая кислота
 Гидролиз по ступеням:
Гидролиз по ступеням:
1cт.: S2- + HOН Û HS- + ОН-
2ст.: HS- + HOН Û H2S + ОН-

КГ(1ст) > КГ(2ст)

 кw
кw


- константа гидролиза по аниону
(Кг 1 Þ КД последней)
Расчет рН гидролиза по аниону:

Гидролиз и по катиону и по аниону:

NН4СN, РbCO3, Аl2S3
NН4СN Û NН4+ + ОН-
Гидролиз:
СN- + НОН Û НСN + ОН-
NН4+ + НОН Û NН4ОН + Н+
NН4+ + СN- + Н2О Û NН4ОН + НСN
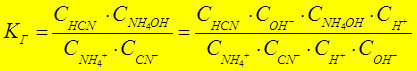
 |

КД(NH4OH)=1,79×10-5 > КД(НСN) =7,9×10-10 Þ

Концентрация соли не влияет на b Þ
Расчет рН гидролиза по катиону и аниону:
 |
Если в результате гидролиза Þ труднорастворимые или газообразные вещества Þ гидролиз необратимым:
PbCO3 + Н2О ® Pb(ОН)2¯ + CO2
 |
 1) при температуры:
1) при температуры:

 DНГ > 0 Þ с температурыÞ КГ =b2 ×С0 ;
DНГ > 0 Þ с температурыÞ КГ =b2 ×С0 ;
 2) с разбавлением раствора (концентрация );
2) с разбавлением раствора (концентрация );
 3) при концентрации иона, определяющего среду
3) при концентрации иона, определяющего среду
СN- + НОН Û НСN + ОН-
НСl ® Cl- + H+
Задача
Рассчитать КГ, b и рН 0,01 М раствора К2SО3.
Решение
Диссоциация сильного электролита К2SО3:

 К2SО3 ® 2К+ + SО32-
К2SО3 ® 2К+ + SО32-
КОН Н2SО3
Сильное основание слабая кислота
Гидролиз по SО32-:
1-ая ступень: SО32-+ НОН Û НSО3-+ОН-
КГ1 =  = 1,59×10-7
= 1,59×10-7
2-ая ступень: НSО3- + Н2О Û Н2SО3 + ОН-
КГ2 =  = 5,9×10-13 КГ1 > КГ2
= 5,9×10-13 КГ1 > КГ2
b =  =
=  = 4×10-3 < 1 Þ расчет по приближенной формуле правомерен.
= 4×10-3 < 1 Þ расчет по приближенной формуле правомерен.
СOH- = b×c0 = 4×10-3×10-2 = 4×10-5
рН = 14 + lg СOH- =14 - 4,4 = 9,6
 |
В насыщенных растворах сильных электролитов АnBm равновесие:
АnBm(тв) Û n Am+(p-р) + m Bn-(p-р) - гетерогенный пр.
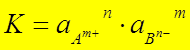 = ПРАnBm, т.к. аАnВm(тв) = const
= ПРАnBm, т.к. аАnВm(тв) = const


ПР зависит: от природы электролита и
растворителя, от температуры;
ПР не зависит от активностей ионов.
ПР25С –таблица
Пример: Ag2CO3(тв) Û 2Ag+(р-р) + CO32-(р-р)

Если (  ) ³ ПРтабл – осадок выпадает
) ³ ПРтабл – осадок выпадает
Если (  ) < ПРтабл – осадок не выпадает
) < ПРтабл – осадок не выпадает

сР - растворимость - концентрация насыщенного раствора электролита
В насыщенном растворе:
АnBm(тв) Û n Am+(нас. p-р) + m Bn-(нас. p-р)
СР nсР mсР моль/л
ПР =  = (gАm+×n ×сР)n × (gB n-×m ×сР)m=
= (gАm+×n ×сР)n × (gB n-×m ×сР)m=
=(gАm+)n ×(gB n-)m × nn × mm ×(сР)n+m
 |
- - растворимость
- труднорастворимого
сильного электролита
 если g ® 1
если g ® 1
Задача
Определить сР MgF2, в растворе, в котором
g(Mg2+)=0,7, g(F-)=0,96
MgF2 Û Mg2+ (нас.р-р) + 2F-(нас.р-р)
ПР(MgF2) = 4×10-9 = 
СР =  моль/л
моль/л
 |
1) ионной силы раствора – введение растворимого электролита, не имеющего общих ионов
 ПР = gMg2+ ×СMg2+ ×СF-2 ×gF-2
ПР = gMg2+ ×СMg2+ ×СF-2 ×gF-2

 С ионной силы раствора (I) Þ gi Þ CР
С ионной силы раствора (I) Þ gi Þ CР
Þ чтобы при Т=const Þ ПР =const
2) от введения одноименного иона
MgF2 Û Mg2+ (нас.р-р) + 2F-(нас.р-р)
NaF Û Na+ (р-р) + F-(р-р)

 СF- Þ равновесие смещается влево Þ СР
СF- Þ равновесие смещается влево Þ СР
 На этом явлении основано разделение элементов методом осаждения: растворимость СаСО3 и МgСО3 при введении в раствор хорошо растворимых К2СО3 или Nа2СО3 Þ ионы жесткости Са2+ и Мg2+ удаляются из раствора.
На этом явлении основано разделение элементов методом осаждения: растворимость СаСО3 и МgСО3 при введении в раствор хорошо растворимых К2СО3 или Nа2СО3 Þ ионы жесткости Са2+ и Мg2+ удаляются из раствора.