|
|
Частичный случай гетерокоагуляции
-взаимная коагуляция (золь «-» заряд + золь «+» заряд => взаимная коагуляция)
Скрытая коагуляция-образование частиц низших порядков(I,II,III)которое протекает незаметно для невооруженного взгляда.
Явная коагуляция-золь претерпевает видимые изменения,ион мутнеет или изменяется его окраска,при этом величина электрокинетического потенциала частиц уменьшается.
Медленная коагуляция-при которой всякое увеличение концентрации электролита ускоряет коагуляцию.
Быстрая коагуляция-когда дальнейшее повышение концентрации электролита уже не влияет на ее скорость, т.е. коагуляция протекает с максимальной быстротой.
Гетерокоагуляция- коагуляция коллоидных растворов, содержащих разнородные частицы отличающиеся по химической природе, знаку и величине заряда.
1)на водоочистительных станция
Коагуляция - процесс слипания (слияния) коллоидных частиц с образованием более крупных агрегатов с последующей потерей кинетической устойчивости.
В общем смысле под коагуляцией понимают потерю агрегативной устойчивости дисперсной системы.
Скрытая стадия коагуляции – очень быстрая – размер частиц увеличивается, но осадок не выпадает – изменение окраски, помутнение.
Явная стадия – выпадение осадка, выделение двух фаз в растворе. Осадок называется коагулят.
Конечным итогом коагуляции могут быть два результата: разделение фаз и образование объемной структуры, в которой равномерно распределена дисперсионная среда (концентрирование системы). В соответствии с двумя разными результатами коагуляции различают и методы их исследования (для первого результата – оптические, например, для второго – реологические).
Действие электролитов на коагуляцию
Установлен ряд эмпирических закономерностей воздействия электролитов, которые известны под названием правил коагуляции:
Любые электролиты могут вызвать коагуляцию, однако заметное воздействие они оказывают при достижении определенной концентрации.
Порог коагуляции – минимальная концентрация электролита, вызывающая коагуляцию (, моль/л; иногда Ск ).
Порог коагуляции определяют по помутнению, изменению окраски или по началу выделения дисперсной фазы в осадок.
Правило Шульце-Гарди (правило значности, эмпирическое):
Коагулирующим действием обладает тот ион электролита, который имеет заряд, противоположный заряду потенциалопределяющих ионов мицеллы (гранулы), причем, коагулирующее действие тем сильнее, чем выше заряд.
где К – коагулирующая способность (примем ее за единицу).
По правилу Шульца – Гарди значение порогов коагуляции для противоионов с зарядами 1, 2 и 3 соотносятся как 1:1/20:1/500, т.е. чем выше заряд, тем меньше требуется электролита, чтобы вызвать коагуляцию.
Правило Шульце – Гарди имеет приближенный характер и описывает действие ионов лишь неорганических соединений.
В ряду органических ионов коагулирующее действие возрастает с повышением адсорбционной способности.
Коагуляция коллоидных систем может происходить и в результате вибрационных воздействий и влияния ультразвукового поля. Особенное значение вибрационная коагуляция имеет в технике при получении различных паст, бетонов и других систем. Например, виброобработка бетонной смеси вначале ведет к разрушению в ней коагуляционной структуры и в результате этого к увеличению текучести смеси, что облегчает заполнение смесью форм. [1]
Коагуляция коллоидных систем в момент их образования, в отличие от коагуляции золей, изучена еще недостаточно. Исследования, проведенные в этом направлении, посвящены галогени-дам и роданиду серебра. [2]
Коагуляция коллоидных систем может быть вызвана самыми разнообразными причинами и прежде всего добавкой электролита. Наблюдается коагуляция также и при изменении температуры, механическом воздействии, под влиянием света, ультразвука и пр. Но как бы ни были разнообразны эти причины, нарушение агре-гативной устойчивости всегда связано с изменениями структуры защитных слоев стабилизатора. [3]
Коагуляция коллоидных систем может происходить и в результате вибрационных воздействий и влияния ультразвукового поля. Особенное значение вибрационная коагуляция имеет в технике при получении различных паст, бетонов и других систем. Например, виброобработка бетонной смеси вначале ведет к разрушению в ней коагуляционной структуры и в результате этого к увеличению текучести смеси, что облегчает заполнение смесью форм. Однако при дальнейшей виброобработке образуется прочная кристаллизационная структура. [4]
Коагуляция коллоидных систем наступает не только иод, действием электролитов, но и при смешении двух золей с различными знаками зарядов частиц. [5]
Коагуляция коллоидных систем может происходить и в результате вибрационных воздействий и влияния ультразвукового поля. Особенное значение вибрационная коагуляция имеет в технике при получении различных паст, бетонов и других систем. Например, виброобработка бетонной смеси вначале ведет к разрушению в ней коагуляционной структуры и в результате этого к увеличению текучести смеси, что облегчает заполнение смесью форм. [6]
Самопроизвольно коагуляция коллоидных систем протекает чрезвычайно медленно. В основном она происходит в результате воздействия внешних факторов - механических воздействий, электрического тока, изменения температуры, жесткого излучения, введения в систему электролитов и неэлектролитов, приводящих к понижению t - потенциала. Начальная стадия, при которой укрупнение частиц не вызывает внешнего изменения золя, что можно оценить только с помощью ультрамикроскопа, называется скрытой коагуляцией. Появление опалесценции, изменение окраски и выделение дисперсной фазы в осадок, называемый коагулятом, характеризует явную коагуляцию. Наибольшее значение - потенциала, при котором коагуляция протекает с заметной скоростью, называется критическим. [7]
Факторы коагуляции коллоидных систем бывают весьма разнообразными. Коагуляция может быть вызвана повышением температуры, длительным диализом, добавлением электролитов, разного рода механическими воздействиями ( размешиванием, встряхиванием, взбалтыванием), сильным охлаждением, ультрацентрифугированием, концентрированием, пропусканием электрического тока, а также действием на данный золь других золей. Поскольку главное условие уменьшения устойчивости коллоидных растворов - потеря электрического заряда, основными методами их коагулирования являются методы снятия зарядов. Чаще всего в практике для этой цели пользуются воздействием на коллоидные растворы различных электролитов. [8]
Факторы коагуляции коллоидных систем могут быть весьма разнообразными. Так, например, коагуляция может быть вызвана повышением температуры, длительным диализом, добавлением электролитов, разного рода механическими воздействиями ( размешиванием, встряхиванием, взбалтыванием), сильным охлаждением, ультрацентрифугированием, концентрированием, пропусканием электрического тока, а также действием на данный золь других золей. [9]
Факторы коагуляции коллоидных систем бывают весьма разнообразными. Коагуляция может быть вызвана повышением температуры, длительным диализом, добавлением электролитов, разного рода механическими воздействиями ( размешиванием, встряхиванием, взбалтыванием), сильным охлаждением, ультрацентрифугированием, концентрированием, пропусканием электрического тока, а также действием на данный золь других золей. Поскольку главное условие уменьшения устойчивости коллоидных растворов - потеря электрического заряда, основными методами их коагулирования являются методы снятия зарядов. Чаще всего в практике для этой цели пользуются воздействием на коллоидные растворы различных электролитов. [10]
В ряду неорганических ионов одинаковой зарядности их коагулирующая активность возрастает с уменьшением гидратации.
Гетерокоагуляция широко используется в процессах водопод-готовки и очистки сточных вод. В воду добавляют минеральные коагулянты, например, соли алюминия, железа, магния, кальция. Эти соли снижают агрегативную устойчивость системы, и частицы загрязняющих веществ выпадают в осадок. Однако эффективность очистки воды от коллоидных дисперсий определяется не только снижением электростатического барьера, а главным образом, гете-рокоагуляцией. [1]
Гетерокоагуляции аналогичен процесс флокуляции, заключающийся в образовании агрегатов ( хлопьев) из гетерогенных частиц в результате собирающего действия высокомолекулярных веществ, называемых флокулянтами. Механизм действия флокулянтов заключается в их адсорбции на нескольких частицах с образованием полимерных мостиков, связывающих частицы между собой. При неоптимальных количествах флокулянта может наблюдаться, наоборот, стабилизация дисперсной - системы. Флокулянты подразделяют на неорганические и органические, природные и синтетические, на ионогенные, неионогенные и амфотерные. [2]
Гетерокоагуляция широко используется в процессах водо-подготовки и очистки сточных вод. В воду добавляют минеральные коагулянты, например соли алюминия, железа, магния, кальция. Эти соли снижают агрегативную устойчивость системы, и частицы загрязняющих веществ выпадают в осадок. Эффективность очистки воды от коллоидных дисперсий определяется не только снижением электростатического барьера, а главным образом гетерокоагуляцией. [3]
Гетерокоагуляции аналогичен процесс флокуляции, заключающийся в образовании рыхлых агрегатов ( хлопьев) из частиц ( не имеющих непосредственного контакта между собой) в результате собирающего действия высокомолекулярных веществ, называемых флокулянтами. Механизм действия флоку-лянтов заключается в их адсорбции на нескольких частицах с образованием полимерных мостиков, связывающих частицы между собой. [4]
Гетерокоагуляция и гетероадакоагуляция имеют важнейшее значение в процессе контактного осветления воды. [5]
Гетерокоагуляция коллоидных частиц, несущих противоположные заряды, представляет собой очень сложное явление, поскольку поведение системы зависит от относительных размеров и концентрации частиц, способа приготовления смеси и некоторых операций, выполняемых после смешивания. Как было показано Хил и и др. [271], при смешивании коллоидных кремнезема и оксида алюминия-происходит коагуляция. В том случае, когда коагулят диспергируется путем перемешивания, то он формируется снова, но уже более медленно, пока коагуляция не прекратится. [6]
Нейтрализационная коагуляция происходит при добавлении к золю неиндифферентного электролита. При этом потенциалопределяющие ионы связываются в малорастворимое соединение, что приводит к уменьшению абсолютных величин термодинамического потенциала, а следовательно, и z-потенциала вплоть до нуля.
Если взять в качестве исходного только что рассмотренный золь хлорида серебра, то для нейтрализации потенциалопределяющих ионов Ag+ в золь необходимо ввести, например, хлорид калия. После добавления определённого количества этого неиндифферентного электролита мицелла будет иметь вид:
В системе не будет ионов, способных адсорбироваться на поверхности частицы AgCl, и поверхность станет электронейтральной. При столкновении таких частиц происходит коагуляция.
Так как причиной коагуляции в данном случае является нейтрализация потенциалопределяющих ионов, такую коагуляцию называют нейтрализационной коагуляцией.
Необходимо отметить, что для полной нейтрализационной коагуляции неиндифферентный электролит должен быть добавлен в строго эквивалентном количестве.
концентрационная коагуляция обусловлена сжатием двойного электрического слоя в результате увеличения ионной силы раствора. [1]
Наряду с нейтрализационной коагуляцией существует концентрационная коагуляция, Концентрационная коагуляция имеет место, когда она происходит под действием индифферентного электролита вследствие сжатия диффузного слоя противоионов и уменьшения абсолютного значения -потенциала.
Кинетика коагуляции характеризуется двухстадийным преодолением энергетического барьера, связанным со стабильностью латекса, обусловленной наличием адсорбционного слоя, образующегося за счет эмульгатора и полиэлектролита. Разрушение солевой формы полимера и перевод его в кислотную способствует понижению агрегативной устойчивости системы. [1]
Различают медленную и быструю коагуляцию. Во время быстрой коагуляции все сталкивающиеся первичные частицы объединяются в агрегаты, а вот во время медленной коагуляции в агрегаты соединяются на много меньше первичных частиц. Также Коагуляция может происходить в жидкой и в газообразной среде.
Согласно правилу Шульце-Гарди, с увеличением заряда иона-коагулятора порог коагуляции уменьшается, а коагулирующая способность возрастает
11. Пентизация- процесс, обратной коагуляции –превращение свежего осадка, образовавшегося при коагуляции, в коллоидный раствор под действием пептизаторов
Коллоидная защита –повышение агрегативной устойчивости лиофобных золей при добавлении к ним достаточного количества высокомолекулярных соединений
Флокуляция –агрегирование частиц дисперсной фазы в лиофобных золях под действием небольших количеств высокомолекулярных соединений, имеющих гибкие макромолекулы и содержащих одинаковые функции групп на концах
Биологическая роль
1)Флокулянты широко исп. при подготовке воды для технических и бытовых нужд обогащений полезных ископаемих в бумажном производстве в с/х (для улучшения структуры почв) при водоочистке


 12. Лиофильные растворы – растворы в которых ДС и ДФ взаимодействуют сильно, термодинамически устойчивы.
12. Лиофильные растворы – растворы в которых ДС и ДФ взаимодействуют сильно, термодинамически устойчивы.
ККА- повышенная концентрация до критической величины
Мицеллы ПАВ-
ПАВ –(поверхностно –активные вещества ) –химические соединения . которые концентрируясь на поверхности раздела фаз вызывают снижение поверхностные натяжения
В прямых мицеллах –образуются ядра
Наружная часть мицеллы-оболочка, образованная полярными группами.
Полярные группы молекулы ПАВ обращены к полярной ДС.
В обратных мицеллах молекулы ПАВ диаметрально противоположны по сравнению с прямыми мицеллами.
Ядро состоит из полярных групп,в сторону неполярной ДС обращены УВ цепи.
Липосомы-замкнутые пузырьки воды, окруженные двумя или несколькими слоями фосфолипидов или сфинголипидов.
Липосомальная терапия-применяется при лечении онкологических,инфекционных заболеваий, диабета.
Гидрофильно-липофильный баланс(ГЛБ) – число, характеризующее эффективность эмульгатора, соотношение 2х противоположных групп молекулы-гидрофильной и гидрофобной(лиофильной).


 13.ВМС – высокомолекулярные соединения,с молекулярной массой 10 в 4степ-10 в 6 степ и выше.
13.ВМС – высокомолекулярные соединения,с молекулярной массой 10 в 4степ-10 в 6 степ и выше.
Классификация ВМС:
-природного происхождения9белки,полисахариды,пептиды)
-синтетические(полученные в процессе полимеризации или конденсации)
В зависимости от строения основной цепи ВМС делятся на линейные, разветвленные и трехмерные (пространственные) структуры.
Примеры биополимеров:
-белки
-нукл.кислоты
-полисахариды
Методы получения:
-полимеризация-реакция присоединения без выделения побочных продуктов.
-поликонденсация-замещения с отщеплением низкомолекулярных побочных продуктов
Применение в медицине:
В медицине применяются изготовленные из синтетических полимеров искусственные суставы, сосуды и т. п. ,полностью заменяющие настоящие. Часто они изготавливаются из материалов на основе ВМС (полимеров) – пластмасс
Примеры: глюкоза, фруктоза, галактоза, рибоза, дезоксирибоза.




 14.
14. 

 15.
15. 

 16.
16. 
 17.
17. 


 18.
18. 

 19.
19. 

 20.
20. 

 |  | ||
 21.
21. 
 22. Карбонильная группа имеет тригональный sp2-гибридизованный атом углерода(C),который образует 3 сигма-связи,лежащие в одной плоскости и пи-связь с атомом кислорода(O) за счет негибридизованной p-орбитали.
22. Карбонильная группа имеет тригональный sp2-гибридизованный атом углерода(C),который образует 3 сигма-связи,лежащие в одной плоскости и пи-связь с атомом кислорода(O) за счет негибридизованной p-орбитали.
Схема распределения электронной плотности:
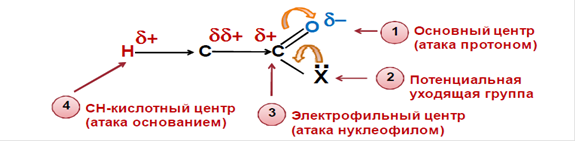
Реакционные центры альдегидов и кетонов:
1)Электрофильный центр- электронно-дефицитный атом С,предопределяющий возможность нуклеофильной атаки.
2)Основный(Нуклеофильный)- атом О карбонильной группы.Является местом электрофильной атаки
3)СН-кислотный центр – имеется в альдегидах и кетонах,может подвергаться атаке основанием.
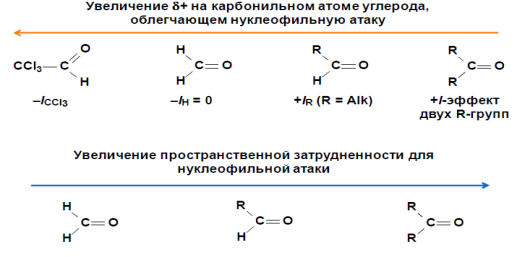
 23. Реакции нуклеофильного присоединения – реакции, в которых атаку на начальной стадии осуществляет нуклеофил — частица, заряженная отрицательно или имеющая свободную электронную пару. На конечной стадии образующийся карбанион подвергается электрофильной атаке.
23. Реакции нуклеофильного присоединения – реакции, в которых атаку на начальной стадии осуществляет нуклеофил — частица, заряженная отрицательно или имеющая свободную электронную пару. На конечной стадии образующийся карбанион подвергается электрофильной атаке.
По данным схемам мы можем сопоставить реакционную способность An в гомологическом ряду альдегидов, кетонов и сравнить их между собой.
24. А)Спирты при взаимодействии с альдегидами образуют полуацетали,которые превращаются в ацетали при обработке избытком спирта 
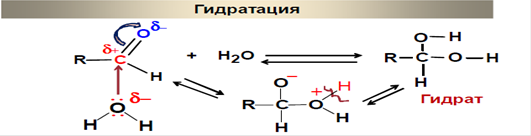
Б)Гидратация-присоединение воды к карбонильной группе,обратимая реакция
В)Образование иминов(оснований Шиффа)-реакция между альдегидами,кетонами и первичными аминами: 
Восстановительное аминирование: 
Циановодородная кислота присоединяется к альдегидам и кетонам с образованием альфа-гидроксинитрилов: 
Реакции конденсации альдегидов и кетонов проходят в присутствии некоторых количеств кислот и щелочей.Если кислоты и щелочи разбавлены происходит альдольная конденсация,если же условия более жесткие,то происходит кротоновая конденсация: 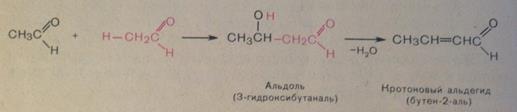 Полимеризация характерна в основном для альдегидов.Примером может служить образование параформа из формалина:
Полимеризация характерна в основном для альдегидов.Примером может служить образование параформа из формалина: 


 25. Строение карбоновых кислот-молекула содержит одну или несколько функциональных карбоксильных групп -COOH.
25. Строение карбоновых кислот-молекула содержит одну или несколько функциональных карбоксильных групп -COOH. 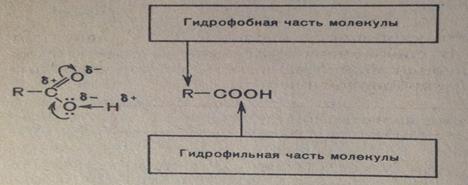
Классификация.Карбоновые кислоты могут быть:алифатическими,ароматическими и гетероциклическими.
Тип гибридизации углерода – sp2.Электронное строение молекул:
Электронная плотность сдвинута в сторону карбонильного кислорода С=О, что снижает величину отрицательного заряда на кислороде группы – ОН и создает условия для диссоциации (отщепление протона Н+) и образования ацелат – иона.
Реакционные центры карбоновых кислот:
1)OH-кислотный
2)СН-кислотный
3)Электрофильный
 26. Кислотность карбоновых кислот зависит от влияния связанного с карбоксилом углеводородного радикала. Самой сильной одноосновной карбоновой кислотой является муравьиная, в которой карбоксил не связан с радикалом. Кислоты, содержащие в соединении с карбоксилом предельные углеводородные остатки, значительно слабее муравьиной кислоты. Это объясняется электродонорными свойствами алкильных остатков; они вызывают смещение электронов связи R-C.А это в свою очередь в некоторой степени компенсирует положительный заряд карбонильного углерода и, следовательно, уменьшает его влияние на гидроксильную группу.
26. Кислотность карбоновых кислот зависит от влияния связанного с карбоксилом углеводородного радикала. Самой сильной одноосновной карбоновой кислотой является муравьиная, в которой карбоксил не связан с радикалом. Кислоты, содержащие в соединении с карбоксилом предельные углеводородные остатки, значительно слабее муравьиной кислоты. Это объясняется электродонорными свойствами алкильных остатков; они вызывают смещение электронов связи R-C.А это в свою очередь в некоторой степени компенсирует положительный заряд карбонильного углерода и, следовательно, уменьшает его влияние на гидроксильную группу.
 27. Образование сложных эфиров происходит путем реакции этерификации:
27. Образование сложных эфиров происходит путем реакции этерификации: 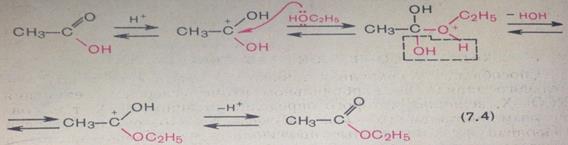
28. Двухосновные карбоновые кислоты-соединения с двумя карбоксильными группами.
Щавелевая кислота НООС-СООН – ее соли называют оксалатами,некоторые из которых друдно растворимы и образуют камни в мочевом пузыре.
Малоновая кислота НООС-СН2-СООН
Янтарная и глутаровая кислоты легко отщепляют воду при нагревании и образуют 6 и 5-членные циклические ангидриды,а при обработке аммиаком – циклические амиды

 .
. 
Превращение янтарной кислоты в фумаровую катализируется ферментом сукцинатдегидрогеназой и коферментом ФАД: 
 29. Аминоспирты- соединения, содержащие одновременно амино- и гидроксигруппы. Простейшим аминоспиртом является коламин. Коламин-вязкая жидкость ,образующая устойчивые соли с сильными кислотами. Компонент сложных липидов.
29. Аминоспирты- соединения, содержащие одновременно амино- и гидроксигруппы. Простейшим аминоспиртом является коламин. Коламин-вязкая жидкость ,образующая устойчивые соли с сильными кислотами. Компонент сложных липидов. 
Из коламина при исчерпывающем метилировании образуется холин. Холин-витаминоподобное вещ-во регулирующее жировой обмен.В организме образуется из серина. Компонент сложных липидов.
30. 

31. 








38.ФОСФОЛИПИДЫ, природные липиды, содержащие в молекуле остаток фосфорной к-ты, связанной эфирной связью с производным многоатомного спирта. Наиб. распространенная группа фосфолипидов- фосфоглицериды общей ф-лы ROCH2CH(OR' )СН2ОР(О)(О-)ОХ (R, R' - алкил, алкенил, ацил; X = H, CH2CH2N+H3 и др·)· К фосфолипидам относятся также фосфосфинголипиды RCH(OH)CH(NHCOR')CH2OP(O)(O-)OX (R - алкил, алкенил, R' - ацил), диольные фосфолипиды RO(CH2)nCH2OP(O)(O-)Х (см. Диольные липиды, n =1-4)и фосфонолипиды [напр., ROCH2CH(OR')СН2ОР(О)(О-) — CH2CH2N+H3 и ROCH2CH(OR')CH2P(O)(O-)OCH2CH2N+H3].
Молекулы фосфолипидов содержат неполярные гидрофобные "хвосты" и полярную гидрофильную "головку" (остаток фосфорной к-ты), что определяет мн. физ.-хим. св-ва, в т. ч. способность формировать мембраны биологические.
При рН ок. 7 фосфатная группа мн. фосфолипидов ионизирована. Фосфолипиды гидролизуются фосфолипазами. При мягком щелочном гидролизе отщепляются жирные к-ты, но не затрагиваются сложноэфирные связи остатка фосфорной к-ты; при жестком щелочном гидролизе отщепляется также XOH. К-ты гидро-лизуют все сложноэфирные связи.
основан на фосфорилировании 1,2-ди-ацил-sn-глицеринов разл. активированными производными N-защищенного фосфоэтаноламина или на взаимод. фосфа-тидовых к-т с N-защищенным этаноламином в присут. активирующих агентов.
ФОСФАТИДИЛХОЛИНЫ(1,2-диацил-sn-и-глицеро-3-фос-фохолины, лецитины), соед. общей ф-лы  , где R - обычно ацил насыщенной, R' - ненасыщенной к-ты с 16-24 атомами С в цепи (преобладают к-ты C16 и C18). Фосфатидилхоли́ны ― группа фосфолипидов, содержащих холин. Также входят в группу лецитинов. Фосфатидилхолины одни из самых распространенных молекул клеточных мембран.
, где R - обычно ацил насыщенной, R' - ненасыщенной к-ты с 16-24 атомами С в цепи (преобладают к-ты C16 и C18). Фосфатидилхоли́ны ― группа фосфолипидов, содержащих холин. Также входят в группу лецитинов. Фосфатидилхолины одни из самых распространенных молекул клеточных мембран.
ФОСФАТИДИЛЭТАНОЛАМИНЫ (1,2-диацил-  -глице-ро-3-фосфоэтаноламины), соед. общей ф-лы -глице-ро-3-фосфоэтаноламины), соед. общей ф-лы  , где R - обычно ацил насыщенной, a R' - ненасыщенной к-ты с 16-24 атомами С в цепи.
Бесцв. кристаллы. Для димиристоил-, дипальмитоил- и дистеароилфосфатидилэтаноламинов т. пл. соотв. 195-196, 186-187 и 180-182 0C; т.размягч. 86, 88 и 83 0C; [a]26D +6,7, +6,4 и 6,0 0C (хлороформ). При обработке щелочью фосфатидилэтаноламины гидролизуются с образованием к-т и sn-глицеро-3-фосфоэта-ноламина.
При диспергировании в воде и солевых р-рах при рН ок. 7 фосфатидилэтаноламины липосом не образуют, однако при диспергировании в р-рах с низкой ионной силой, а также при высоких значениях рН формируют бислойные модельные мембраны. Аналогичные структуры они образуют в смеси с фосфатидилхолинами.
Фосфатидилэтаноламины содержатся во всех органах животных. В значит, кол-вах обнаружены в головном мозге, в плазме крови, печени и почках. Фосфатидилэтаноламины и N-ацил-фосфатидилэтаноламины найдены и в разл. видах морских организмов, в т. ч. у рыб; являются одними из осн. представителей липидов бактерий. , где R - обычно ацил насыщенной, a R' - ненасыщенной к-ты с 16-24 атомами С в цепи.
Бесцв. кристаллы. Для димиристоил-, дипальмитоил- и дистеароилфосфатидилэтаноламинов т. пл. соотв. 195-196, 186-187 и 180-182 0C; т.размягч. 86, 88 и 83 0C; [a]26D +6,7, +6,4 и 6,0 0C (хлороформ). При обработке щелочью фосфатидилэтаноламины гидролизуются с образованием к-т и sn-глицеро-3-фосфоэта-ноламина.
При диспергировании в воде и солевых р-рах при рН ок. 7 фосфатидилэтаноламины липосом не образуют, однако при диспергировании в р-рах с низкой ионной силой, а также при высоких значениях рН формируют бислойные модельные мембраны. Аналогичные структуры они образуют в смеси с фосфатидилхолинами.
Фосфатидилэтаноламины содержатся во всех органах животных. В значит, кол-вах обнаружены в головном мозге, в плазме крови, печени и почках. Фосфатидилэтаноламины и N-ацил-фосфатидилэтаноламины найдены и в разл. видах морских организмов, в т. ч. у рыб; являются одними из осн. представителей липидов бактерий.
|
39.Сфинголипиды — это класс липидов, относящихся к производным алифатических аминоспиртов. Они играют важную роль передаче клеточного сигнала и в клеточном распознавании. Особенно богата сфинголипидами нервная ткань. Основу сфинголипидов составляет сфингозин, связанный амидной связью с ацильной группой (например, с жирной кислотой). При этом несколько возможных радикалов связаны со сфингозином за счёт эфирной связи. Простейший представитель сфинголипидов — церамид.
Церамиды — подкласс липидных молекул, самый простой тип сфинголипидов, состоящих из сфингозина и жирной кислоты. Церамиды являются важным липидным компонентом клеточной мембраны. Церамид участвует в качестве молекулы-предшественника в синтезе сфингомиелина. Церамиды играют роль в клетке не только как элемент мембраны, но и как сигнальная молекула. Участвуют в таких клеточных процессах какклеточная дифференцировка, клеточная пролиферация и апоптоз.
Пути образования в клетке
Существует два основных пути образования церамидов: сфингомиелиназный путь и синтез de novo.
- Гидролиз сфингомиелина под действием фермента сфингомиелиназа приводит к образованию фосфохолина и церамида. Образованный таким путём церамид может служить сигнальной молекулой клеточных процессов, таких как апоптоз.
- Синтез под действием церамидсинтазы из более простых компонентов в эндоплазматическом ретикулуме, откуда церамид поступает ваппарат Гольджи, где из него синтезируются сфингомиелин или гликосфинголипиды.
Сфингомиелин — это тип сфинголипида, который находится вклеточной мембране животных. Особенно этим фосфолипидом богата миелиновая оболочка аксонов нервных клеток (отсюда и название) Сфингомиелин представляет собой единственный фосфолипид человека, основа которого не включает глицериновый остаток. Сфингомиелин состоит из сфингозина, соединённого сложноэфирной связью с полярной группой. Полярная группа может быть фосфохолин илифосфоэтаноламин. Ко второму углероду сфингозина за счёт амидной связи присоединена жирная кислота.
40. Половые гормоны можно рассматривать как производные трех углеводородов: андростана, прегнана и эстрана.
• андрогены — мужские половые гормоны, или С19-стероиды, в основе молекулы которых лежит скелет молекулы углеводорода сложного строения — андростана:

Наиболее важными андрогенами являются тестостерон, дигид-ротестостерон и андростандиол:
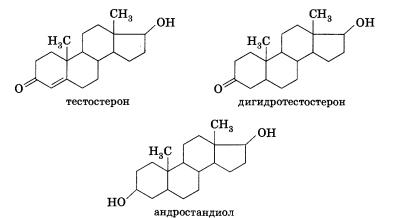
(химическое название тестостерона — 17-гидрокси-4-андростен-3-он, дигидротестостерона — 17-гидроксиандростан-З-он).
Очевидно, что тестостерон является ненасыщенным кетоно-спиртом, дигидротестостерон и андростандиол можно рассматривать как продукты его гидрирования, а принадлежность андростандиола к многоатомным спиртам и его насыщенный характер отражаются в названии;
Эстран — насыщенный тетрациклический углеводород, относящийся к группе стероидов c 18-ю углеводородными атомами.
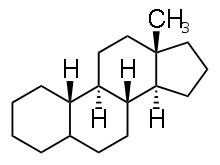

Структурная формула эстрана
В основе скелета эстрана лежит структура гонана (стерана) с метильной группой у С-13. Структура эстрана является основой для гормонов эстрогенного ряда (эстрона, эстриола, эстрадиола и др.).
Известны три естественных эстрогенных гормона: эстрадиол, эстрон (фолликулин) и эстриол.

Эстрон, эстрадиол-17β, эстриол
Эстрогенной активностью обладают многие производные естественных эстрогенных гормонов (их эфиры и ацетиленовые производные).
41. Холестери́н (холестерол) - органическое соединение, природный жирный (липофильный) спирт, содержащийся в клеточных мембранах всех живых организмов. Холестерин обеспечивает стабильность клеточных мембран в широком интервале температур. Он необходим для выработки витамина D, выработки надпочечниками различных стероидных гормонов, включая кортизол, альдостерон, женских половых гормонов эстрогенов и прогестерона, мужского полового гормона тестостерона, а по последним данным — играет важную роль в деятельности синапсовголовного мозга и иммунной системы, включая защиту от рака. Нарушение обмена холестерина приводит откладыванию его на стенках сосудов, образуя так называемые атеросклеротические бляшки. Бляшки сужают сосуды и препятствуют нормальному току крови. Это приводит к атеросклерозу.
42. Же́лчные кисло́ты (синонимы: жёлчные кислоты[1], холевые кислоты, холиевые кислоты, холеновые кислоты) — монокарбоновые гидроксикислоты из класса стероидов.
Желчные кислоты — производные холановой кислоты С23Н39СООН, отличающиеся тем, что к её кольцевой структуре присоединены гидроксильные группы.

Биологическая роль желчных кислот состоит в том, чтоэто группа стероидных кислот, содержащихся в ЖЕЛЧИ. У человека наиболее обычной является холевая кислота, С24Н40О5, карбоксильная группа которой связана с аминогруппой глицина и таурина (аминокислот). Желчные кислоты служат эмульгаторами для жиров и растворимых в жирах витаминов, тем самым облегчая их впитывание стенками внутренностей.
Практический блок
1. 
2. 
3. 
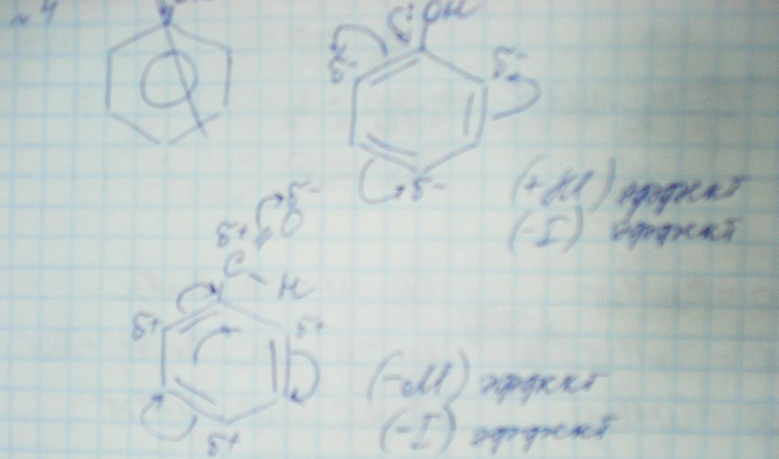
4. 
5.

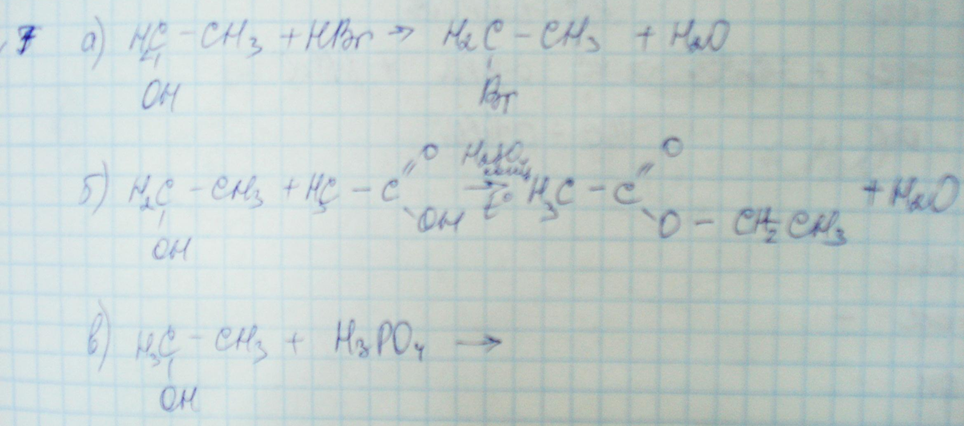

9.