 |
|
Теоретические основы метанового брожения
4.2.1.Микрофлора
Процессы, протекающие в основном в бактериальной биомассе, включают конверсию сложных органических субстратов, таких, как полисахариды, липиды и белки, в метан и диоксид углерода. Симбиотическое сообщество микроорганизмов, благодаря тому, что оно может менять используемые им пути ферментации, функционирует как саморегулирующаяся система, поддерживающая значения рН, окислительно-восстановительного потенциала и термодинамическое равновесие оптимальным для роста образом и, следовательно, обеспечивающая стабильность сбраживателя. По своим пищевым потребностям эти бактерии могут быть удобно разделены на три обширные группы. Первая включает гидролитические бактерии, обычно называемые ацидогенными, так как они обеспечивают начальный гидролиз субстрата до низкомолекулярных органических кислот и других малых молекул. Вторая группа представляет собой гетероацетогенные бактерии, которые продуцируют уксусную кислоту и водород, а третья – это метаногенные бактерии, которые продуцируют метан. Эта последняя группа может быть в дальнейшем подразделена на потребителей водорода (литотрофы) и уксусной кислоты (ацетотрофы)
Кроме состава субстрата другие условия культивирования также влияют на состав популяции в процессе смешанной ферментации. Один из таких параметров – температура. Сбраживатели могут работать при психрофильных (<20 °С), мезофильных (20 – 45 °С) или термофильных (50 – 65 °С) условиях. Термофильные сбраживатели имеют высокие скорости реакции, но часто получаемая при этом выгода недостаточно велика, чтобы возместить стоимость дополнительной тепловой энергии, необходимой для поддержания более высоких температур.
Влияние температуры, на видовой состав микрофлоры пока изучено недостаточно, хотя считается, что микрофлора мезофильного режима значительно богаче по количеству и разнообразию видов, чем микрофлора термофильных сообществ. Вместе, с тем, показано, что из общей популяции мезофильного реактора, 9 % микроорганизмов могло развиваться в термофильных условиях, а 1 % являлись облигатно термофильными. В целом же метановые бактерии в мезофильных и термофильных микробных метаногенных ассоциациях предоставлены, разными видами. Тем не менее, несмотря на это, температурный режим влияет только на скорость процесса, а не на качественный состав образующихся продуктов, способность системы адаптироваться к различным субстратам или ингибирующим соединениям.
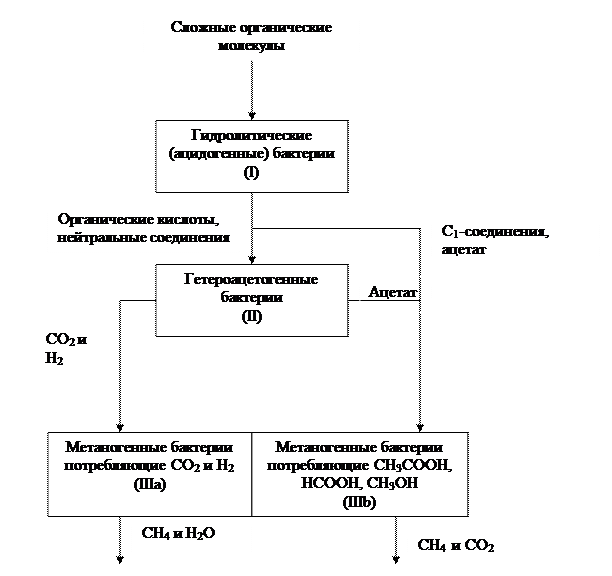
Рис. 6. Упрощенная схема утилизации органических веществ в анаэробных условиях
Поэтому большинство установок в настоящее время работает в температурном интервале 34 – 38 °С, что экономически выгодно и к тому же допускает существование большего числа видов микроорганизмов.
4.2.2. Гидролитические бактерии (I ГРУППА)
Эта функциональная группа бактерий гидролизует макромолекулы до растворимых продуктов, которые могут быть в свою очередь превращены в низкомолекулярные органические соединения.
Ниже приведены некоторые продукты анаэробного сбраживания – соединения, образующиеся в количестве больше 0,2 моль на моль субстрата в неперегруженном анаэробном сбраживателе:
органические кислоты – уксусная, пропионовая, масляная, капроновая, муравьиная, молочная, янтарная;
спирты и кетоны – метанол, этанол, изопропилоный спирт, бутанол, глицерин, ацетон;
газы – водород, метан, диоксид углерода;
ферменты – целлюлаза, алкогольдегидрогсназа;
витамины – рибофлавин, витамин B12.
Члены этой группы могут быть как облигатными, так и факультативными анаэробами. По данным литературы, субстрат включает спорулирующие и неспорулирующие грамм-положительные палочки, такие как протеолитические Eubacterium, целлюлолитические Clostridium, Acetobacterium, облигатные анаэробы, такие как Bacteroides и Bifidobacteria и факультативные анаэробы Streptococcus и Enterobacteriaceae. Гидролитические бактерии используют ряд экзоферментов, таких как протеазы, липазы, амилазы, целлюлазы и пектиназы. Эти ферменты часто видоспецифичны и могут отличаться от таковых у аэробных бактерий. Следовательно, процесс сбраживания представляет собой растворение природных субстратов, таких как белки, липиды, гомо- и гетерополисахариды.
Некоторые реакции:
С6Н12О6 + 2Н2О → 2СН3СООН + 4Н2 + 2СО2
При резком увеличении количества водорода и уксусной кислоты, включаются альтернативные пути конверсии биомассы:
С6Н12О6 + 2Н2 → 2С2Н5СООН + 2Н2О
С6Н12О6 → С3Н7СООН + 2Н2 + 2СО2
4.2.3. Гетероацетогенные бактерии (II ГРУППА)
Недавно описаны два новых вида гетероацетогенных бактерий: Synthrobacter wolinii (грамм-отрицательная палочка) и Synthrophomonas wolfii (нефототрофная бактерия). Именно эти бактерии разлагают жирные кислоты (пропионовую и масляную), некоторые спирты.
Конверсия пропионовой и масляной кислот протекает так:
С2Н5СООН + 2Н2О → CH3COOH + СО2 + ЗН2
С3Н7СООН + 2Н2О → 2СН3СООН + 2Н2.
Для конверсии пропионовой кислоты ∆G° = 48,1 кДж. Однако при низком парциальном давлении водорода эта реакция становится энергетически более выгодной. Низкое парциальное давление водорода, необходимое для биоконверсии кислот гетероацетогенными бактериями, объясняет, почему они успешно растут только при совместном культивировании с утилизирующими водород метаногенными бактериями и почему симбиоз, и межвидовой перенос водорода усиливает рост обеих трофических групп.
4.2.4.Метаногенные бактерии (III ГРУППА)
Эта трофическая группа определяется на основе специфических субстратов, используемых для образования метана. К подгруппе IIIa относятся хемолитотрофные бактерии, они превращают водород и диоксид углерода в метан, используя газообразный водород как донор электронов, в том числе водород, получаемый из воды:
СО2+4Н2 → СН4 + 2Н2О
В результате этой реакции также происходит превращение одной молекулы АДФ в АТФ, следовательно, реакция термодинамически выгодна.
Микроорганизмы второй подгруппы Шb известны как перерабатывающие уксусную и муравьиную кислоту, метанол в метан. Уравнение конверсии уксусной кисло выглядит так:
СН3СООН → СН4 + СО2
Эта реакция дает только 0,25 моль АТФ и поэтому термодинамически относительно не выгодна.
В группу входят представители родов Methanobaclerium, Methanospirillum, Methanococus, Methanosarctna и Methanothrix.
4.2.5. Некоторые сведения о метанобразующих бактериях
Предположение о биологической природе образования метана было высказано еще в XIX в. Однако изучение этого процесса и организмов, его осуществляющих, тормозилось из-за отсутствия чистых культур. Сложность заключается в чрезвычайной чувствительности большинства метанобразующих бактерий к О2. Быстрый прогресс в изучении этой группы архибактерий связан с использованием методов культивирования анаэробов, разработанных Р. Е. Хангейтом (R. E.Hungate). В качестве основных приемов используется удаление О2 из газов, в атмосфере которых осуществляются культивирование и все необходимые для работы операции, а также применение предварительно восстановленных сред.
Общая характеристика. Метанобразующие бактерии (метаногены) – морфологически разнообразная группа, объединяемая двумя общими для всех ее представителей признаками: облигатным анаэробиозом и способностью образовывать метан. Для создания таксономической структуры метанобразующих бактерий был использован филогенетический подход, основанный на сравнительном анализе нуклеотидных последовательностей 16S рРНК. В соответствии с таким подходом в девятом издании Определителя бактерий Берги группа разделена на три порядка (Methanobacteriales, Methanococcales, Methanomicrobiales), коэффициент сходства (SAB) для которых составляет 0,2 – 0,28. Далее порядки разделены на 6 семейств (SAB = 0,34 – 0,36) и 13 родов (SAB = 0,46 – 0,51). Число видов достигает более 40. SAB для них колеблется в пределах 0,55 – 0,65. О гетерогенности группы можно судить и по нуклеотидному составу ДНК ее представителей (молярное содержание ГЦ-оснований – от 27 до 61 %).
В состав группы входят бактерии с разной морфологией: прямые или изогнутые палочки разной длины; клетки неправильной формы, близкие к коккам; извитые формы. У некоторых видов наблюдается тенденция формировать нити или пакеты. Клетки неподвижные или передвигающиеся с помощью перитрихиально или полярно расположенных жгутиков. У представителей рода Methanosarcina в клетках найдены газовые вакуоли. Для некоторых метаногенов характерна развитая система внутриклеточных элементарных мембран, являющихся результатом разрастания и выпячивания в цитоплазму ЦПМ и сохраняющих с ней связь. У этой группы архебактерий обнаружены клеточные стенки трех типов: состоящие из псевдомуреина, построенные из белковых глобул и гетерополисахаридной природы. Недавно описан микоплазмоподобный метаноген, выделенный в род Methanoplasma, не имеющий клеточной стенки и фильтрующийся через мембранные фильтры с диаметром пор 0,45 мкм.
20 – 30 % мембранных липидов метаногенов представлены нейтральными и 70 – 80 % - полярными липидами. Последние – это в основном два типа простых эфиров глицерина и терпеноидных спиртов (С20-фитаниловый и С40-бифитаниловый), на основе которых образуются полярные фосфо- и гликолипиды. В зависимости от вида клеточные мембраны могут содержать оба типа эфиров или только один. Основными нейтральными липидами являются С20-, С25- и С30-ациклические изопреноидные углеводороды, насыщенные или содержащие двойные связи. Запасных продуктов в виде поли-β-оксимасляной кислоты или гликогена в клетках не обнаружено.
Метанобразующие бактерии – строгие анаэробы. Первые исследования чистых культур, выделенных из рубца жвачных животных, показали, что рост их возможен при начальном окислительно-восстановительном потенциале среды ниже -300 мВ. Рост некоторых видов полностью подавляется при содержании в газовой фазе более 0,004 % молекулярного кислорода. В последнее время, однако, описаны виды с относительно низкой чувствительностью к О2. Возможно, в природе такие виды могут сохранять жизнеспособность при кратковременных контактах с О2 и возобновлять рост в анаэробных условиях.
Большинство метанобразующих бактерий имеют температурный оптимум для роста в области 30 – 40 °С, т.е. являются мезофилами, но есть виды, у которых оптимальная зона сдвинута в сторону более низких (25 °С) или высоких (55 – 65 °С) температур. Недавно выделен экстремально термофильный организм Methanothermus fervidus, растущий при 55 – 97 °С (оптимум 80 °С). Все известные представители этой группы – нейтрофилы с оптимальным рН в области 6,5 – 7,5. Среди метаногенов есть галофилы, требующие в качестве одного из оптимальных условий для роста содержания в среде до 65 – 70 г/л NaCl.
В качестве источника углерода и энергии для роста метаногены используют узкий круг соединений. Наиболее универсальными источниками углерода и энергии для них является газовая смесь Н2 и СО2. Более 3/4 известных видов утилизируют Н2 + СО2. Некоторые метаногены приспособились к облигатному использованию этих соединений. Следующими по распространенности источниками углерода и энергии служат формиат ион, ацетат ион, метанол, метиламины и оксид углерода(II).
Около половины изученных видов не нуждаются в каких-либо органических соединениях. Для роста многих культур в атмосфере Н2 и СО2 требуется внесение в среду органических веществ, стимулирующих рост или абсолютно для него необходимых. Это могут быть некоторые витамины группы В, ацетат, пируват, сукцинат, отдельные аминокислоты, дрожжевой экстракт или компоненты неизвестного состава, содержащиеся в природных средах обитания. Так, штаммы, выделенные из рубца жвачных животных, нуждаются в добавках рубцовой жидкости. Сложные органические соединения метанобразующие бактерии использовать не могут.
В качестве источника азота метаногены используют аммонийный азот или некоторые аминокислоты. Для ряда видов показана способность к азотфиксации. Источником серы могут служить сульфаты, сульфид или серосодержащие аминокислоты.
Энергетические процессы. Как отмечалось выше, почти все метанобразующие бактерии могут получать энергию за счет окисления Н2, сопряженного с восстановлением СО2. Опытами с меченым водородом показано, что Н2 в этом процессе служит только донором электронов, а источником протонов в молекуле метана является вода.
Многие виды для получения энергии могут использовать формиат:
4НСООН → СН4 + ЗСО2 + 2Н2О
Для некоторых представителей показана способность образовывать метан при использовании метанола:
4СН3ОН → ЗСН4 + СО2 + 2Н2О,
У ряда метаногенов обнаружена способность окислять окись углерода, что также сопровождается синтезом метана:
4СО + 2Н2О → СН4 + ЗСО2
Наконец, представители нескольких родов могут использовать в качестве источника энергии и углерода ацетат:
СН3СООН → СН4 + СО2
Таким образом, акцепторами электронов (а в ряде случаев и донорами, и акцепторами) у метанобразующих бактерий является ряд одноуглеродных соединений (СО2, СО, формиат, метанол, метилированные амины) и единственное двухуглеродное соединение – ацетат.
Механизм энергетических процессов метаногенов еще не расшифрован, но общие принципиальные положения установлены. Ясно, что получение энергии, по крайней мере при окислении Н2, сопряженном с восстановлением СО2, связано с функционированием электронтранспортной системы, включающей дегидрогеназы, переносчики электронов и редуктазы, т.е. определенным видом анаэробного дыхания.