 |
|
Средняя скорость молекул
Кафедра физики
МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ЛАБОРАТОРНОЙ РАБОТЕ № 2 м.ф.
“Определение средней длины свободного пробега и эффективного диаметра молекул воздуха”.
Составили: Самсонова Н.П.,
Ярков Д.М
Тюмень, 2002 г.
№ 14. ОПРЕДЕЛЕНИЕ СРЕДНЕЙ ДЛИНЫ СВОБОДНОГО ПРОБЕГА И ЭФФЕКТИВНОГО ДИАМЕТРА МОЛЕКУЛ ВОЗДУХА.
ЦЕЛЬ РАБОТЫ: измерение средней длины свободного пробега и эффективного диаметра молекул воздуха.
ОБОРУДОВАНИЕ: сосуд с водой, капилляр, секундомер.
КРАТКАЯ ТЕОРИЯ
Согласно молекулярно - кинетической теории, хаотическое молекулярное движение является причиной наблюдаемых в газах явлений переноса: перенос энергии при выравнивании температур (теплопроводность), перенос массы при выравнивании концентраций (диффузия), перенос импульса при выравнивании скоростей (вязкость).
Хотя величины скоростей молекул относительно велики и могут достигать сотен метров в секунду, процессы переноса совершаются сравнительно медленно. Происходит это потому, что молекулы непрерывно соударяются друг с другом. Между двумя последовательными соударениями молекулы движутся прямолинейно и равномерно, проходя в среднем расстояние, называемое средней длиной свободного пробега  молекулы.
молекулы.
Столкновения молекул характеризуются эффективным диаметром. Эффективным диаметром d молекулы называется минимальное расстояние между центрами двух молекул, на которое они могут сблизиться при столкновении.
Молекулярно - кинетическая теория позволяет при помощи легко измеряемых макроскопических параметров (давления, объёма, температуры) получить интересующие нас микроскопические параметры - эффективные размеры молекул и её среднюю длину свободного пробега.
Для определения средней длины свободного пробега l молекул газа используют формулу связи коэффициента внутреннего трения (вязкости) h с  и
и  (средней арифметической скоростью молекул):
(средней арифметической скоростью молекул):
 (1)
(1)
r - плотность газа.
Из уравнения Менделеева - Клапейрона:
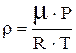 (2)
(2)
Средняя скорость молекул
 (3)
(3)
Подставляя в формулу (1) значения r и  из уравнения (2) и (3), получим:
из уравнения (2) и (3), получим:
 (4)
(4)
В данной работе для измерения  пользуются методом истечения газа через капиллярную трубку малого диаметра.
пользуются методом истечения газа через капиллярную трубку малого диаметра.
Объём V газа, протекающего через трубку с круглым внутренним сечением радиуса r за время t, определяется по формуле Паузейля:
 , (5)
, (5)
DР - разность давлений на концах капилляра, которой и обусловлено течение газа, l - длина капилляра.
Из уравнения (5) коэффициент вязкости:
 (6)
(6)
Сравнивая уравнения (4) и (6), получим следующую формулу для определения средней длины свободного пробега:
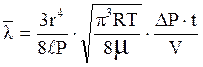 (7)
(7)
Эффективный диаметр d молекул вычисляют из формулы, выражающей его связь со средней длиной свободного пробега `l:
 , (8)
, (8)
n - число молекул газа в единице объёма при данных условиях (концентрация молекул). Из основного уравнения кинетической теории газов для величины нормального давления Р0 и давления в лаборатории, получаем равенство:
Р0 = n0kT0, (9)
Р = nkT, (10)
n0 = 2,69×1025 м-3 - число Лошмидта, т.е. число молекул газа в единице объёма при нормальных условиях (Т0 = 273К, Р0 = 101,33кПа); k --постоянная Больцмана.
Из уравнения (9) и (10) находим:
 . (11)
. (11)
Решая уравнение (8) относительно d и учитывая уравнение (11), получим:
 (12)
(12)