 |
|
Определение параметров состояния водяного пара.
Кипящая жидкость
Состоянию кипящей жидкости соответствует нижняя пограничная кривая (х=0).
Обозначим через q′ теплоту, необходимую для нагрева жидкости от 00С до tнас при Р = const.
Из общей термодинамики известна общая формула теплоемкости
 Þ q′=
Þ q′=  @
@  р tнас
р tнас
Полагая среднюю массовую изобарную теплоемкость (  р) воды в диапазоне температур 0 - tнас равной 4,19 (кДж/(кг·К)), получим
р) воды в диапазоне температур 0 - tнас равной 4,19 (кДж/(кг·К)), получим
|
, [кДж/кг]
из первого начала термодинамики: q= ΔU + A
и формулы для работы термодеформационной системы в изобарном процессе:

для нашего случая получим:
q′ = (U′ – Uo′) + P(V′ – Vo′);
Здесь: второе слагаемое – это работа расширения жидкости в случае нагрева её от 0°С до tнас при постоянном давлении:
Аp = P(V′ – Vo′),
где Vo′ и Uo′ – удельный объем и удельная внутренняя энергия жидкости при 00С.
в инженерских расчетах условились принимать внутреннюю энергию системы при t=0°С, равной нулю.
|
таким образом, при U0′ = 0 и
q′ > U′
При давлениях, не превышающих 4МПа,
|
Это приближенное равенство используется в практических расчетах.
|
(*)
2.1.1 УДЕЛЬНАЯ ЭНТАЛЬПИЯ КИПЯЩЕЙ ЖИДКОСТИ .
Из общей термодинамики
i = U + PV Þ i′ = U′ + PV′.
Подставим сюда значение U′из формулы (*) данного параграфа:
 |
i′ = q′ – PV′ + PVo′ + PV′ = q′ + PVo′, [кДж /кг]
|
,
следовательно i′>q′>U′
для практических расчетов слагаемым PV0′ пренебрегают и тогда получается приближенное соотношение:
|
.
2.1.2 УДЕЛЬНАЯ ЭНТРОПИЯ КИПЯЩЕЙ ЖИДКОСТИ (S′)
В инженерных расчетах условились принимать энтропию системы при 0°С равной нулю
ΔS = S′ – S0′, откуда S′ = S0′ + ΔS ,
Здесь S0′- удельная энтропия жидкости при 0°С
Т.к. S0′ = 0, то S′ = ΔS .
Из общей термодинамики известно соотношение :
dq = TdS Þ ΔS = 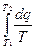 .
.
Для нашего случая: ΔS=  .
.
Подставляя в эту формулу  и интегрируя при
и интегрируя при  , получим: ΔS = 4,19ln
, получим: ΔS = 4,19ln  ,
,
|
|
 ]
]