 |
|
Формулы химических соединений, изучаемых в теме 2
Сопряженные ациклические соединения


 СН3–СН=СН – СООН
СН3–СН=СН – СООН
бутадиен-1,3 метилбутадиен-1,3 хлорэтен 2-бутеновая кислота
(изопрен) (хлорвинил) (кротоновая)
Карбоароматические соединения


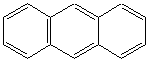

бензол нафталин антрацен фенантрен
Гетероароматические соединения





фуран тиофен пиррол имидазол индол


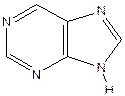
пиридин пиримидин пурин
 витамин А (ретинол)
витамин А (ретинол)
 витамин А (ретиналь)
витамин А (ретиналь)

Раздел 3 Передача электронных влияний в биоорганических соединениях. Кислотно-основные свойства биоорганических соединений.
Исходный уровень знаний для усвоения темы основан на школьной программе химии, разделах 1, 2 данного пособия и протолитической теории кислот и оснований.
Гибридизация орбиталей, пространственная ориентация орбиталей, ковалентные σ - и π – связи, полярные и неполярные ковалентные связи, изменение электроотрицательности элементов в периоде и группе, функциональные группы, сопряженные системы, делокализация.
Для усвоения темы и приобретения компетенции по данному разделу надо знать:
- определения « индуктивный», «мезомерный» эффект,
- электронные эффекты заместителей в алифатических и сопряженных системах
- диаграммы распределения электронной плотности,
- определения «кислота», «основание» по теории Бренстеда- Лоури
- влияние факторов на изменение кислотно-основных свойств.
Ключевые слова.
Заместитель донорный, акцепторный, кислота, основание, распределение электронной плотности в молекуле биоорганического соединения, сопряженная кислота, сопряженное основание, теория Бренстеда - Лоури, электроотрицательность, эффект индуктивный, мезомерный.
Содержание раздела 3
3.1. Типы химических связей в биоорганических соединениях. Механизмы смещения электронной плотности (индуктивный и мезомерный эффекты). Группы «доноры» и «акцепторы»
3.1.2. Индуктивный эффект. Сравнительная электроотрицательность атомов и элементов. Обозначение индуктивного эффeкта. Диаграммы распределения электронной плотности.
Передача индуктивного эффекта по длине углеродной цепи. Понятие а- углеродный атом рядом с акцепторной группой (карбонильной, карбоксильной).
Примеры для иллюстрации индуктивных эффектов: кислоты этановая, пропановая, бутановая, 2-гидроксипропановая, 3-гидроксипропановая. Сравнение индуктивных эффектов двух групп: амино -NH2 и положительно заряженной триметиламмонийной - +N(CH3)3 на примере
2-аминоэтанола-1 (коламина) и холина.
3.1.3.Мезомерый эффект в сопряженных системах. Донорные и акцепторные группы, знаки эффекта (± М).
3.1.3.1. Мезомерный эффект в ациклических сопряженных системах. Примеры для иллюстрации: хлорэтен (сравнить с хлорэтаном), пропеновая 2-бутеновая, 2-оксопропановая кислоты (сравнить с 2-гидроксипропановой).
3.1.3.2. Мезомерный эффект в карбоароматических соединениях. «Правило 2,4,6 ».
Примеры для иллюстрации: толуол, фенол, анилин, бензойная кислота.
3.1.3.3 Мезомерный эффект в гетероароматических соединениях.
Примеры для иллюстрации: пиридин, пиридиниевый катион, никотиновая кислота, пиримидин
Сравнение распределения электронной плотности и величин зарядов б+ в парах соединений: пиридин- пиримидин, пиридин - пиридиниевый катион,
Пиридин - никотиновая кислота, никотиновая кислота- катион никотиновой кислоты.
3.2. Кислотно - основные свойства биоорганических соединений (теория Бренстеда-Лоури). Определения кислота, сопряженное основание, основание, сопряженная кислота. Константа кислотности, основности. Значения рКа, рКв.
3.2.1. Кислотные свойства. Виды кислот (-ОН, -SH, -NН, -CH - кислоты), Факторы, влияющие на кислотные свойства:
-природа кислотного центра,
- полярность связи,
- влияние заместителей,
-поляризуемость атома (наибольшая у серы в сравнении с кислородом),
Изменение кислотных свойств в гомологических рядах.
Примеры: гомологические ряды
- спиртов: метанол, этанол, пропанол-1;
- монокарбоновых кислот: муравьиная, уксусная, пропановая и т.д.
-дикарбоновых кислот: щавелевая, малоновая, янтарная, глутаровая
Сравнение кислотных свойств
- одно – и многоатомных спиртов – этанол, глицерин
-аминоэтанола (коламина) и холина
- фенола и его производных – фенол, 4-нитрофенол, п-дигидроксибензол (гидрохинон),
- гидроксикарбоновых кислот (2-гидроксипропановая,
3-гидроксибутановая, 2-гидроксибутандиовая)
- оксокарбоновых кислот (2-оксопропановая, 3-оксобутановая, 2-оксобутандиовая)
- карбоновых кислот, гидрокси - и оксокарбоновых кислот между собой
3.2.2. Основные свойства. Факторы, влияющие на основные свойства:
- природа основного центра
- влияние заместителей
-изменение основных средств в гомологических рядах
Основные свойства азотсодержащих ароматических гетероциклических соединений и сравнение основных свойств.
Примеры:
- гомологический ряд аминов
- алифатические и ароматические амины - этиламин, анилин
- замещенные ароматические амины - анилин, 4-аминофенол
- пиридин, никотиновая кислота
- сравнение : амины, спирты, тиолы
Приложение. Основы теории.
Индуктивный и мезомерный эффекты.
Для объяснения направления и силы индуктивного эффекта надо знать ряд сравнительной электроотрицательности элементов.
Сравнительная электроотрицательность атомов и элементов:
А) С( sp3) < С( sp2 ) < С (sp)
Б) С < N < O; C < галоген (F < Cl < Br < I)