 |
|
Элементы квантовой физики атомов, молекул и твердых тел.
1. Обобщенная формула Бальмера  ,
,  - постоянная Ридберга, m=1,2,3… - определяет серию, n=m+1, m+2, m+3… - определяет отдельные линии в серии.
- постоянная Ридберга, m=1,2,3… - определяет серию, n=m+1, m+2, m+3… - определяет отдельные линии в серии.
2. Первый постулат Бора 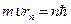 ,
,  , n=1,2,3…,
, n=1,2,3…,  - масса электрона,
- масса электрона,  - скорость электрона на n-ойорбите с радиусом
- скорость электрона на n-ойорбите с радиусом  .
.
3. Второй постулат Бора (правило частот)  .
.
4. Энергия электрона в водородоподобном атоме 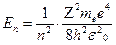 , n=1,2,3…, е=
, n=1,2,3…, е=  - заряд электрона, z- зарядовое число (порядковый номер элемента).
- заряд электрона, z- зарядовое число (порядковый номер элемента).
5. Длина волны де Бройля  .
.
6. Соотношение неопределенностей  ,
,  .
.
7. Вероятность нахождения частицы в элементе объема dV  ,
, 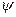 - волновая функция,
- волновая функция,  ,
,  - функция комплексно сопряженная
- функция комплексно сопряженная 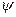 .
.
8. Условие нормировки вероятностей  .
.
9. Общее уравнение Шредингера  ,
,  , U-потенциальная энергия частицыв силовом поле.
, U-потенциальная энергия частицыв силовом поле.
10. Уравнение Шредингера для стационарных состояний  . E – полная энергия частицы.
. E – полная энергия частицы.
Элементы физики атомного ядра и элементарных частиц.
1. Радиус ядра 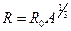 .
.  , А- массовое число.
, А- массовое число.
2. Энергия связи нуклонов в ядре  .
.
3. Дефект массы ядра  Zmp + (A – Zmn) –mя ,
Zmp + (A – Zmn) –mя ,  и
и  - массы протона, нейтрона и ядра.
- массы протона, нейтрона и ядра.
4. Магнетон Бора  .
.
5. Закон радиоактивного распада  ,
, 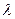 - постоянная радиоактивного распада.
- постоянная радиоактивного распада.
6. Период полураспада  .
.
7. Среднее время жизни радиоактивного ядра  .
.
8. Активность нуклида 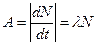 .
.
9. Правило смещения для  распада
распада 
 .
.
10. Правило смещения для  - распада
- распада 
 .
.
11. Правило смещения для 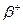 - распада
- распада 
 .
.
12. Символическая запись ядерной реакции  или X(a,b)Y.
или X(a,b)Y.
Примеры решения задач.
Задача 1
Красная граница фотоэффекта для некоторого металла равна 0,5 мкм. При какой частоте света оторвавшиеся с его поверхности электроны полностью задерживаются обратным потенциалом в 3В? Заряд электрона принять равным 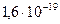 Кл; постоянная Планка
Кл; постоянная Планка  Дж с; скорость света
Дж с; скорость света  м/с
м/с
Решение.
Основным расчетным соотношением для решения задачи служит выражение закона сохранения энергии. Действительно, чтобы задержать вылетающие электроны, необходимо приложить задерживающееэлектрическое поле, причем вылет электронов прекратиться, очевидно, когда потенциальная энергия электрона в задерживающем поле, равная Е  , станет равной его кинетической энергии Е
, станет равной его кинетической энергии Е  , поэтому
, поэтому 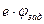 =
=  . Кинетическая энергия электрона входит в выражение закона сохранения энергии для явления фотоэффекта, где этот закон записывается в виде формулы Эйнштейна:
. Кинетическая энергия электрона входит в выражение закона сохранения энергии для явления фотоэффекта, где этот закон записывается в виде формулы Эйнштейна:  , в этом уравнении
, в этом уравнении  - энергия фотона, А- работа выхода электрона из металла. Из двух вышеприведенных уравнений имеем:
- энергия фотона, А- работа выхода электрона из металла. Из двух вышеприведенных уравнений имеем:
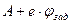 =
=  , откуда
, откуда 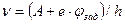 . Неизвестна работа выхода электрона из металла, которую можно найти из следующих рассуждений: явление фотоэффекта наблюдается только при облучении металла с частотой, не меньшей частоты красной границы фотоэффекта
. Неизвестна работа выхода электрона из металла, которую можно найти из следующих рассуждений: явление фотоэффекта наблюдается только при облучении металла с частотой, не меньшей частоты красной границы фотоэффекта 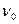 . Воспользуемся заданной в условии задачи красной границей фотоэффекта; учитывая, что частота связана с длиной волны соотношением
. Воспользуемся заданной в условии задачи красной границей фотоэффекта; учитывая, что частота связана с длиной волны соотношением  , где с- скорость света, и полагая, что красная граница фотоэффекта соответствует энергии фотонов, при которых скорость вырываемых с металла электронов равна нулю, получим из уравнения :
, где с- скорость света, и полагая, что красная граница фотоэффекта соответствует энергии фотонов, при которых скорость вырываемых с металла электронов равна нулю, получим из уравнения :  . Тогда:
. Тогда:  .
. 
Ответ: 
Задача 2.
Вычислить полную энергию Е, линейную скорость υ и период Т электрона, находящегося на первой (n=1) боровской орбите атома водорода. Масса покоя электрона m 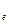 =9,1*10
=9,1*10  кг, его заряд e=1,6*10
кг, его заряд e=1,6*10  Кл.
Кл.
Решение:
Полную энергию электрона в атоме водорода на его первой стационарной орбите, можно определить по формуле: Е= -  .Кинетическая энергия электрона на стационарной орбите определяется классической формулой: W
.Кинетическая энергия электрона на стационарной орбите определяется классической формулой: W  =
=  . Потенциальная энергия электрона на орбите определяется произведением заряда электрона e на потенциал ядра
. Потенциальная энергия электрона на орбите определяется произведением заряда электрона e на потенциал ядра 
 : W
: W  =e∙ φ
=e∙ φ  , где
, где 
 =
=  , отсюда потенциальная энергия: W
, отсюда потенциальная энергия: W  = -
= -  . Знак «-» учитывает, что взаимодействующие протон ядра и электрон имеют противоположные знаки. Тогда полная энергия электрона Е будет равна: E =
. Знак «-» учитывает, что взаимодействующие протон ядра и электрон имеют противоположные знаки. Тогда полная энергия электрона Е будет равна: E =  Радиус первой боровской орбиты определяется ее номером n = 1 согласно выражению
Радиус первой боровской орбиты определяется ее номером n = 1 согласно выражению  r =
r =  , тогда Е =
, тогда Е =  =
=  или
или  . После преобразований получим формулу для определения линейной скорости движения электрона по орбите:
. После преобразований получим формулу для определения линейной скорости движения электрона по орбите:  , Период вращения электрона связан с линейной скоростью отношением:
, Период вращения электрона связан с линейной скоростью отношением:  , где
, где  и r=
и r=  . Следовательно: Т=
. Следовательно: Т=  .
.
[E] = 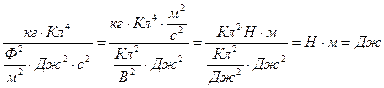
[  ] =
] = 
[Т]=  . Подставляя численные значения, имеем: Е =
. Подставляя численные значения, имеем: Е =  ;
;  =
=  ; Т =
; Т =  .
.
Ответ: Е = - 2,2*10  Дж; ,
Дж; ,  = 2,2*10
= 2,2*10 
 ; Т = 1,4*10
; Т = 1,4*10  с.
с.
Задача 3.
Определить радиус атома водорода, в котором электрон находится на ближайшей к ядру орбите. Определить скорость движения электрона по этой орбите.
Решение.
Ядро атома водорода (протон) и вращающийся вокруг него электрон взаимодействуют по закону Кулона с силой F=  , где е – элементарный электрический заряд. Эта сила и является центростремительной, заставляющей электрон вращаться по орбите с радиусом r
, где е – элементарный электрический заряд. Эта сила и является центростремительной, заставляющей электрон вращаться по орбите с радиусом r  ,то есть
,то есть  =
=  . Согласно постулату Бора электрон может двигаться только по тем орбитам, для которых импульс электрона
. Согласно постулату Бора электрон может двигаться только по тем орбитам, для которых импульс электрона  кратен числу
кратен числу  (квантование орбит Бора), т.е.
(квантование орбит Бора), т.е.  =
=  , где k-целое число. Для ближайшей к ядру орбиты k=1. Следовательно,
, где k-целое число. Для ближайшей к ядру орбиты k=1. Следовательно,  =
=  . Из этого уравнения находим
. Из этого уравнения находим 
 и подставляем его значение в первое уравнение, а затем вычисляем радиус орбиты r
и подставляем его значение в первое уравнение, а затем вычисляем радиус орбиты r  и скорость
и скорость 
 :
:

 =
=  ,
,  =
= 
 ,
,  ,
,  , подставляя численные значения, получим r
, подставляя численные значения, получим r  =
=  м,
м,
тогда 
 =
=  м/с.
м/с.
Ответ: r  =
=  м,
м, 
 =
=  м/с.
м/с.
Задача 4.
При облучении атомов водорода квантами монохроматического светаэлектрон перешел с первой стационарной орбиты ( n  = 1) на третью (n
= 1) на третью (n  = 3), а при возвращении в исходное состояние он перешел сначала с третьей орбиты на вторую (n
= 3), а при возвращении в исходное состояние он перешел сначала с третьей орбиты на вторую (n  =2), а затем со второй на первую. Определить энергии квантов излученных и поглощенных при переходах.
=2), а затем со второй на первую. Определить энергии квантов излученных и поглощенных при переходах.
Решение
Разобьем задачу на три процесса: переход электрона с первой орбиты на третью, с третьей – на вторую и со второй орбиты на первую: Е  = h
= h  , где n – номер перехода.
, где n – номер перехода.
n  ,n
,n  ,n
,n  - номера энергетических уровней, с которых и на которые переходил электрон при переходе атома в возбужденные и основное состояния. Е
- номера энергетических уровней, с которых и на которые переходил электрон при переходе атома в возбужденные и основное состояния. Е  - энергия кванта поглощенная атомом при переходе электрона с первой стационарной орбиты на третью, Е
- энергия кванта поглощенная атомом при переходе электрона с первой стационарной орбиты на третью, Е  - энергия кванта, излученного атомом при переходе электрона с третьей орбиты на вторую, Е
- энергия кванта, излученного атомом при переходе электрона с третьей орбиты на вторую, Е  - энергия кванта, излученная атомом при переходе электрона со второй орбиты на первую.
- энергия кванта, излученная атомом при переходе электрона со второй орбиты на первую.  ;
;  ;
;  , где R – постоянная Ридберга, R=
, где R – постоянная Ридберга, R=  . Подставляем полученные формулы, в формулу для определения энергии: Е
. Подставляем полученные формулы, в формулу для определения энергии: Е  = h
= h  , Е
, Е  =h
=h  , Е
, Е  = h
= h  ,[E] =
,[E] = 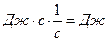 .
.
Е  =
=  Дж; Е
Дж; Е  =
=  Дж; Е
Дж; Е  =
=  Дж.
Дж.
Ответ: Е  =
=  Дж; Е
Дж; Е  =
=  Дж; Е
Дж; Е  =
=  Дж.
Дж.
Задача 5.
Найти удельную энергию связи  ядра
ядра 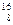 О.
О.
Решение:
А-массовое число элемента, Z- его зарядовое число, m 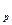 - масса одного протона, m
- масса одного протона, m  -масса одного нейтрона, M
-масса одного нейтрона, M  - масса ядра кислорода,
- масса ядра кислорода,  - удельная энергия связи ядра кислорода. Удельная энергия связи ядра может быть определена
- удельная энергия связи ядра кислорода. Удельная энергия связи ядра может быть определена
отношением всей энергии связи  , то есть энергией связи, приходящейся на все нуклоны ядра, к их общему числу, то есть массовому числу А,
, то есть энергией связи, приходящейся на все нуклоны ядра, к их общему числу, то есть массовому числу А,
 =
=  . Энергию связи ядра
. Энергию связи ядра  можно определить по формуле:
можно определить по формуле:
 =
=  МэВ. Здесь N=A-Z – число нейтронов в ядре(массы протонов, электронов и нейтронов следует оставить в атомных единицах массы – а.е.м., тогда энергия будет выражена в мегаэлектронвольтах - МэВ).
МэВ. Здесь N=A-Z – число нейтронов в ядре(массы протонов, электронов и нейтронов следует оставить в атомных единицах массы – а.е.м., тогда энергия будет выражена в мегаэлектронвольтах - МэВ).
Тогда общая формула для определения удельной энергии связи ядра будет иметь вид:  =
=  /А. Подставив численные значения, получим следующий результат:
/А. Подставив численные значения, получим следующий результат:  =8,2
=8,2 
Ответ:  =8,2
=8,2 
Задача 6.
Какая доля радиоактивных ядер некоторого элемента распадается за время t, равное половине периода полураспада?
Решение:
В задаче 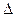 N – количество ядер, распавшихся за время t, N0 – первоначальное количество ядер (то есть в момент t=0), Т – период полураспада элемента. Количество ядер
N – количество ядер, распавшихся за время t, N0 – первоначальное количество ядер (то есть в момент t=0), Т – период полураспада элемента. Количество ядер 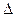 N, распавшихся за время t=
N, распавшихся за время t= 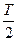 равно разности первоначального количества ядер N0 и количества N, оставшихся нераспавшимися ядер за время t от начала отсчета времени распада,
равно разности первоначального количества ядер N0 и количества N, оставшихся нераспавшимися ядер за время t от начала отсчета времени распада,  . Количество нераспавшихся ядер, время распада и период полураспада связаны соотношением (закон радиоактивного распада):
. Количество нераспавшихся ядер, время распада и период полураспада связаны соотношением (закон радиоактивного распада):  ,
,
где t = 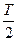 , с учетом этого имеем:
, с учетом этого имеем: 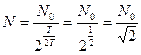 , тогда количество распавшихся ядер
, тогда количество распавшихся ядер 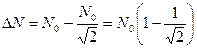 , найдем отношением
, найдем отношением  ,
,  Доля распавшихся ядер за время, равное половине периода полураспада, 0,29 или в процентном отношении 29% от начального числа ядер.
Доля распавшихся ядер за время, равное половине периода полураспада, 0,29 или в процентном отношении 29% от начального числа ядер.
Ответ: 0,29.