 |
|
Номенклатурасы, стереоизомериясы. 5 страница
Заттың химиялық реакцияға қатысу қабілетін және әрекеттесу жылдамдығын оның реакциялық қабілеті деп атайды. Субстраттың реакциялық орталығына неғұрлым зарядтың шамасы көп болса, солғұрлым реакция тез жүреді, яғни оның реакциялық қабілеті жоғары болады.
КӨРНЕКТІ материал: слайдтар, кестелер, схемалар.
ӘДЕБИЕТТЕР:
Негізгі:
1. Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. - М., 2006. – С. 24-47, 85-99.
2. Асанбаева Р.Д. Учебно-методическое пособие по биоорганической химии для самостоятельной работы студентов 1-го курса. - Алматы. 2004.– С. 17-25.
3. Асанбаева Р.Д., Салыкова Ш.Г. Практикум по биоорганической химии. -Алматы. 2003.– 47 с.
4. Асанбаева Р.Д., Илиясова М.И., Салыкова Ш.Г. Методическое пособие по биоорганической химии для самостоятельной работы студентов 1 курса лечебного, педиатрического санитарно – гигиенического и стоматологического факультетов. - Алматы. 2003.– 50 с.
Қосымша:
1. Иванов В.Г. и др. Органическая химия, М., 2005.
2. Ч Райлс А. и др. Основы органической химии, М.,1983.
3. Степаненко Б.Н. Курс органической химии, М., 1981.
4. Артеменко А.Н. Органическая химия. Теоретические основы, углубленный курс. М., 1997.
5. Шабаров Ю.Ф. Органическая химия: учебник для ВУЗов. М., 1996., т 1-2.
Лекция №5
Тема: Гетерофункциональные соединения, участвующие в процессах жизнедеятельности
План лекции:
1. Пиримидиновые и пуриновые основания, строение, таутомерия.
2. Нуклеозиды, нуклеотиды и их производные, значение.
3. Нуклеиновые кислоты. Первичная структура РНК и ДНК, понятие. Биологическоезначениенуклеиновыхкислот.
Цель:
1. Формировать знания об особенностях строения и значения различных представителей нуклеозидов, нуклеотидов и их производных.
2. Формироватьзнания принципов структурной организации ДНК и РНК.
Тезисы лекции:
Нуклеиновые кислоты играют важную роль в передаче информации, наследственных признаков, и биосинтезе белка.
Это высокомолекулярные органическое соединения, при гидролизе которых образуются пуриновые(аденин и гуанин) или пиримидиновые основания(урацил, тимин, цитозин), пентозы (рибоза или дезоксирибоза), фосфорные кислоты.
Пуриновые или пиримидиновые основания с первым углеродным атомом β-рибофуранозы или β-дезоксирибофуранозы, связанные N -гликозидной связью, образуют нуклеозиды, которые находятся в своей лактамной форме.
Нуклеозиды, соединяясь с фосфорной кислотой сложно–эфирной связью, образуют нуклеотиды или нуклеозидфосфорные кислоты. Их ещё называют мононуклеотиды, т.к. они являются мономерами полинуклеотидных цепей нуклеиновых кислот. Фосфорная кислота в нуклеотидах соединена сложно – эфирной связью с одной из гидроксильной групп пентозы, чаще всего с ОН – группой у пятого углерода.В зависимости содержат ли Д-рибозу или же Д-дезоксирибозу они являются соответственно рибонуклеотиды или дезоксирибонуклеотиды.
Нуклеотиды образуют богатые энергией производные нуклеозиддифосфаты, нуклеозидтрифосфаты - являются источниками энергии в организме, особенно АТФ. При разрыве макроэргической связи освобождается энергии в 3 раза больше, чем при разрыве обычной сложно-эфирной связи. Нуклеотиды и их производные могут являться коферментами или входят в состав коферментов. Так, например, они входят в состав коферментаА и коферментов окислительно-восстановительных ферментов: НАД+ (никотинамидадениндинуклеотид) и НАДФ (никотинамидадениндинуклеотидфосфат).Большую роль играют циклические формы нуклеотидов, в частности циклическая АМФ, которая участвует в механизме действия гормонов.
Нуклеотиды являются мономерами нуклеиновых кислот. Нуклеиновые кислоты являются полинуклеотидами. Различают рибонуклеиновые кислоты (РНК) и дезоксирибонуклеиновые кислоты (ДНК). РНК состоит из одной полинуклеотидной цепи, состоящей из рибонуклеотидов. ДНК состоит из двух полинуклеотидных цепей, состоящих из дезоксирибонуклеотидов. В полинуклеотидной цепи нуклеотиды соединяются между собой 3/, 5/-фосфодиэфирной связью. Это прочная ковалентная связь, которая обеспечивает первичную структуру нуклеиновых кислот. Первичная структура нуклеиновых кислот – это порядок, последовательность расположения нуклеотидов в полинуклеотидной цепи. Для нуклеиновых кислот характерна вторичная, третичная и четвертичная структуры.
Иллюстративный материал:слайды, таблицы, схемы.
Литература:
Основная:
1. Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. - М., 2006. – С. 179-181, 420-444.
2. Асанбаева Р.Д., ИлиясоваМ.И.Теоретические основы строения и реакционной способности биологически важных органических соединений.- Алматы, 2003.– 90с.
3. Асанбаева Р.Д., Салыкова Ш.Г. Практикум по биоорганической химии. – Алматы, 2003.–47 с.
4. Асанбаева Р.Д., Илиясова М.И., Салыкова Ш.Г. Методическое пособие по биоорганической химии для самостоятельной работы студентов 1 курса лечебного, педиатрического санитарно – гигиенического и стоматологического факультетов. - Алматы, 2003.– 50 с.
Дополнительная:
1. Иванов В.Г. и др. Органическая химия, М., 2005.
2. Райлс А. и др. Основы органической химии, М.,1983.
3. Степаненко Б.Н. Курс органической химии, М., 1981.
4. Артеменко А.Н. Органическая химия. Теоретические основы, углубленный курс. М., 1997.
5. Шабаров Ю.Ф. Органическая химия: учебник для ВУЗов. М., 1996., т 1-2.
Контрольные вопросы:
1. В каких таутомерных формах участвуют пиримидиновые и пуриновые основания в образовании нуклеотидов и почему?
2. Характер связи нуклеинового основания с углеводным остатком. Конфигурация гликозидного центра.
3. Строение нуклеотидов. Макроэргические связи. Значение.
4. Циклические формы нуклеотидов, значение.
5. Как соединяются мононуклеотиды в полинуклеотидной цепи? Характер связи между нуклеотидными остатками в полинуклеотидной цепи.
6. Виды нуклеиновых кислот. Значение. Чем отличается состав ДНК от РНК?
САБАҚТАРҒА АРНАЛҒАН ӘДІСТЕМЕЛІК ҰСЫНЫСТАР
(практикалық, семинар, лабораториялық)
| Пән аты – химия, Him 1111 | |
| Мамандық – 5В130100 – «Жалпы медицина» | |
| Кафедра - биохимия | |
| Құрастырғандар: | |
| 1 кредит (бейорганикалық химия) | доцент, х.ғ.к. Нечепуренко Е.В. |
| 2 кредит (органикалық химия) | доцент, х.ғ.к. Алмабекова А.А. |
| оқытушы Қағазбекова Г.А. | |
Алматы, 2014 ж
Сабақтарға арналған әдістемелік ұсыныстар (практикалық, семинар, лабораториялық) жұмыс бағдарламасына сәйкес құрастырылған.
Химия кафедрасының мәжілісінде қарастырылды « »2014 ж., хаттама №1.
Кафедра меңгерушісі, профессор_____________________ Н.У. Алиев
№1 Тәжірибелік сабақ
ТАҚЫРЫБЫ: Химиялық реакциялар термодинамикасы мен кинетикасының негіздері. Бейтараптау реакциясының түзілу жылуын тәжірибелік жорлмен анықтау. Химиялық реакция жылдамдығына түрлі факторлардың әсері.
МАҚСАТТАРЫ:
· Химиялық термодинамика мен кинетиканыңі негізгі түсініктерін қалыптастыру;
· бейтараптау реакциясы мысалында химиялық реакцияның түзілу жылуын тәжірибелік жолмен анықтауды үйрету;
· химиялық реакция жылдамдығына түрлі факторлардың әсерін тәжірибелік жолмен дәлелдеу;
· химиялық тәжірибенің жүргізілу принциптері мен оның нәтижелерін талдауға дағдыландыру;
· құқықтық құзыреттілікті қалыптастыру.
ОҚЫТУ МІНДЕТТЕРІ:
· химиялық термодинамика мен кинетиканың негізгі түсініктері жайлы ақпарат беру;
· нақты есептерді шығаруда қажет болатын әртүрлі термодинамикалық параметрлердің стандартты шамасын табу үшін анықтамалық әдебиетпен жұмыс істей білуге үйрету;
· бейтараптау реакциясының түзілу жылуын тәжірибелік жолмен анықтай білуге, реакцияның стандартты энтальпиясын есептей білуге және оны анықтамалық мәнімен салыстыра білуге үйрету;
· жүргізілген тәжірибелер нәтижесінде химиялық реакция жылдамдығына температура мен әрекеттесуші заттар концентрациясының әсерін сипаттай білуге үйрету;
ТАҚЫРЫПТЫҢ НЕГІЗГІ СҰРАҚТАРЫ:
1. Химиялық лабораториядағы техника қауіпсіздігі.
2. Химиялық термодинамиканың негізгі түсініктері.
3. Реакцияның стандартты жылуын тәжірибелік жолмен анықтау.
4. Химиялық реакция жылдамдығы. Массалар әрекеттесуші заңы. Вант-Гофф ережесі.
5. Химиялық реакция жылдамдығына түрлі факторлардың әсерін тәжірибелік жолмен дәлеледеу және реакция ретін анықтау.
ОҚЫТУ әдістері:
Үйлескен түрде:
- материалды мәселелік түрде баяндау (студенттерде гипотезаларды ұсыну, алдын-ала қорытындылар және ойларын түйіндей білуді дамыту);
- әңгімелесу (құқықтық компетенцияны қалыптастыру мақсатында пәннің саясатын және техника қауіпсіздігінің ережелерін бірге талқылау);
- шағын топтарда жұмыс жасау (лабораториялық жұмыс жасау және оның нәтижелерін талдау).
САБАҚТЫҢ ХРОНОМЕТРАЖЫНА МЫСАЛ
| Кіріспе бөлім (ұйымдастыру моменті) | 5 мин | |
| Пән саясатын баяндау және талқылау | 5 мин | |
| Техника қауіпсіздігінің ережелерімен таныстыру | 10 мин | |
| Материалды мәселелік баяндау және пікірталас | 20 мин | |
| Лаборияториялық жұмысты теориялық тұрғыдан талқылау | 10 мин | |
| ҮЗІЛІС | 10 мин | |
| Лабораториялық жұмысты орындау және талқылау | 25 мин | |
| Жазбаша бақылау | 20 мин | |
| Сабақты қорытындылау | 5 мин |
БАҚЫЛАУ
Бағаланатын құзыреттіліктер:
1) Құқықтық құзыреттілік
2) Білім.
Бақылау әдістері:
1) Құқықтық компетенцияны бағалау үшін тест тапсырмаларын орындау;
2)Тест тапсырмаларын немесе бақылау карталарын орындау
Бақылау сұрақтары:
1. Термодинамикалық жүйенің параметрлері: негізгі, күй функциялары (ішкі энергия, энтальпия, энтропия, изобаралық-изотермиялық потенциал), экстенсивті, интенсивті.
2. Термохимия. Химиялық реакцияның жылу эффектісі. Термохимиялық теңдеулер. Мысалдар келтіріңіздер. Стандартты түзілу жылуы, стандартты жану жылуы, стандартты бейтараптану жылуы.
3. Химиялық реакция жылдамдығы деген түсінікке анықтама беріңіз. Реакцияның орташа және шынайы жылдамдығы арасындағы айырмашылықты көрсетіңіз. Химиялық реакция жылдамдығы қандай өлшем бірлігімен өлшенеді?
4. Химиялық реакция жылдамдығына әрекеттесуші заттар концентрациясы қалай әсер етеді? Массалар әрекеттесуші заңы. Химиялық реакция жылдамдығының тұрақтысының физикалық мәнін сипаттаңыз.
5. Әрекеттесуші заттар табиғатының химиялық реакция жылдамдығына әсері. Химиялық реакция жылдамдығына катализатордың қатысы қалай әсер етеді? Активтендіру энергиясын қалай түсінесіз?
6. Химиялық реакция жылдамдығына температураның әсері. Вант-Гофф ережесі.
Әдебиет:
Негізгі:
1. Сейтембетов Т.С. Химия.- Алматы, 1994.- 23-37 б.
2. Равич-Щербо М.И., Новиков В.В. Физическая и коллоидная химия.- М., 2001.-101-131 б.
3. Ленский А.С.Введение в бионеорганическую и биофизическую химию.- М.: ВШ, 1989.- 55-92 б.
4. Веренцова Л.Г., Нечепуренко Е.В., Батырбаева А.Ә., Карлова Э.К. Бейорганикалық, физикалық және коллоидты химия: оқу құралы -29-47 б.
5. Есімжан А.Е. Жалпы химия практикумы- Алматы, 2004.- 102-120 б.
6. Рубина Х.М. и др. Практикум по физической и коллоидной химии. – М., 2001. – 71-89 б.
Қосымша:
1. Ершов Ю.А. и др. Общая химия. Биофизическая химия. Химия биогенных элементов.- М.: ВШ, 2003.- 391-422 б.
2. Слесарев В.И. Химия. Основы химии живого. - СПб.: Химиздат, 2001.- 96-123 б.
3. Ленский А.С., Белавин И.Ю., Быликин С.Ю. Биофизическая и бионеорганическая химия: медициналық ЖОО-на арналған оқу құралы.- М.:ООО «медицинское информационное агентство», 2008.- 174-178, 182-207 б.
4. Зеленин К.Н., Алексеев В.В. Химия.- С.-Пб.: ЭЛБИ-СПб, 2003.- 107-124 б.
5. Попков В.А., Пузаков С.А. Общая химия: құрал.- М.: ГЭОТАР-Медия, 2009.- 200-239 б.
6. Евстратова К.И. и др. Физическая и коллоидная химия. – М.: ВШ, 1990. - 260-302 б.
7. Бірімжанов Б.А. Жалпы химия: ЖОО-на арналған оқу құралы– Алматы.:Білім, 2001.
ҚОСЫМША
Лабораториялық жұмыс «Бейтараптау жылуын анықтау»
Жұмыстың мақсаты: Күшті қышқылдың бейтараптау жылуын күшті негіз арқылы тәжірибелік жолмен анықтау
Жұмыстың жүргізілуі:
| Реакцияның жылу эффектісін өлшеу үшін бірінің ішіне бірі салынған екі стаканнан тұратын қарапайым калориметрді қолданады. Жылу сыртқа кетпеу үшін екі стаканның арасына жылылықты сақтап тұратын материал (пенопласт) салынды. Сыртқы стакан термометр, былғауыш және құйғышқа арналған арнайы тесігі бар қақпақпен жабылады. Сол тесік арқылы стаканға әрекеттесуші заттар құйылады. Калориметрдің ішкі стаканына бюреткадан 50 мл натрий гидроксидінің эквивалентінің молярлық концентрациясы 1 моль/л-ге тең (0,05 моль NaOH) ерітіндісін құяды. Екінші бір стаканға 50 мл тұз қышқылының эквивалентінің молярлық концентрациясы 1 моль/л-ге тең (0,05 моль НС1) ерітіндісін құяды. Қышқылдың ТҚ және сілтінің ТС температурасын анықтайды, сонан соң құйғыш арқылы қышқыл ерітіндісін сілті ерітіндісіне жылдам құяды. Ерітіндіні былғауышпен араластыра отырып, оның ең жоғарғы температурасын өлшейді Т2. Алынған мәліметтерді кестеге жазады. | |||||
| Өлшенген және есептелген мәндер | Әрекеттесуші заттар | |||||
| HCl + NaOH | HNO3 + KOH | |||||
| HCl | NaOH | HNO3 | KOH | |||
| Ерітінділер концентрациясы С, моль/л | ||||||
| Ерітінділер көлемі V, л | ||||||
| Зат мөлшері n, моль n = C .V | ||||||
| Ерітінді температурасы (Т Қ және ТС) | ||||||
| Бастапқы өлшеулердің орташа температурасы (Т1) T1 = (ТҚ + ТС)/2 | ||||||
| Бейтараптанғаннан кейінгі ең жоғарғы температура (Т2) | ||||||
| Температуралар айырымы ΔТ ΔТ = Т2 – Т1 | ||||||
Калориметрлік стакандағы ерітінді массасын келесі формула бойынша анықтайды:  , мұндағы Vер-ді – бейтараптанғаннан кейінгі ерітінді көлемі (VС + VҚ), мл; сұйылтылған ерітінді тығыздығы 1 г/мл-ге тең деп алынады. Бейтараптау реакциясының түзілу жылуын келесі формула бойынша есептейді:
, мұндағы Vер-ді – бейтараптанғаннан кейінгі ерітінді көлемі (VС + VҚ), мл; сұйылтылған ерітінді тығыздығы 1 г/мл-ге тең деп алынады. Бейтараптау реакциясының түзілу жылуын келесі формула бойынша есептейді:  , Дж
, Дж
Сонымен, Q1 – бұл реакция барысында түзілген жылу мөлшері.
Бейтараптау реакциясының меншікті жылуын есептеу үшін реакция барысында түзілген жылу мөлшерін әрекеттесуші қышқыл немесе сілтінің 1 молі үшін қайта есептеу керек, өйткені ол түзілген судың 1 моліне сәйкес келеді:  , Дж/моль.
, Дж/моль.
Түзілген бейтараптау жылуын теория жүзіндегі мәнімен салыстырып, тәжірибенің абсолюттік және меншікті қатесін есептеңіз. Қатенің себептерін түсіндіріңіз.
Қорытынды: Бейтараптау реакциясының түзілу жылуын анықтаңыз, тәжірибенің абсолюттік және меншікті қатесін есептеңіз.
Лабораториялық жұмыс «Реакция жылдамдығының әр түрлі факторларға тәуелділігін зерттеу»
1-ші тәжірибе.«Реакция жылдамдығының әрекеттесуші заттардың концентрациясына тәуелділігі»
Жұмыстың мақсаты: Реакция жылдамдығының әрекеттесуші заттардың концентрациясына тәуелділігін натрий тиосульфаты мен күкірт қышқылының арасындағы реакция арқылы зерттеу.
Na2S2O3 + H2SO4 = S↓ + Na2SO4 + H2O
Жұмыстың жүргізілуі: Нөмірленген үш пробиркаға натрий тиосульфатының 1М ерітіндісін құяды: біріншісіне – 7 тамшы, екіншісіне – 14 тамшы, үшіншісіне – 21 тамшы. Бірінші пробиркаға 14 тамшы су, ал екінші пробиркаға 7 тамшы су тамызады. Басқа үш пробиркаға 7 тамшыдан күкірт қышқылын тамызады.
Реакция жылдамдығын анықтау үшін натрий тиосульфаты мен қышқыл құйғаннан бастап ақ түсті лай пайда болғанға дейінгі уақытты (күкірттің пайда болу белгісі) секундомердің көмегімен анықтайды. Натрий тиосульфаты құйылған басқа пробиркаларға да алдын-ала дайындалған (7 тамшы) күкірт қышқылының ерітіндісін құйып, ақ түсті лай пайда болғанға дейінгі уақытты анықтайды. Алынған мәліметтерді кестеге жазады.:
| Пробирка № | Ерітінді көлемі (тамшылар) | Ерітіндінің жалпы көлемі (тамшы) | Натрий тиосульфатының меншікті концентрациясы (C) | Ақ түсті лайдың пайда болу уақыты t, с | Реакцияның меншікті жылдамдығы w=1/t (с-1) | ||
| Na2S2O3 | H2O | H2SO4 | |||||
| - |
Реакцияның меншікті жылдамдығын уақытқа кері шама ретінде анықтайды. (w=1/t). Тәжірибе нәтижесінде реакция меншікті жылдамдығының натрий тиосульфатының меншікті концентрациясына тәуелділік графигін тұрғызады (абцисса осінде концентрация, ордината осінде – реакция жылдамдығы).
Қорытынды: Әрекеттесуші заттар концентрациясының реакция жылдамдығына тәуелділігін сипаттаңыз. Натрий тиосульфаты бойынша реакцияның ретін анықтаңыз
2-ші тәжірибе.«Химиялық реакция жылдамдығының температураға тәуелділігі»
Жұмыстың мақсаты: Химиялық реакция жылдамдығының температураға тәуелділігін зерттеу.
Зерттелетін реакция:
Na2S2O3 + H2SO4 = S↓ + Na2SO4 + H2O
Жұмыстың жүргізілуі: Нөмірленген үш пробиркаға натрий тиосульфатының 1М ерітіндісін 10 тамшыдан құяды. Басқа үш пробиркаға 10 тамшыдан күкірт қышқылының 1М ерітіндісін құяды.
Бірінші жұп пробиркаларды (күкірт қышқылы – натрий тиосульфаты) және термометрді бөлме температурасындағы су құйылған стаканға салып, 5 минуттан соң пробиркалардағы температура теңескенде термометр көрсеткіштерін жазады. Пробиркаларды бір-біріне құйып араластырады да, құйғаннан бастап лай пайда болғанға дейінгі уақытты санайды.
Пробиркалардың екінші жұбын бөлме температурасынан 10 градусқа, ал үшінші жұбын 20 градусқа жоғары су құйылған стаканға 5 минутқа салады. Температура теңескеннен кейін пробиркалардағы ерітінділерді бір-біріне құйып араластырады да, бірінші тәжірибедегі сияқты құйғаннан бастап лай пайда болғанға дейінгі уақытты санайды. Алынған мәліметтерді кестеге жазады:
| Пробирка № | Ерітінді көлемі (тамшылар) | Температура, оС | Ақ түсті лайдың пайда болу уақыты, t, с | Реакцияның меншікті жылдамдығы w=1/t (с-1) | |
| Na2S2O3 | H2SO4 | ||||
Тәжірибе нәтижесінде реакция меншікті жылдамдығының температураға тәуелділік графигін тұрғызады (абцисса осінде температура, ордината осінде – реакция жылдамдығы).
Вант-Гофф теңдеуі бойынша температуралық коэффициенттің орта мәнін есептеңіз. ΔТ = 10-ға тең болғандықтан температуралық коэффициентті жылдамдықтардың қатынасы бойынша анықтайды:
 ;
; 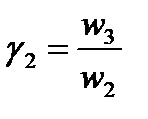 ;
; 
Қорытынды: Берілген реакция үшін температуралық коэффициенттің мәнін есептеңіз және реакция жылдамдығының температураға тәуелділігін сипаттаңыз.
№2 тәжірибелік сабақ
ТАҚЫРЫБЫ: Ерітінділер: құрамын өрнектеу тәсілдері және коллигативтік қасиеттері. Концентрлі ерітіндіден сұйылтылған ерітінді дайындау
МАҚСАТТАРЫ:
· ерітінділер теориясының негізгі түсініктері жайлы және табиғаттағы ерітінділердің биологиялық рөлі жайлы түсініктерін кеңейту;
· ерітінділер құрамын өрнектеу тәсілдері жайлы түсінік қалыптастыру;
· биологиялық нысандарды талдау үшін қажет болатын түрлі концентрациядағы ерітінділерді дайындауға қажет есептеулерді үйрету;
· ерітінділердің медициналық тәжірибеде қолданылуын көрнекілікті қарастыру арқылы студенттерде химияны зерттеу мотивациясын дамыта білу;
· Ақпаратпен өздігінен жұмыс істей білу дағдыларын дамыту.
ОҚЫТУ МІНДЕТТЕРІ:
· түрлі концентрациядағы ерітінділерді дайындау және ерітінді құрамын өрнектеудің бір тәсілінен екінші бір тәсіліне өту үшін қажет есептеулерді үйрету;
· есептеу үшін қажетті мәндерді табу үшін анықтамалық әдебиеттерді дұрыс қолдана білуді дағдыландыру;