 |
|
Лабораторная работа «Определение теплоты нейтрализации»
Цель работы: Экспериментальное определение теплоты нейтрализации сильной кислоты сильным основанием
Ход работы:
| | Калориметрическая установка состоит из внутреннего и наружного стаканов, которые для уменьшения потерь тепла не соприкасаются друг с другом. С этой же целью внутренний стакан установлен на подставке из теплоизоляционного материала (пенопласта). Наружный стакан закрыт крышкой, в которой имеются отверстия для термометра, мешалки и воронки, через которую вводятся реагирующие вещества. |
В сухой внутренний стакан калориметра наливают из бюретки 50 мл раствора гидроксида натрия с молярной концентрацией эквивалента, равной 1 моль/л (0,05 моль NaOH). В другой стакан наливают 50 мл раствора хлороводородной кислоты с молярной концентрацией эквивалента, равной 1 моль/л (0,05 моль-эквивалентов НС1). Определяют температуру кислоты Тк и температуру щелочи Тщ, затем через воронку быстро выливают раствор кислоты в раствор щелочи. Пepемешивaя раствор, наблюдают за столбиком ртути термометра. Фиксируют максимальную температуру раствора Т2 .
| Измеренные и вычисленные величины | Реагирующие вещества | |||
| HCl + NaOH | HNO3 + KOH | |||
| HCl | NaOH | HNO3 | KOH | |
| Концентрация растворов С, моль/л | ||||
| Объем растворов V, л | ||||
| Количество вещества n, моль n = C .V | ||||
| Температура раствора (Тк и Тщ) | ||||
| Начальная температура опыта (Т1) T1 = (Тк + Тщ)/2 | ||||
| Самая высокая температура после нейтрализации (Т2) | ||||
| Разность температур ΔТ ΔТ = Т2 – Т1 |
Массу раствора в калориметрическом стакане определите по формуле
 , где Vр-ра – это объем раствора после нейтрализации (Vщ + Vк), мл; плотность для разбавленных растворов принимается равной 1 г/мл.
, где Vр-ра – это объем раствора после нейтрализации (Vщ + Vк), мл; плотность для разбавленных растворов принимается равной 1 г/мл.
Количество теплоты, выделившееся в данной реакции, рассчитывают по формуле:
 , Дж
, Дж
Таким образом, Q1 – это количество теплоты, которое выделилось при образовании рассчитанного числа моль воды.
Для расчета удельной теплоты реакции нейтрализации найденное значение теплоты необходимо пересчитать на один моль реагирующей кислоты или основания, что соответствует 1 моль образовавшейся воды:
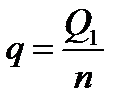 , Дж/моль.
, Дж/моль.
Сравните полученную теплоту нейтрализации с теоретическим значением и рассчитайте абсолютную и относительную ошибки опыта. Объясните причины погрешностей.
Вывод: Укажите найденное значение теплоты нейтрализации, абсолютную и относительную ошибки опыта.