 |
|
Атом фосфора в реакции является
Окислительно-восстановительные реакции, электролиз
Схема реакции, в которой медь проявляет окислительные свойства, имеет вид

Сумма коэффициентов в левой части уравнения
KMnO4 +K2SO3+ H2SO4 =>
Ответ -10
Сумма всех коэффициентов:
4 Mg +10 HNO3 => 4Mg(NO3)2 + NH4NO3 + 3 H2O
Ответ -22
KMnO4 +16 HCl =>2 MgCl2+5Cl2 + 2 KCl + 8H2O
Ответ -35
2KMnO4 +10 KJ + H2SO4 = MnSO 4 +5J2 + 2 K2SO4 + 8H2O
Ответ -41
5PbO2 + 2 Mn(NO3)2 +6 HNO3=> HMnO 4 +5Pb (NO3)2 + 2H2O
Ответ -22
Сколько электронов присоединяет 1 моль окислителя:
H2O2 + K2Cr2O7 + H2SO4 =>Cr2( SO4)3 + K2SO4 +O2 + H2O
Ответ -6
Атом фосфора в реакции является
P+NaOH + H2O => PH3 +NaH2PO4
Ответ – Окислителем и восстановителем
Для окислительно-восстановительной реакции

молярная масса вещества восстановителя равна __34__ г/моль.
Коэффициент перед формулой восстановителя в уравнении окислительно-восстановительной реакции

Коэффициент перед формулой окислителя в уравнении окислительно-восстановительной реакции равен …

Число моль электронов, которое принимает 1 моль окислителя в окислительно-восстановительной реакции

В данной реакции окислителем является 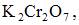
 Следовательно, 1 моль окислителя принимает 6моль электронов.
Следовательно, 1 моль окислителя принимает 6моль электронов.
Число электронов, которое отдает 1 моль восстановителя в окислительно-восстановительной реакции , равно …4

Схема процесса, в котором происходит восстановление железа, имеет вид …
1 



Восстановление железа происходит в реакции, уравнение которой имеет вид

Уравнение реакции, протекающее на индикаторном электроде при определении концентрации ионов водорода методом прямой потенциометрии:
Ответ – 2 Н3О + 2 е = Н2+ 2 Н2О
Cумма коэффициентов уравнения процесса электролиза раствора нитрата серебра
4 AgNO3 + 2 H2O =>4Ag + 4 HNO3 +O2 , Сумма равна15
Сумма коэффициентов при электролизе раствора иодида калия
Ответ – 8
При электролизе раствора бромида калия на катоде протекает реакция:
2H2O + 2e =>H2 + 2OH-
При электролизе водного раствора сульфата натрия на катоде протекает процесс, уравнение которого имеет вид …
2H2O + 2e =>H2 + 2OH-
При электролизе водного раствора гидроксида калияУравнение процесса, протекающего на катоде, имеет вид …
2H2O + 2e =>H2 + 2OH-
Значение рН не изменяется при электролизе с инертными электродами водного раствора соли, формула которой имеет вид …( галогениды, сульфиды малоактивных металлов)
При электролизе водного раствора сульфата меди (II) с инертными электродами на аноде происходит выделение вещества, формула которого имеет вид …О2
Н2О -2е = 1\2 О2 + 2Н+
Одинаковые продукты образуются на инертных электродах при электролизе расплава и водного раствора соединения, формула которого …
При электролизе водного раствора фторида калия на инертном аноде протекает процесс, уравнение которого имеет вид …
2F— -2e = F2
При электролизе водного раствора хлорида калия на инертном аноде протекает процесс, уравнение которого имеет вид …
2Cl— -2e = Cl2
При электролизе водного раствора бромида калия на инертном катоде протекает процесс, уравнение которого имеет вид …

При нарушении оловянного покрытия на железном изделии в кислой среде на аноде будет протекать реакция, уравнение которой имеет вид …

При нарушении никелевого покрытия на медном изделии в кислой среде на аноде будет протекать реакция, уравнение которой имеет вид …
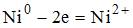
Сумма коэффициентов в общем уравнении электролиза водного раствора йодида калия с инертными электродами равна 8
Покрытое металлом железное изделие при нарушении целостности покрытия во влажной атмосфере будет разрушаться быстрее, если металлом покрытия является
Ni
Zn
Mg
Cr
Уравнение процесса, протекающего на катоде при нарушении никелевого покрытия на железном изделии в нейтральной среде, имеет вид … 
При электролизе водного раствора фторида калия на инертном аноде протекает процесс, уравнение которого имеет вид …

Уравнение процесса, протекающего на катоде при нарушении никелевого покрытия на железном изделии в нейтральной среде, имеет вид …

Значение рН не изменяется при электролизе с инертными электродами водного раствора соли, формула которой имеет вид …K2SO4
ЭДС серебряного концентрационного гальванического элемента будет иметь наибольшее значение, если концентрация раствора нитрата серебра у одного из электродов составляет 0,1 М, а у второго – ______ моль/л.
Моль/л.
наименьшее количество электричества потребуется для получения 1 г ртути
При одинаковых значениях m = 1 г и ne = 2 количество затраченного электричества будет тем меньше, чем больше значение молярной массы выделяемого вещества. Следовательно, наименьшее количество электричества потребуется для получения 1 г ртути (Аr = 201).
Время, в течение которого необходимо пропускать ток силой 11,92 А через раствор соли кадмия, для получения 25 г металла с выходом по току 80%, составляет 75____ минут 