 |
|
Обработка результатов измерений
1. По формуле (9) рассчитать вязкость жидкости  для каждого опыта, при расчетах принять g = 9,81 м/с2.
для каждого опыта, при расчетах принять g = 9,81 м/с2.
2. Рассчитать среднее значение вязкости  , а также абсолютную
, а также абсолютную  и относительную (ε) погрешности (применить методику расчета погрешностей косвенных невоспроизводимых измерений).
и относительную (ε) погрешности (применить методику расчета погрешностей косвенных невоспроизводимых измерений).
3. Записать окончательный результат в виде:
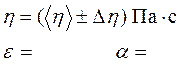
4. Заполнить таблицу.
5. Сделать выводы по результатам работы.
Контрольные вопросы
1. Как возникает сила внутреннего трения?
2. Уравнение Ньютона. Смысл входящих в уравнение параметров.
3. Коэффициент вязкости жидкости. От чего он зависит.
4. Формула Стокса. Смысл входящих в неё параметров.
5. Силы, действующие на шарик при его падении в вязкой жидкости.
6. Какой физический закон применяется при выводе рабочей формулы?
7. Почему необходимо опускать шарик как можно ближе к оси симметрии цилиндра с жидкостью?
8. Почему время движения шарика измеряется только при его движении между метками на цилиндре?
9. Порядок выполнения работы. Обработка результатов измерений.
Лабораторная работа 2–3
ОПРЕДЕЛЕНИЕ ОТНОШЕНИЯ  ДЛЯ ВОЗДУХА
ДЛЯ ВОЗДУХА
Цель работы: ознакомление с методом Клемана и Дезорма и определение отношения  для воздуха.
для воздуха.
Приборы и принадлежности: лабораторный модуль  приборный модуль.
приборный модуль.
Краткая теория
Теплоемкость газов зависит от условий, при которых происходит их нагревание. Различают теплоемкости, соответствующие разным процессам нагревания. Наибольшее практическое значение имеют молярные теплоемкости газа при постоянном объеме 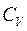 и при постоянном давлении
и при постоянном давлении  .
.
Отношение этих теплоёмкостей  является важным параметром. В частности, оно входит в уравнение адиабаты (уравнение Пуассона):
является важным параметром. В частности, оно входит в уравнение адиабаты (уравнение Пуассона):
 , (1)
, (1)
показывающее как связаны давление и объём газа в процессах, происходящих с газом без теплообмена с окружающей средой. Из молекулярно-кинетической теории идеального газа следует, что для воздуха параметр  1,4.
1,4.
В данной лабораторной работе определяется значение показателя адиабаты  (её называют постоянной, или коэффициентом Пуассона) для воздуха методом, предложенным и осуществлённым в 1819 г. Клеманом и Дезормом.
(её называют постоянной, или коэффициентом Пуассона) для воздуха методом, предложенным и осуществлённым в 1819 г. Клеманом и Дезормом.
 Баллон вместимостью несколько литров (рис. 1) наполняется исследуемым газом при атмосферном давлении Р0. С помощью насоса в баллон дополнительно накачивается небольшая порция того же газа, затем кран К1 закрывается. Через некоторое время температура газа в баллоне становится равной температуре окружающей среды Т0. При этом давление газа будет отличаться от атмосферного: Р1= Р0 +
Баллон вместимостью несколько литров (рис. 1) наполняется исследуемым газом при атмосферном давлении Р0. С помощью насоса в баллон дополнительно накачивается небольшая порция того же газа, затем кран К1 закрывается. Через некоторое время температура газа в баллоне становится равной температуре окружающей среды Т0. При этом давление газа будет отличаться от атмосферного: Р1= Р0 +  Р1.
Р1.
Разность давлений (перепад давлений) внутри и вне сосуда определяется с помощью водяного манометра по формуле Паскаля для гидростатического давления:
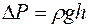 , (2)
, (2)
где  плотность воды;
плотность воды;  ускорение свободного падения;
ускорение свободного падения;  разность уровней воды в изогнутой трубке манометра (см. рис. 1).
разность уровней воды в изогнутой трубке манометра (см. рис. 1).
Затем на короткое время открывают кран К2. Газ, находившийся в баллоне, расширяется, при этом часть его выходит из баллона. Давление в баллоне становится атмосферным, а температура понижается до некоторого значения Т. Охлаждение связано с тем, что газ, расширяясь во внешнюю среду, совершает работу за счёт своей внутренней энергии. Из-за кратковременности процесса расширения он проходит без теплообмена с окружающей средой, т. е. адиабатически.
Спустя некоторое время после закрытия крана К2 температура газа опять сравнивается с температурой окружающего воздуха. Поскольку этот процесс происходит изохорно, давление в баллоне повысится: Р2= Р0 +  Р2. Величина
Р2. Величина  Р2 также определяется с помощью манометра.
Р2 также определяется с помощью манометра.
Измеренные значения перепадов давлений  Р1 и
Р1 и  Р2 позволяют вычислить величину коэффициента Пуассона для воздуха.
Р2 позволяют вычислить величину коэффициента Пуассона для воздуха.
| |
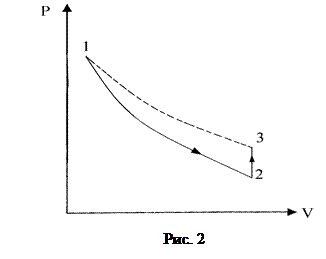 1 состояние: Р1 Т0 V1
1 состояние: Р1 Т0 V1
2 состояние: Р0 Т V2
3 состояние: Р2 Т0 V2
Эти состояния и переходы между ними показаны в координатах P – V на рис. 2. Процесс 1–2 происходит адиабатически, процесс 2–3 – изохорно. Состояния 1 и 3 лежат на одной изотерме (пунктирная линия). Это означает, что для параметров перечисленных состояний справедливы уравнения:

и

из которых следует:
 . (3)
. (3)
Логарифмируя (3), получаем:
 (4)
(4)
Зная атмосферное давление, пользуясь (4) можно найти искомую постоянную Пуассона. Однако без измерения Р0 можно обойтись. Дело в том, что в опыте Клемана и Дезорма давления Р1 и Р2 мало отличаются от Р0, т. е. выполняются неравенства:  и
и  . Причём, согласно (2):
. Причём, согласно (2):
 ,
,
а
 .
.
Если принять во внимание, что при  для функции
для функции  справедливо выражение:
справедливо выражение:
 ,
,
из (4) нетрудно получить приближенную формулу для расчёта коэффициента Пуассона:
 (5)
(5)
Отметим, что постоянная Пуассона при учёте уравнения Майера  позволяет находить молярные теплоёмкости исследуемого газа:
позволяет находить молярные теплоёмкости исследуемого газа:
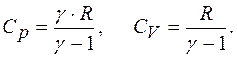 (6)
(6)