 |
|
Декарбоксилирование солей низших карбоновых кислот
(для газообразных углеводородов)
t0
CH3COONa + NaOH  Na2CO3 + CH4↑
Na2CO3 + CH4↑
тв тв
t0
CH3 CH 2COOK + KOH  K2CO3 + C 2H6↑
K2CO3 + C 2H6↑
тв тв
2.2Химические свойства алканов
1. Галогенирование – реакция радикального замещения (SR)атомов
водорода на галогены.
а) Инициирование– образование свободных радикалов
Молекулы хлора поглощают свет и диссоциируют на атомы:

б) Рост цепи
Атом хлора может отнимать атом водорода у молекулы алкана с
образованием хлороводорода и алкильного радикала:

Алкильный радикал атакует молекулу хлора,образуя молекулу
алкилгалогенида и атом хлоа, который способен начать следующую
стадию этой цепной реакции
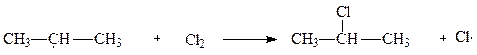
в) Обрыв цепи
Обрыв цепи происходит при взаимодействии каких-либо двух
имеющихся в смеси радикалов: 
Вообще получить по этому методу монозамещённые продукты
практически невозможно, так как образующиеся алкилгалогениды
взаимодействуют дальше с атомами хлора. На ярком свету реакция
протекает очень бурно(со взрывом).
Устойчивость свободных радикалов уменьшается в следующем ряду:

аллил третбутил изопропил пропил
Поэтому основным продуктом радикального замещения в реакциях галогенирования алканов являются соединения, в которых атом галогена связан с аллильным или третичным атомом углерода. Гораздо меньше продуктов замещения по вторичному и первичному атомам углерода.
Бромирование протекает менее энергично, взаимодействие с иодом осуществить практически не удаётся, наоборот, фтор взаимодействует с алканами со взрывом.
При бромировании преобладают соединения, в которых атом брома связан с третичным атомом углерода. При хлорировании образуется сложная смесь, в которых атом хлора связан с третичным, вторичным и первичным
атомами углерода.
һ ν
СН3− СН2− СН− СН3 + Br2  СH3−CH2 – CBr − CH3 + HBr +
СH3−CH2 – CBr − CH3 + HBr +
| |
CH3 CH3
2-метилбутан 2-бром-2-метилбутан
(основной продукт)
CH3 – CH – CH – CH3
| |
Br CH3
2- бром- 3- метилбутан
(побочный продукт)
В молекуле алкана могут замещаться один или несколько атомов водорода СН3 − СН2− СН3 + Cl2  СН3 − СН − СН3 + HCl
СН3 − СН − СН3 + HCl
|
Cl
Cl
|
СН3 − СН2 − СН3 + 2 Cl2  СН3 − С − СН3 + 2 HCl
СН3 − С − СН3 + 2 HCl
|
Cl
Cl
|
СН3 − СН2 − СН3 + 3 Cl2  СH2 − С − СН3 + 3 HCl
СH2 − С − СН3 + 3 HCl
| |
Cl Cl
При этом образуется смесь галогенпроизводных.