 |
|
Некоторые свойства стирола.
Как уже было сказано выше, стирол не относится к аренам, так как имеет двойную связь, и основным типом химических реакции для него будут реакции присоединения, окисления и полимеризации.
Так стирол легко реагирует с бромной водой, обесцвечивая ее, что является качественной реакцией на двойную связь:

По той же схеме происходит гидрирование стирола на никелевом катализаторе:

Окисление стирола осуществляется холодным водным раствором перманганата калия, продуктом окисления будет ароматический двухатомный спирт:

При окислении горячим раствором перманганата калия в присутствии серной кислоты будет образовываться бензойная кислота и углекислый газ.
Важной реакцией, имеющей большое практическое значение, является реакция полимеризации стирола:
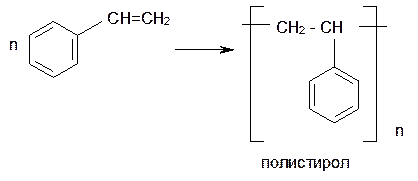
Винильная группа представляет собой ориентант I рода, поэтому дальнейшее каталитическое замещение (например, галогеналканами) пойдет в орто- и пара- положения.
7.3.Примеры решения задач
Пример 21.Плотность по озону газовой смеси, состоящей из паров бензола и водорода, равна 0,2. После пропускания через контактный аппарат для синтеза циклогексана величина этой относительной плотности составила 0,25. Определить объемную долю паров циклогексана в конечной смеси и практический выход циклогексана.
Решение:
1)Найдем молярную массу исходной смеси:
Мсм = D(O3)∙M (O3) = 0.2∙ 48=9.6 г/моль.
2) Молярная масса конечной смеси равна 0,25 ∙ 48=12 г/моль.
3) Найдем молярное соотношение компонентов в исходной смеси
Мсм= φ∙М(бенз.) + М(водор.) ∙(1-φ ), где φ-молярная (объемная) доля бензола
9,6 = 78φ + 2(1 –φ); 7,6 = 76φ; φ =0,1.
Значит, объемная доля водорода равна 0,9.
Следовательно, водород – в избытке, расчет ведем по бензолу.
4) Пусть количество исходной смеси равно 1 моль.
Тогда n(C6H6) = 0.1 моль, n(H2) = 0,9 моль,
а масса исходной смеси mсм =1∙9,6= 9,6г.
Обозначим количество прореагировавшего бензола –z(моль) и
составим количественный баланс этой реакции.
С6Н6 + 3Н2 = С6Н12
Было 0,1 0,9 0
Прореагировало z 3 z z
Запишем эти данные для удобства в виде таблицы:
| Вещества | Было(моль) | Прореаг.(моль) | Стало(моль) |
| С6Н6 | 0,1 | Z | 0,1- z |
| Н2 | 0,9 | 3z | 0,9 –3z |
| С6Н12 | - | - | Z |
5) Найдем общее количество веществ в конечной реакционной смеси:
n(кон) = 0,1 – z + 0,9 – 3z + z = 1 - 3 z .
Так как общая масса веществ в контактном аппарате не изменилась,
то n(кон)= mсм/ М(конечн) = 9,6/12 = 0,8моль.
6) Тогда 1 – 3z = 0,8; 3 z = 0,2; z= 0,067.
В таком случае объемная доля циклогексана равна 0,067/0,8 = 0, 084.
7) Теоретическое количество циклогексана составляет 0,1 моль; количество образовавшегося циклогексана 0,067 моль. Практический выход
η =0,067/0,1= 0,67 (67,0%).
Ответ: φ(циклогексана) = 0,084. η =0,067/0,1= 0,67 (67,0%).
Пример 22. На нейтрализацию смеси ароматических кислот, полученных окислением смеси этилбензола и его изомеров, требуется объем раствора гидроксида натрия в пять раз меньший, чем минимальный объем такого же раствора, необходимого для поглощения всего углекислого газа, полученного при сжигании той же порции смеси изомеров. Определить массовую долю этилбензола в исходной смеси.
Решение:
1) Этилбензол - С6Н5С2Н5. М = 106 г/моль; его изомерами являются диметилбензолы, имеющие одинаковую молекулярную формулу С6Н4(СН3)2 и ту же молярную массу, что и этилбензол.
Пусть количество этилбензола равно х(моль), а количество смеси диметилбензолов – y(моль).
2) Напишем уравнения реакций окисления этилбензола и его изомеров:
5C6H5C2H5 + 12KMnO4 + 18H2SO4  5C6H5COOH + 5CO2 +
5C6H5COOH + 5CO2 +
x x
+ 12MnSO4 + 6K2SO4 + 28H2O
5C6H4(CH3)2 + 12KMnO4 + 18H2SO4  5C6H4(COOH)2 +
5C6H4(COOH)2 +
y y
+ 12MnSO4 + 6K2SO4 + 28H2O
Очевидно, что количества бензойной кислоты и смеси фталевых кислот тоже равны x и yсоответственно.
3) Уравнения нейтрализации полученных органических кислот:
С6Н5СООН + NaOH = С6Н5СООNa + H2O
x x
С6Н4(СООН)2 + 2NaOH = С6Н4(СООNa)2 + 2 H2O
y 2 y
Из этих уравнений следует, что общее количество щелочи, пошедшее на
нейтрализацию смеси кислот n(общ) = x + 2 y
4) Рассмотрим уравнения сжигания углеводородов, учитывая, что все они
имеют молекулярную формулу С8Н10.
С6Н5С2Н5 + 10,5 О2  8 СО2 + 5H2O
8 СО2 + 5H2O
x 8x
С6Н4(СН3)2 + 10,5 О2  8 СО2 + 5H2O
8 СО2 + 5H2O
y 8y
5) Из этих уравнений следует, что общее количество углекислого газа после сжигания исходной смеси аренов равно n(СО2) = 8x + 8y
6) Так как требуется затратить минимальное количество щелочи, то нейтрализация протекает с образованием кислой соли:
NaOH + СО2 = NaHCO3
8x + 8y 8x + 8y
Таким образом, количество щелочи на нейтрализацию СО2 тоже равно
8x + 8y. В таком случае 8x + 8y = 5(x + 2y ); y =1,5x. x =2/3y 7) Расчет массовой доли этилбензола
ω(этилбензола) = m(этилбензола)/m(общ) = 106x/(106x +106y) =
1/ ( 1 +1,5) = 0,4 .
Ответ: ω (этилбензола) = 0,4 =40% .
Пример 23.Смесь толуола и стирола сожгли в избытке воздуха. При пропускании продуктов сгорания через избыток известковой воды образовалось 220 г осадка. Найдите массовые доли компонентов в исходной смеси, если известно, что она может присоединить
2,24 л HBr (н. у.).
Решение:
1) С бромоводородом реагирует только стирол в соотношении 1:1.
C8H8 + HBr = C8H9Br
2) Количество вещества бромоводорода
n( HBr) = n (C8H8) = 2,24/22,4 = 0,1моль.
3) Запишем уравнение реакции сгорания стирола:
C8H8 + 10 О2  8 СО2 + 4H2O
8 СО2 + 4H2O
В соответствии с уравнением реакции при сгорании 0,1моль стирола образуется 0,8 моль углекислого газа.
4) Углекислый газ реагирует с избытком гидроксида кальция тоже в
мольном соотношении 1:1 с образованием осадка карбоната кальция:
Ca(OH)2 + СО2 = CaCO3
5) Общее количество карбоната кальция равно
n(CaCO3) = m(CaCO3)/ M(CaCO3) = 220/100 = 2,2моль.
Значит, при сгорании углеводородов образовалось тоже 2,2моль СО2, из
которых 0,8моль дает при сгорании стирол.
Тогда на долю толуола приходится 2,2 - 0,8 = 1,4 моль СО2.
6) Уравнение сгорания толуола:
C7H8 + 9 О2  7СО2 + 4H2O
7СО2 + 4H2O
Количество толуола в 7 раз меньше, чем количество углекислого газа:
n(толуол) = 1,4/7 = 0,2 моль.
7) Масса стирола m(стир.) = n(стир)∙M(стир) = 0,1∙104 =10,4(г);
масса толуола m(тол) = n(тол)∙M(тол) =0,2∙92 = 18,4(г).
8) Общая масса смеси углеводородов 10,4 + 18,4= 28,8(г).
массовая доля стирола: ω =10,4/ 28,8 = 0,361;
массовая доля толуола ω=0,639.
Ответ: ω(стирол) = 0,361 = 36,1%; ω(толуол)=0,639=63,9%.