 |
|
Для всех компонентов смеси, с учетом законов Дальтона и Амага, справедливо
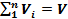 и
и 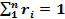
Объемные доли также часто задаются в процентах. Для воздуха rO2 ≈ 21% rN2 ≈ 79%
Мольной долей называется отношение количества молей Ni рассматриваемого компонента к общему количеству молей смеси N.
Общее количество молей смеси  .
.
Мольная доля i-го компонента равна
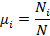
В соответствии с законом Авогадро
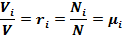
И, следовательно, задание смеси идеальных газов мольными долями равно заданию ее объемными долями.

1. Газовая постоянная смеси идеальных газов.
Закон Клапейрона для смеси идеальных газов имеет вид:
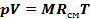
где Rсм - газовая постоянная смеси
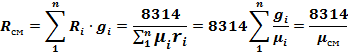
2. Кажущаяся молекулярная масса смеси.
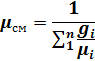
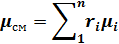
3. Соотношение между объемными и массовыми долями.
Для каждого компонента и для всей смеси в целом справедливо соотношение

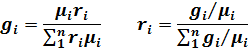
4. Расчет теплоемкости смеси
При расчете теплоемкости смеси принимают, что для нагрева (охлаждения) газовой смеси необходимо нагреть (охладть) каждый ее компонент

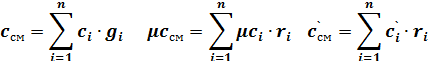
Если тепоемксть компоненов задана в функции от температуры , например ci=ai+biT

Расчетно-графическая работа №1
Задан объемный состав газовой смеси:  . Данные для расчета приведены в таблице 1.
. Данные для расчета приведены в таблице 1.
Определить массовый 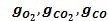 и мольный
и мольный 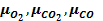 состав смеси, кажущуюся молекулярную массу µсм, газовую постоянную Rсм, удельный объем vсм и плотность смеси ρсм при давлении смеси P, МПа температуре смеси t, оС.
состав смеси, кажущуюся молекулярную массу µсм, газовую постоянную Rсм, удельный объем vсм и плотность смеси ρсм при давлении смеси P, МПа температуре смеси t, оС.
Определить массовую Cсм, объемную C’см и мольную µCсм теплоемкости смеси. Принять линейную зависимость теплоемкости от температуры. Исходные данные для расчетов взять в справочнике.
Таблица 1.
| Вариант | 
| 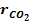
| 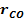
| P, МПа | t, оС |
| 0,1 | 0,6 | 0,30 | 0,10 | ||
| 0,15 | 0,5 | 0,35 | 0,15 | ||
| 0,2 | 0,4 | 0,40 | 0,20 | ||
| 0,25 | 0,5 | 0,25 | 0,25 | ||
| 0,3 | 0,6 | 0,10 | 0,30 | ||
| 0,35 | 0,5 | 0,15 | 0,35 | ||
| 0,4 | 0,4 | 0,20 | 0,40 | ||
| 0,45 | 0,3 | 0,25 | 0,35 | ||
| 0,5 | 0,2 | 0,30 | 0,30 | ||
| 0,55 | 0,1 | 0,35 | 0,25 | ||
| 0,6 | 0,1 | 0,30 | 0,20 | ||
| 0,65 | 0,2 | 0,15 | 0,15 | ||
| 0,6 | 0,3 | 0,10 | 0,10 | ||
| 0,55 | 0,2 | 0,25 | 0,15 | ||
| 0,5 | 0,1 | 0,40 | 0,20 | ||
| 0,45 | 0,2 | 0,35 | 0,25 | ||
| 0,40 | 0,3 | 0,30 | 0,30 | ||
| 0,35 | 0,4 | 0,25 | 0,35 | ||
| 0,30 | 0,3 | 0,40 | 0,40 | ||
| 0,25 | 0,4 | 0,35 | 0,45 |
Молекулярные массы газов:
μCO2 = 44 кг/кмоль
μO2 = 32 кг/кмоль
μCO = 28 кг/кмоль