 |
|
Идеальный газ – молекулы которого являются не взаимодействующими материальными точками.
Идеальный газ это физическая модель.
Fвзаим = 0 Vмол = 0
1. Вакуум – это разряженный газ
Применения вакуума:
- Электро лучевая трубка (кинеском)
-Ускоритель элементарных частиц (микрофазатрон)
3. Термодинамические параметры газа – это величины однозначно характеризующие состояние газа P,V,T (давление, объем, температура)
а) Давление Р
P=⅔n0  пост - основное уравнение МКТ. (
пост - основное уравнение МКТ. (  пост - Средняя кенетическая энергия поступательного движения молекул.)
пост - Средняя кенетическая энергия поступательного движения молекул.)
Измеряется манометрами, барометрами.
[P] = 1 Па
б) Температура Т
 пост=
пост=  кТ (К – постоянная Больцмана)
кТ (К – постоянная Больцмана)
Температура – это мера средней кенетической энергии поступательного движения молекул.
[T] = 1K
T = tC + 273o
(Понятие температуры пременимо только к телам и не может применятся к одной молекуле).
в) Объем V
Vгаза = Vсосуда
[V] = 1м3
Вопрос
Вывод уравнения Менделеева-Клаперона. Объедененый газовый закон.
Выведем уравнение, которое связывет 3 динамические параметра: P,V,T.
1) 

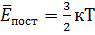
 – уравнение состояния идеального газа или уравнение Менделеева-Клаперона
– уравнение состояния идеального газа или уравнение Менделеева-Клаперона
R – молярная газовая постоянная.
2) Пусть m = const  = const
= const



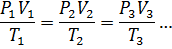
Вопрос
Изопроцессы в газах.
Изопроцессами в газах называются такие процессы, в которых не изменяется один из термодинамических параметров.
| m = const M = const | ||||
V = const
Изохорный процесс
 Закон Шарля
Закон Шарля

| P = const
Изобарный процесс
 Закон Гей Люссона
Закон Гей Люссона 
| T = const
Изотермический процесс
PV = const
Закон Бойля Мариотта

| ||
| Работа газа | ||||
| А = 0 | А = P∙ΔV | A = S | ||
Физичиский смысл молярной газовой постоянной.
Расчитаем работу 1 моля газа при изобарном нагревании
А1моль = P∙ΔV =  R∙ΔT = RΔT
R∙ΔT = RΔT
A1моль = R∙ΔT
R = 
Молярная газовая постоянная численно равна работе одного моля газа при изобарном нагревании на 1 Кельвин.
Вопрос