 |
|
Суть полярогафического метода.
Полярографический метод основан на определении зависимости силы тока от потенциала при электролизе раствора исследуемого вещества в определенных условиях.
Для полягрофического анализа пригодна любая установка, на которой можно поляризовать микроэлектрод до желаемого потенциала и измерять силу тока. 
Основная часть полярографа -представляет собой электролитическую ячейку, состоящую из сосуда, наполненного раствором анализируемого вещества, и двух ртутных электродов. Анодом является ртуть, заполняющая дно сосуда; катодом—капли ртути образующиеся на конце капиллярной трубки, заполненной ртутью. Под влиянием собственной тяжести капля ртути падает на дно сосуда, после чего образуется новая капля и т. д. Таким образам, катодом является непрерывно возобновляющаяся капля ртути.
При прохождении через раствор даже небольшой силы тока (10-6а) происходит химическая поляризация катода за счет восстановления ионов или молекул исследуемого вещества на поверхности электрода. В результате электрохимического восстановления на поверхности ртутной капли образуется вещество, при этом потенциал катода ек определяется соотношением концентраций исходного и восстановленного.
Так как площадь ртутного анода большая, а плотность тока на нем мала, то химические явления не способны изменить электродный потенциал анода еа, поэтому потенциал анода практически сохраняется неизменным.
Таким образом, при прохождении тока через описанную ячейку, когда протекает непрерывный электролиз, возникает электродвижущая сила поляризации, равная  направленная навстречу приложенному напряжению Е. Если учесть омическое сопротивление, то сила тока по закону Ома равна:
направленная навстречу приложенному напряжению Е. Если учесть омическое сопротивление, то сила тока по закону Ома равна:  отсюда следует
отсюда следует  где R — сопротивление раствора между электродами. Поскольку сопротивление R раствора обычно не превышает 100 Ом, то произведение IR очень мало (10-6-100= =0,1 мвB); в таком случае можно считать, что IR=0, следовательно:
где R — сопротивление раствора между электродами. Поскольку сопротивление R раствора обычно не превышает 100 Ом, то произведение IR очень мало (10-6-100= =0,1 мвB); в таком случае можно считать, что IR=0, следовательно:
Е == еа — ек.
Принимая постоянный потенциал анода условно за нуль, получим выражение: 
показывающее, что все приложенное напряжение Е уравновешивается потенциалом поляризации катода. Поэтому такой ртутный электрод называют абсолютно поляризующим. Потенциал его зависит от природы восстанавливающегося на нем иона или вещества.
Зависимость «сила тока - потенциал» выражается обычно графически в виде поляризационных кривых (полярограмм). Величины потенциалов в вольтах (или милливольтах) откладываются на оси абсцисс, а соответствующие им силы тока в микроамперах — на оси ординат.

Общий вид типичной поляризационной кривой приведен на рис. 3. Так как ртутные капли сменяют друг друга через определенный промежуток времени, то полярограммы имеют обычно зубчатый вид, поскольку в момент отрыва капли ток прерывается. Сопротивление раствора должно быть возможно меньшим (<1000 Ом), поэтому для увеличения электропроводности вводят в раствор добавки электролитов, не вступающих в реакцию с испытуемым раствором и не выделяющихся на электроде при потенциалах восстановления исследуемых веществ. Такие добавки называют фонами (КС1, LiCl, Na2S04, NH4CI, тетраалкиламмониевые соли и др.).
Основное условие правильного проведения полярографического анализа - подавление миграционного и конвективного токов. Эти токи возникают вследствие того, что кроме диффузии доставка деполяризатора к ртутно капающему электроду может осуществляться миграцией, обусловленной действием электрического поля, и конвекцией при механическом перемешивании раствора или вследствие различий в плотности внутри раствора, вызванных перепадами концентрации или температуры. Миграция и конвекция мешают диффузии ионов к ртутно капающему электроду, следовательно, мешают полярографированию.
При низких потенциалах через электролизер проходит очень слабый, почти не меняющийся с ростом потенциала ток (остаточный ток). При определенном, характерном для каждого вещества, потенциале начинаемся процесс электролиза: растворенное вещество восстанавливается или окисляется на капельном ртутном электроде.
Потенциал, при котором начинается электролиз, называют потенциалом выделения. Начало процесса электролиза характеризуется быстрым ростом силы тока даже при незначительном увеличении потенциала — скачок силы тока (см. рис. 3). Но сила тока возрастает не бесконечно, а достигает некоторого предельного значения, после чего не меняется при дальнейшем увеличении потенциала.
Этот ток называют предельным, или диффузионным, так как он зависит от скорости диффузии восстанавливающегося вещества. В результате на графике получается
характерная кривая с изгибом, которую называют полярографической волной.
Образование волны указывает прежде всего на наличие в испытуемом растворе вещества, способного к восстановлению (или окислению, если капельный ртутный электрод служит анодом). Потенциал, при котором наблюдается скачок тока, может служить для целей качественного анализа, а высота волны, то есть отрезок между двумя горизонтальными участками кривой, может служить для целей количественного анализа, так как ток определяется скоростью диффузии ионов к катоду, зависящей от концентрации ионов в растворе. Высота Н волны полярограммы зависит также от размеров ртутной капли и от времени смены капли. Однако кривые, полученные для различных концентраций определяемого вещества в растворе (рис. 4), симметричны относительно середины волны. Напряжение, соответствующее полуволне, не зависит от концентрации ионов или молекул в растворе, от масштабов диаграммы и от параметров ячейки. Поэтому при качественном анализе пользуются потенциалами -полуволн 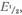 так как они характерны для каждого вещества.
так как они характерны для каждого вещества.


Потенциалом полуволны называется то значение потенциала, при котором происходит возрастание силы тока до половины предельного значения.
Потенциал полуволны можно определить с помощью уравнения полярографической волны: 
где  — предельная сила тока; п — число электронов, участвующих в электрохимической реакции.
— предельная сила тока; п — число электронов, участвующих в электрохимической реакции.
Если откладывать на оси абсцисс значения Е, а на оси ординат  ., то построенный график представляет собой прямую, отсекающую на оси абсцисс отрезок, равный потенциалу полуволны, так как при
., то построенный график представляет собой прямую, отсекающую на оси абсцисс отрезок, равный потенциалу полуволны, так как при  ,
,  и, следовательно,
и, следовательно, 
Потенциал полуволны можно определить и другим, более простым способом. Для этого на полярограмме из середины волны опускают перпендикуляр на ось абсцисс. Расстояние от точки пересечения перпендикуляра с осью абсцисс до начала координат равно  . Однако этот способ определения менее точен.
. Однако этот способ определения менее точен.
По этому графику можно определить число электронов п, участвующих в электрохимической реакции. Сделать это можно, найдя котангенс (мВ) и сравнив его с теоретическим значением. Из уравнения полярографической волны следует, что теоретические величины равны соответственно: 59,16 мВ для n = 1; 29,58 мВ для n = 2; 19,7 мВ для n = 3. Если же число электронов, участвующих в электрохимической реакции известно, то по этому критерию можно установить, обратимо ли протекает данная реакция на электроде. При совпадении экспериментальной величины наклона с теоретической можно полагать, что электрохимическая реакция протекает обратимо.
Ток, проходящий через электролизер до скачка силы тока (см. рис. 3), называется остаточным током. В ряде случаев он вызван примесями различных восстанавливающихся веществ, например следами меди и др.
Второй составляющей остаточного тока является так называемый емкостный ток (конденсаторный ток). Прохождение такого тока наблюдается даже в том случае, если раствор совершенно не содержит восстанавливающихся веществ. Емкостный ток обычно невелик и не вызывает каких-либо затруднений при полярографировании. Его следует учитывать в тех случаях, когда концентрация определяемого вещества настолько мала, что диффузионный ток по своей величине становится соизмеримым с емкостным током или меньше. Тогда нужно принимать особые меры для его устранения.