 |
|
Химические свойства
Аминокислоты – бесцветные кристаллические вещества с высокими температурами плавления, которые мало отличаются для разных аминокислот и поэтому не характерны. Плавление сопровождается разложением вещества. Плавление с разложением характерно для солей. Будучи солями аминокислоты хорошо растворимы в воде. Водный раствор аминокислот имеет нейтральную реакцию, что также характерно для солей. Аминокислоты представляют собой так называемые внутренние соли (биполярные ионы):
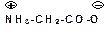
Такой ион в кислой среде ведет себя как катион, так как подавляется диссоциация карбоксильной группы, а в щелочной среде аминокислота ведет себя как анион:

Значение рH при котором достигается максимальная концентрация биполярного иона – называется изоэлектрической точкой.
Подобно другим соединениям со смешанными функциями, аминокислоты проявляют свойства кислот и аминов.
Аминокислоты образуют соли с основаниями. Соли α-аминокислот с тяжелыми металлами могут иметь комплексный характер:

соль имеет интенсивно синее окрашивание.
Аминокислоты образуют соли с неорганическими кислотами:

Подобно другим кислотам, аминокислоты образуют сложные эфиры, хлорангидриды, амиды и т.д:

При действии азотистой кислоты аминокислоты образуют гидроксикислоты:

Аминогруппа в аминокислотах легко ацилируется при действии ангидридов и хлорангидридов кислот:

При алкилировании аминогруппы получаются вторичные и третичные аминокислоты. В избытке галоидного алкила образуются четырехзамещенные аммонийные основания. Внутренние соли таких оснований называются бетаинами:

Поведение α, β и γ-аминокислот при нагревании:
α-аминокислоты межмолекулярно образуют циклические амиды – дикетопиперазины:
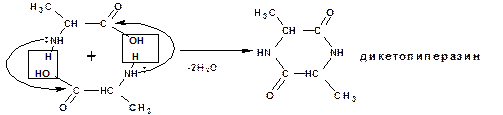
β-аминокислоты при нагревании отщепляют молекулу аммиака с образованием α,β-ненасыщенных кислот (аммонийная соль ):

γ и δ-аминокислоты при нагревании отщепляют воду и образуют внутримолекулярные циклические амиды – лактамы:

БЕЛКИ
Классификация
Определение: Белки – это сложные высокомолекулярные органические соединения , построенные из остатков аминокислот, соединенных между собой амидными связями.
Белки разделяются на протеины (простые белки), в состав которых входят только остатки аминокислот и протеиды (сложные белки). Это белки построенные не только из аминокислот, но и из других веществ: сахаридов или остатков фосфорной кислоты и нуклеиновые кислоты.
Протеины классифицируются по трем группам.
1. По растворимости в воде:
Альбумины - растворимые в воде и разбавленных растворах солей.
Глобулины – мало растворимые в воде и растворимые в разбавленных растворах солей.
Проламины – нерастворимые в воде и растворимые в водном спирте.
Глютелины - нерастворимые в воде, в разбавленных растворах солей и водном спирте, растворимы в растворах кислот и щелочей.
Склеропротеины - нерастворимые в воде, в разбавленных растворах солей, водном спирте и в растворах кислот и щелочей.
2. Протеиды классифицируются по продуктам гидролиза:
Нуклеопротеиды – гидролизуются на протеины и нуклеиновые кислоты.
Фосфопротеиды - гидролизуются на протеины и фосфорную кислоту.
Глюкопротеиды - гидролизуются на протеины и углевод.
Хромопротеиды - гидролизуются на протеины и красящие вещества.
3. Все белки классифицируются по функциям в организме:
Резервные белки
Структурные белки
Белки, управляющие метаболизмом.
Как и аминокислоты, белки обладают амфотерным характером и изоэлектрической точкой. Положение изоэлектрической точки для белков может колебаться в широких пределах от кислой до сильнощелочной.
Все белки оптически активны. Большинство из них обладает левым вращением.
Существует ряд качественных цветных реакций на белки:
1. Ксантопротеиновая с азотной кислотой. Белки обработанные азотной кислотой дают желтое окрашивание.
2. Биуретовая с солями меди в присутствии щелочи. Белки дают фиолетовую окраску за счет образования комплексной соли.
3. Реакция Миллона. С раствором нитрата ртути в азотистой кислоте белки дают красное окрашивание.
4. Сульфгидрильная. При нагревании белков с раствором плюмбита натрия выделяется черный осадок сульфида свинца.
Белки построены из остатков 26 аминокислот. Аминокислоты делятся на заменимые, которые могут быть синтезированы организмом и незаменимые, которые человеческим организмом не синтезируются. Например, изолейцин и треонин.
Остатки аминокислот связаны в белковой молекуле амидными связями. Амидная связь в белках называется пептидной связью:

Карбоксильная группа одной молекулы аминокислоты образует амид, взаимодействуя с аминогруппой соседней молекулы аминокислоты. Отдельные пептидные звенья:
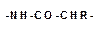
отличаются друг от друга только радикалами «R» при α-углеродном атоме.
Соединения, содержащие несколько аминокислотных остатков, называются пептидами. Соединения с большим количеством пептидных звеньев называются полипептидами.
При исследовании полипептидов в первую очередь выясняют, из каких аминокислот построена макромолекула, а также какая аминокислота является N-концевой (свободная аминогруппа), а какая является С-концевой (свободная корбоксильная группа).
Белки нацело гидролизуются в аминокислоты концентрированной соляной кислотой или 2% соляной кислотой при нагревании и при повышенном давлении. Гидролиз белков можно провести под действием щелочи. Выбор реагента зависит от того, какие конкретно аминокислоты необходимо получить из молекулы белка.