 |
|
Химические свойства азота
Лабораторная работа №5
«Химические свойства серы, азота, фосфора
И их соединений»
ТЕОРЕТИЧЕСКОЕ ВВЕДЕНИЕ
СЕРА
Сера Sв свободном состоянии образует несколько аллотропных соединений, важнейшие из которых:
a - сера (ромбическая)
b - сера (моноклиническая)
Сера Sвстречается в природных условиях в виде залежей почти чистой самородной серы, а также входит в состав различных сульфидных руд:
FeS2- железный колчедан (пирит);
ZnS- цинковая обманка;
CaSO4- гипс;
HgS- киноварь;
Na2SO4∙10H2O - глауберова соль;
MgSO4∙7H2O - горькая соль.
Сера Sвходит в состав биологических тканей всех растений и живых организмов в форме аминокислот, таких как цистеин, цистин, метионин.
Химические свойства серы
Атом серы S, имеет незавершённый внешний энергетический уровень и может присоединять два электрона, проявляя степень окисления (-2).
При отдаче электронов к атому более электроотрицательного элемента степень окисления серы может быть +2, +4, +6.
Сера Sлегко образует соединения со многими элементами. При сгорании её на воздухе или в кислороде образуется оксид серы (IV) SO2и оксид серы (VI) SO3.
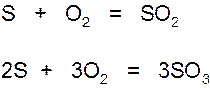
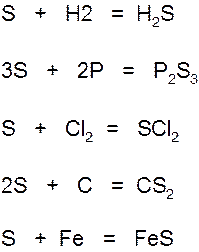
Сероводород и сульфиды
H2S - бесцветный газ с запахом тухлых яиц, хорошо растворим в воде. Очень ядовит - поражает нервную систему.
Получение
1. При нагревании серы Sв водороде:

2. Действием разбавленных соляной (HCl) или серной (H2SO4) кислот на сульфид железа:

Химические свойства сероводорода – H2S
1. При сильном нагревании разлагается:
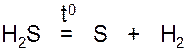
2. Газообразный сероводород горит на воздухе голубым пламенем:

3. Энергично реагирует с растворами галогенов:

4. Слабая сероводородная кислота H2S диссоциирует на ионы:
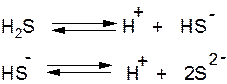
5. Сероводородная кислота H2S2- является восстановителем и окисляется как сильными окислителями, такими как хлор:
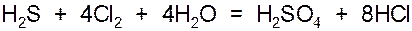
так и более слабыми окислителями:

Оксид серы (IV) - SO2. Сернистая кислота (H2SO3)
Оксид серы (IV) SO2- бесцветный газ, образуется:
1. При сгорании серы на воздухе:

2. При сгорании сероводорода:

3. При взаимодействии с некоторыми металлами:

4. При обжиге сульфидных минералов:
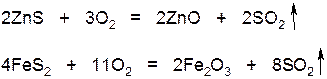
При растворении в воде образуется слабая сернистая кислота H2SO3 , которая мало устойчивая и вновь распадается на оксид серы (IV)SO2 и воду:
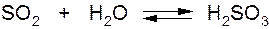
Кислота даёт два ряда солей: средние – сульфиты и кислые – гидросульфиты.
Оксид серы (VI) - SO3. Серная кислота (H2SO4)
Получение
1. Окисление на катализаторе и при высоком давлении:

2. При растворении в воде образуется серная кислота:

H2SO4 - сильная двухосновная кислота:

Азот
Азот N2 – газ без цвета,вкуса и запаха; легче воздуха.
Общее содержание азота в земной коре - 0,03%. Наибольшая его часть сосредоточена в атмосфере - N2 (около 78 об.%).
Азот Nвходит в состав растений и животных организмов (в форме белков). Растения синтезируют белки, используя нитраты из почвы.
Получение азота
1. «Фракционная перегонка» жидкого воздуха.
2. В лаборатории азот N2 получают при нагревании концентриро-ванного раствора нитрита аммония:

или разложением солей аммония:

Химические свойства азота
Хотя азот N2 один из наиболее электроотрицательных элемен-тов, он обладает сравнительно низкой реакционной способностью. Причина заключается в том, что его двухатомные молекулы неполярные, а тройная связь между двумя атомами азота в них обладает очень высокой прочностью. Энтальпия этой связи равна +944 кДж/моль.

При обычных условиях азот N2 реагирует только с литием, образуя нитрид:

С другими металлами реакция идёт только при нагревании:
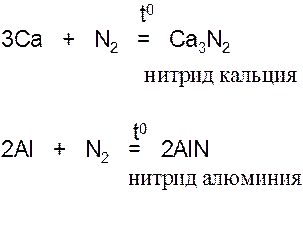
Азот N2 взаимодействует с водородом и кислородом:

Нитриды металлов легко гидролизуются и взаимодействуют с кислотами:

Аммиак - NH3
Аммиак - NH3– бесцветный газ с характерным резким запахом.
Получение NH3
1. В лаборатории NH3получают, нагревая смесь хлористого аммония с гашёной известью.
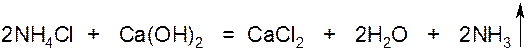
2. Промышленный способ получения NH3 -синтезом из азота и водорода над катализатором (катализатор – железо).

Раствор аммиака в воде называют нашатырным спиртом.


Химические свойства аммиака NH3
В аммиаке NH3 азот достигает низшей степени окисления (-3), поэтому он обладает только восстановительными свойствами.
1. Аммиак NH3 сгорает в кислороде и в воздухе:

2. Взаимодействует с хлором и с бромом:

3. Взаимодействует с окисью меди (с помощью этой реакции получают азот в лаборатории):
