 |
|
Термодинамическая система. Термодинамические состояние и процесс
Термодинамической системой называется совокупность макроскопических тел, которые могут обмениваться энергией как друг с другом, так и с внешней средой.
Термодинамические параметры – это физические величины, характеризующие термодинамическое состояние системы.
Основные термодинамические параметры:
1). Объём
Объём V(м3) – очевидный параметр.
Иногда используют понятие «удельный объем» тела – величина, равная отношению объёма к его массе:  =
=  ,
,  . Величина, обратная удельному объёму называется плотностью тела:
. Величина, обратная удельному объёму называется плотностью тела:  =
=  ,
,  .
.
2). Давление
Давлением Р – называется скалярная величина, равная, отношению нормально направленной силы Fn к площади поверхности S, на которую действует эта сила: P = 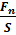 , Па.
, Па.
В МКТ давление – это усреднённая сила удара молекул о стенки сосуда.
3). Температура
Температура характеризует степень нагретости тел, является мерой интенсивности теплового движения молекул (атомов) тела.
В СИ термодинамическая (абсолютная) температура Т измеряется в Кельвинах: Т =(t0C + 273,15), К.
Абсолютный нуль температур Т = 0 К на практике не достижим.
Во всех частях термодинамической системы, находящейся в равновесии, температура одинакова.
Другие термодинамические параметры: плотность, теплоёмкость, удельное электросопротивление и др.
Два состояния системы считаются разными, если для них неодинаковы значения хотя бы одного из термодинамических параметров.
Равновесное состояние (состояние термодинамического равновесия) – состояние системы, при котором все её параметры остаются неизменными при неизменных внешних параметрах сколь угодно долго.
Если какой-то параметр системы изменяет своё значение, то состояние будет неравновесным.
Понятие «равновесное состояние» - идеализация.
Термодинамическим процессом называется процесс изменения состояния термодинамической системы.
Всякий термодинамический процесс связан с нарушением равновесия системы. Однако, если этот процесс протекает бесконечно медленно, то такой процесс можно считать практически равновесным (квазистатическим).
Все реальные процессы неравновесные, т.к. протекают с конечной скоростью.
Виды термодинамических процессов
Изопроцессы – это термодинамические процессы, происходящие в системе с постоянной массой (m = const) при каком-либо постоянном параметре:
· T = const – изотермический;
· V = const – изохорический (изохорный);
· P = const – изобарический (изобарный).
Адиабатический (адиабатный) процесс – процесс, который происходит в термодинамической системе без теплообмена с внешними телами (  .
.
Адиабатный процесс – идеализация, их реально не существует. Однако многие быстро протекающие процессы можно считать практически адиабатными, т.к. за время такого процесса существенный теплообмен с внешней средой произойти не успевает.