 |
|
Перерахунок концентрацій
Визначення молярної і нормальної концентрацій за відомою процентною концентрацією розчину
Процентна концентрація розчину показує вміст розчиненої речовини в 100 г розчину, а молярна і нормальна – в 1 л розчину.
Необхідно вирахувати:
- масу розчиненої речовини в 1 л розчину  ;
;
- масу розчину (  );
);
- кількість моль розчиненої речовини  або кількість його еквівалентів
або кількість його еквівалентів 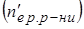 в 1 л розчину, що відповідає
в 1 л розчину, що відповідає  і
і  розчину.
розчину.
У загальному вигляді

| Приклад
 % %  г/мл г/мл
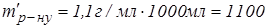 г г
|
Складаємо пропорцію:
100 г розчину — Ср г р.р-ни


| Складаємо пропорцію:
100 г р-ну – 5 г  1100 г р-ну –
1100 г р-ну –  г г 
 г г
|


|  г/моль г/моль

|

| 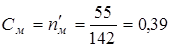 моль/л моль/л
|

|  моль/л моль/л
|
Визначення моляльної концентрації за відомою процентною концентрацією розчину
Моляльна концентрація  розраховується на 1000 г розчинника. Отже, при розрахунку моляльної концентрації необхідно спочатку перейти від маси розчину до маси розчинника. Наприклад, дається 20%-ний розчин
розраховується на 1000 г розчинника. Отже, при розрахунку моляльної концентрації необхідно спочатку перейти від маси розчину до маси розчинника. Наприклад, дається 20%-ний розчин  . Це, з одного боку, означає, що 20 г
. Це, з одного боку, означає, що 20 г  знаходиться в 100 г розчину, а з другого, – що 100 г розчину складається із 20 г
знаходиться в 100 г розчину, а з другого, – що 100 г розчину складається із 20 г  і 80 г
і 80 г 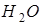 . Останнє трактування дозволяє скласти пропорцію, необхідну для розрахування моляльної концентрації:
. Останнє трактування дозволяє скласти пропорцію, необхідну для розрахування моляльної концентрації:
20 г  – 80 г
– 80 г 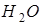
Х – 1000 г 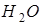
 г.
г.
Вираховуємо  , тобто кількість моль
, тобто кількість моль  у 1000 г води, знаючи, що
у 1000 г води, знаючи, що  =39+127=166 г/моль.
=39+127=166 г/моль.
 моль.
моль.
Розрахування титру розчину за його відомою процентною концентрацією
Титр вираховується на 1 мл розчину. Тому для переходу від процентної концентрації до титру спершу потрібно вирахувати об’єм 100 г розчину, використовуючи значення насиченості цього розчину:
 .
.
Після цього титр розчину можна знайти за пропорцією
 містить Ср г р.р-ну
містить Ср г р.р-ну
1 мл – Х
 .
.
Приклад. Вирахувати титр 40 %-ного розчину  , густина якого дорівнює 1,307 г/мл.
, густина якого дорівнює 1,307 г/мл.
Розв’язування. Об’єм 100 г розчину обраховуємо, використовуючи значення його густини:
 мл.
мл.
Складаємо пропорцію:
У 76,7 мл знаходиться 40 г 
1 мл – 
 г/мл.
г/мл.